1.6. Сопряжение возбуждения и сокращения в миокарде
Фундаментальные свойства миокарда (возбудимость, проводимость и автоматия) обеспечивают его сократимость – способность мышечных волокон укорачиваться или увеличивать свое напряжение. В соответствии с теорией «скользящих нитей», предложенной X. Хаксли и А. Хаксли еще в 1950-х гг., при сокращении миофибрилл происходит укорочение саркомера, то есть уменьшение его продольного размера вследствие активного перемещения актиновых нитей относительно миозиновых. При этом длина нитей не изменяется. Молекулярными исследованиями 1970–1980-х гг. установлено, что актиновые нити скользят вдоль миозиновых благодаря «гребковым» движениям головок миозина. Головка прикрепляется к участку связывания на актине, потом наклоняется, вызывая укорочение саркомера, и отсоединяется от актина. Далее головка прикрепляется к следующему участку связывания на актиновой нити, и цикл повторяется. При этом сила сокращения определяется количеством связей (мостиков) между миозином и актином.
В расслабленном миокарде соединению миозина и актина препятствуют молекулы тропонина, «закрывающие» участки связывания на актиновой нити. Однако при повышении концентрации кальция в цитоплазме, что имеет место во время возбуждения кардиомиоцита, ионы кальция соединяются с тропонином С. Присоединение Са2+ к этому белку приводит к конформационным изменениям тропонин-тропомиозинового комплекса. В результате молекулы тропомиозина смещаются, миозиновые и актиновые нити вступают во взаимодействие, и начинается процесс сокращения. Чем больше ионов Са2+ поступит к миофибриллам при возбуждении, тем большее количество актомиозиновых мостиков будет образовываться, и тем сильнее, следовательно, будет сокращение. Таким образом, повышение концентрации ионов Са2+ в цитоплазме кардиомиоцита является ключевым фактором, обеспечивающим электромеханическое сопряжение – связь между возбуждением и сокращением миокарда.
Исследования, проведенные в 1980–1990-е гг., позволили установить, что на мембране Т-трубочек поверхностной мембраны кардиомиоцитов имеется кальциевый потенциалзависимый канал, который блокируется препаратами из группы дигидропиридинов. Поэтому он получил название дигидропиридинового рецептора (DHPR). На мембране терминальных цистерн саркоплазматического ретикулума расположен другой потенциалзависимый кальциевый канал, проницаемость которого модулируется растительным алкалоидом рианодином, поэтому он получил название рианодинового рецептора (RyaR). Кроме того, с последним, возможно, связан белок кальмодулин, конформационные изменения которого могут приводить к активации рианодинового рецептора и выходу ионов кальция из цистерн саркоплазматического ретикулума. По другим данным, рианодиновые рецепторы непосредственно активируются ионами кальция (рис. 7).
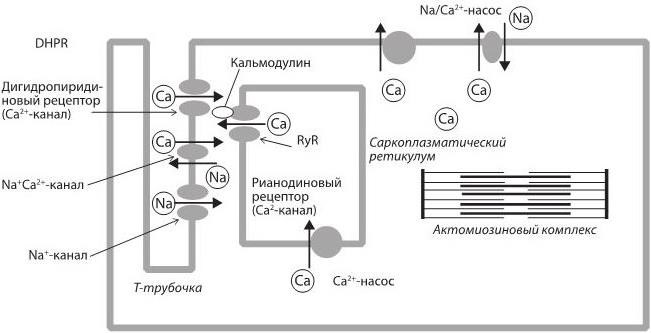
Рис. 7. Транспорт ионов кальция в процессах сопряжения возбуждения и сокращения в сердечной мышце
Электромеханическое сопряжение в кардиомиоците начинается с возникновения фазы 0 потенциала действия на плазматической мембране. Когда мембранный потенциал достигает уровня –65 мВ, открываются потенциалзависимые Са2+-каналы L-типа, обеспечивающие формирование входящего ICa2+L тока, который ускоряет деполяризацию кардиомиоцитов. В результате активируются потенциалзависимые кальциевые ионные каналы мембраны T-трубочек (дигидропиридиновый рецептор), через которые ионы кальция поступают внутрь кардиомиоцитов. «Внешние» ионы кальция взаимодействуют (прямо или через посредство кальмодулина) с рианодиновыми рецепторами саркоплазматического ретикулума. Вследствие этого кальциевые ионные каналы саркоплазматического ретикулума открываются, и кальций начинает поступать из мембранных цистерн в цитоплазму кардиомиоцита. В результате концентрация кальция в цитоплазме клетки возрастает с менее чем 10-7 М/л до 10-5 М/л. Резкое повышение концентрации ионов Са2+ в саркоплазме устраняет тропомиозиновую блокаду взаимодействия актина и миозина и запускает процесс сокращения кардиомиоцитов.
Таким образом, поступление «внешних», или триггерных, ионов кальция вызывает высвобождение «внутренних» ионов кальция из саркоплазматического ретикулума. Такой процесс получил название кальций-индуцированного высвобождения кальция. Важно подчеркнуть, что чем более выраженным будет поступление внешних ионов кальция в цитоплазму кардиомиоцита, тем в большей степени будет возрастать количество ионов кальция, выходящих из саркоплазматического ретикулума. Поскольку входящий кальциевый ток ICa2+L достигает максимальной величины во время фазы 2 (плато) потенциала действия рабочего кардиомиоцита, длительность именно этой фазы в норме определяет силу сокращения миокарда. Следовательно, сократимость сердечной мышцы непосредственно зависит от силы входящего кальциевого тока (ICa2+L), которая может возрастать, например, под влиянием катехоламинов, влияющих на степень открытия кальциевых каналов L-типа. Наряду с этим поступление в цитоплазму внешних ионов кальция восполняет запасы кальция в цистернах саркоплазматического ретикулума, что в итоге также влияет на сократимость миокарда.
Существует и другой механизм поступления больших количеств ионов Са2+ в цитоплазму рабочего кардиомиоцита при его возбуждении. Он обеспечивается сопряженным транспортом ионов кальция и натрия через мембрану, то есть Са2+/Na+-обменом. Во время диастолы Са2+/Na+-насос активно удаляет из клетки ионы Са2+ в обмен на ионы Na+. При возбуждении кардиомиоцита направление Са2+/Na+-обмена меняется на противоположное: ионы Са2+ активно переносятся в клетку, тогда как ионы Na+, напротив, удаляются, и в результате концентрация ионов кальция в цитоплазме кардиомиоцита возрастает.
Нарушение процесса электромеханического сопряжения при патологии сердца может привести к тому, что потенциалы действия, продолжая возникать в синусовом узле и распространяться по проводящей системе к рабочему миокарду, не вызывают его сокращения. Отсутствие сократительной функции миокарда приводит к остановке кровообращения. Однако электрическая активность сердца может быть выявлена, например, с помощью регистрации электрокардиограммы. Такое состояние называется электромеханической диссоциацией и может явиться одной из непосредственных причин смерти, например при инфаркте миокарда.
Снижение сократимости миокарда является одной из основных причин развития сердечной недостаточности – состояния, при котором нарушаются гемодинамическая функция сердца и нормальное кровоснабжение органов и тканей. В клинической практике для лечения сердечной недостаточности применяют сердечные гликозиды – вещества, выделенные из таких растений, как наперстянка (дигиталис), строфант, ландыш и др. (Впервые в клиническую практику препараты наперстянки были внедрены английским врачом В. Уитерингом еще в 1785 г.) Как показали физиологические и фармакологические исследования, проведенные в середине 1970–1980-х гг., механизм действия этих препаратов обусловлен их способностью влиять на работу К+/Na+-насоса мембран кардиомиоцитов, а также метаболизм миокарда. В малых терапевтических дозах сердечные гликозиды усиливают работу К+/Na+-насоса, что отчасти увеличивает концентрацию ионов калия в клетках, вызывая увеличение его сократимости.
В средних и высоких терапевтических дозах данные препараты, напротив, угнетают К+/Na+-насос мембраны кардиомиоцитов, что приводит к возрастанию внутриклеточной концентрации Na+ и усилению поступления ионов Са2+ в клетку по механизму Са2+/Na+-обмена (как в покое, так и при возбуждении). В результате увеличивается продолжительность фазы плато потенциала действия рабочего кардиомиоцита, а следовательно, еще больше возрастает сократимость миокарда.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.