Гормоны при стрессе
Гормоны при стрессе
Любое воздействие на организм приводит прежде всего к активации симпатической нервной системы, в результате чего усиливается выделение адреналина из мозгового слоя надпочечников и норадреналина из нервных окончаний в стенках сосудов. Следует подчеркнуть, что многочисленные взаимные влияния между симпато-адреналовой системой и гипофиз-адреналовой системой существуют как на уровне надпочечника, так и на гипоталамо-гипофизарном уровне. Например, активировать симпато-адреналовую систему может и кортиколиберин, секреция которого надпочечниками индуцируется симпатической нервной системой.
Когда животное подвергается стрессорному воздействию, активируются многочисленные пути в ЦНС, в результате чего стимулируются синтез и секреция кортиколиберина в гипоталамусе. Кортиколиберин, выделяясь из нервных окончаний в портальную систему, достигает клеток гипофиза, которые синтезируют АКТГ и эндорфины. Из гипоталамуса выделяются и другие гормоны, стимулирующие секрецию АКТГ, – вазопрессин и окситоцин.
Следует отметить их влияние на стимулирующий эффект кортиколиберина на секрецию АКТГ. Вазопрессин сам по себе незначительно увеличивает секрецию АКТГ, но усиливает действие кортиколиберина на гипофиз. В малых дозах окситоцин тормозит секрецию АКТГ у человека, а в больших – увеличивает ее. Секреция вазопрессина и окситоцина зависит от типа воздействия. У крыс окситоцин может быть важным стрессорным фактором реакции на новизну. При социальной изоляции секреция вазопрессина возрастает у многих, но не у всех видов животных, а секреция окситоцина не меняется. При ограничении подвижности на секрецию АКТГ влияет окситоцин, но не влияет вазопрессин. Если ограничение свободы движений связано с умеренным физическим воздействием и жестким обездвиживанием, на секрецию АКТГ влияют оба гормона.
АКТГ стимулирует продукцию глюкокортикоидов корковым слоем надпочечников. Кортиколиберин может стимулировать выделение глюкокортикоидов корковым слоем надпочечников, воздействуя на их мозговой слой и стимулируя в нем образование АКТГ. Кроме АКТГ, непосредственно на корковый слой надпочечников способны влиять вазопрессин и окситоцин. Синтез стероидов в коре надпочечников может стимулироваться и некоторыми другими гормонами. Кроме этого, существуют и другие, не вполне пока понятные механизмы активации синтеза и секреции глюкокортикоидов, в которых участвуют клетки крови.
Стадия аларм-реакции отличается от стадии резистентности избытком адреналина при недостатке глюкокортикоидов
Следует подчеркнуть разную скорость работы симпато-адреналовой и гипофиз-адреналовой систем. Адреналин начинает выделяться в первые секунды воздействия, так как его секреция управляется нервными импульсами. Так же быстро по окончании воздействия происходит исчезновение адреналина, который метаболизируется ферментами крови. Кортизол лишь через несколько минут начинает выделяться корой надпочечников, так как управляется гуморальными сигналами. Так же медленно выводится он из крови, так как инактивирующие его ферменты находятся в клетках печени. В результате в первые минуты стресса организм «залит» адреналином, и только спустя примерно десять минут адреналиновый пожар начинают гасить глюкокортикоиды. При сильных воздействиях б?льшая часть животных гибнет в первые же минуты, когда глюкокортикоиды еще не успели поступить в кровь и достичь органов-мишеней.
Секреция кортизола (у человека, обезьяны, собаки) и кортикостерона (у крыс и мышей) регулируется по механизму отрицательной обратной связи. При этом глюкокортикоидные гормоны воздействуют на клетки гипофиза, гипоталамуса и экстрагипоталамических структур, в первую очередь гиппокампа.
Две основные эндокринные стрессорные системы: симпато-адреналовая и гипофиз-адреналовая. Адреналин – основной гормон симпато-адреналовой системы. К гипофиз-адреналовой относятся: кортиколиберин, АКТГ, глюкокортикоиды, эндогенные опиаты, а также вазопрессин и окситоцин
Глюкокортикоиды тормозят синтез и секрецию кортиколиберина, АКТГ, но не синтез вазопрессина, который выделяется в системный кровоток.
Активация симпато-адреналовой системы и гипофиз-адреналовой системы, в результате которой в системный кровоток выделяются значительные количества АКТГ, глюкокортикоидов, адреналина и норадреналина, ведет к изменениям в обмене веществ и в поведении. Основным аспектом метаболического ответа является быстрое увеличение доступности биохимических субстратов для реакций обмена веществ. Это происходит под влиянием глюкокортикоидных гормонов. Под действием АКТГ и глюкокортикоидов возрастает распад жиров и белков, интенсифицируется глюконеогенез, увеличивается потребление глюкозы клетками, а синтез белков тормозится. Повышенная концентрация адреналина в крови также увеличивает поступление к клеткам энергетического субстрата и кислорода, стимулируя частоту сердечных сокращений и артериальное кровяное давление, а также липолиз и гликогенолиз. Кроме того, при стрессе изменяется секреция многих других гормонов.
Глюкокортикоиды оказывают разнообразное действие практически на все ткани организма. Их главная функция – усиление его сопротивляемости при длительном действии стрессора, а также перераспределение адаптивного потенциала организма. Таким образом, с одной стороны, глюкокортикоиды регулируют основную адаптивную функцию организма, а с другой – избыточная концентрация глюкокортикоидов в крови может быть вредной для него. Повышенный уровень глюкокортикоидов может вызывать сердечно-сосудистые, почечные, ревматические и психические заболевания. Эта группа получила название болезней адаптации. Таким образом, теория стресса тесно связана с проблемой возникновения болезней.
В последние годы появились экспериментальные доказательства того, что основная функция глюкокортикоидов заключается не только в увеличении резистентности к повреждающему воздействию, а в торможении других компонентов стрессорного ответа, в частности активности стрессорных медиаторных систем ЦНС. При этом особую актуальность приобретает проблема кортикостероидных рецепторов, в первую очередь находящихся в гипофизе и ЦНС.
Впервые клеточные рецепторы глюкокортикоидов были обнаружены в 1968 г. Брюсом Макюеном (McEwen), который показал, что глюкокортикоиды, проникая в мозг, связываются с белковыми молекулами. В настоящее время насчитывается четыре типа рецепторов. Два первых типа локализованы в цитоплазме клетки, а третий и четвертый – в клеточной мембране. Молекулярные механизмы функционирования рецепторов прямо не касаются предмета настоящей работы, поэтому здесь не рассматриваются.
Основные изменения в эндокринной системе при стрессе представлены на рис. 4.16. Обратите внимание на то, что прямой психотропный эффект есть у всех приведенных в таблице гормонов, за исключением адреналина. Его влияние на психику вторично, оно определяется условным рефлексом на висцеральные изменения при стрессе. Адреналин вызывает сердцебиение, сухость во рту, дрожание рук и прочие висцеральные реакции, которые у всех людей ассоциируются с чувством тревоги. Если испытуемого предупредить, что вводимый препарат вызовет сердцебиение и т. п., то он не сообщает о чувстве тревоги или беспокойстве.
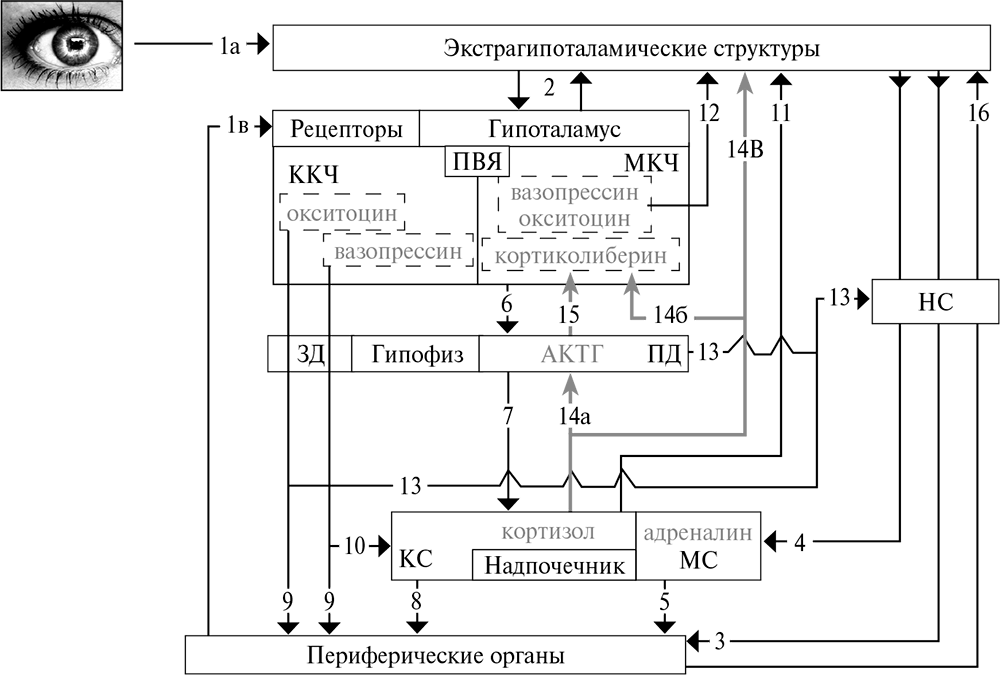
Рис. 4.16. Схема эндокринной системы при стрессе: НС – нервная система, ПВЯ – паравентрикулярное ядро гипоталамуса, МКЧ – мелкоклеточная часть ПВЯ, ККЧ – крупноклеточная часть ПВЯ, ПД – передняя доля гипофиза, ЗД – задняя доля гипофиза, МС – мозговой слой надпочечников, КС – корковый слой надпочечников.
1 – Информация об изменениях:
а – внешней среды;
б – внутренней среды, нервный сигнал;
в – внутренней среды, гуморальный сигнал.
2 – Связи гипоталамуса с другими отделами ЦНС.
3 – Нервные сигналы из ЦНС к периферическим органам.
4 – Нервный сигнал к мозговому слою надпочечника (МС).
5 – Гуморальный сигнал от МС к периферическим органам.
6 – Гуморальный сигнал от гипоталамуса к передней доле гипофиза через портальную сосудистую систему.
7 – Гуморальный сигнал от передней доли гипофиза к КС.
8 – Гуморальный сигнал от КС к периферическим органам.
9 – Гуморальный сигнал от гипоталамуса, через ЗДГ.
10 – Гуморальный сигнал от вазопрессинергических нейронов к КС.
11 – Гуморальные сигналы коры надпочечника в ЦНС.
12 – Нервные сигналы от пептидергических (секретирующих пептиды, которые выполняют функции медиаторов, т. е. выделяются в синаптическом окончании отростков нервной клетки) нейронов гипоталамуса в ЦНС.
13 – Гуморальные сигналы в ЦНС через периферические ганглии.
14 – Сигналы отрицательной обратной связи:
а – в гипофиз;
б – в гипоталамус;
в – в экстрагипоталамические структуры (гиппокамп).
15 – Сигнал короткой отрицательной обратной связи.
Основные данные по эндокринологии стресса получены в экспериментах на животных. Сложности постановки опыта на человеке уже были перечислены. Таким образом, данных об изменении гормональных показателей у человека немного. Имеющиеся результаты ни в чем не противоречат схемам, составленным на основании исследований животных. На рис. 4.17 показано изменение содержания АКТГ и кортизола в крови здоровых испытуемых после введения 100 микрограмм кортиколиберина. Следует обратить внимание на разную динамику двух гормонов. Постоянные времени для гипофизарного АКТГ меньше, чем для кортизола, секретируемого корой надпочечников.
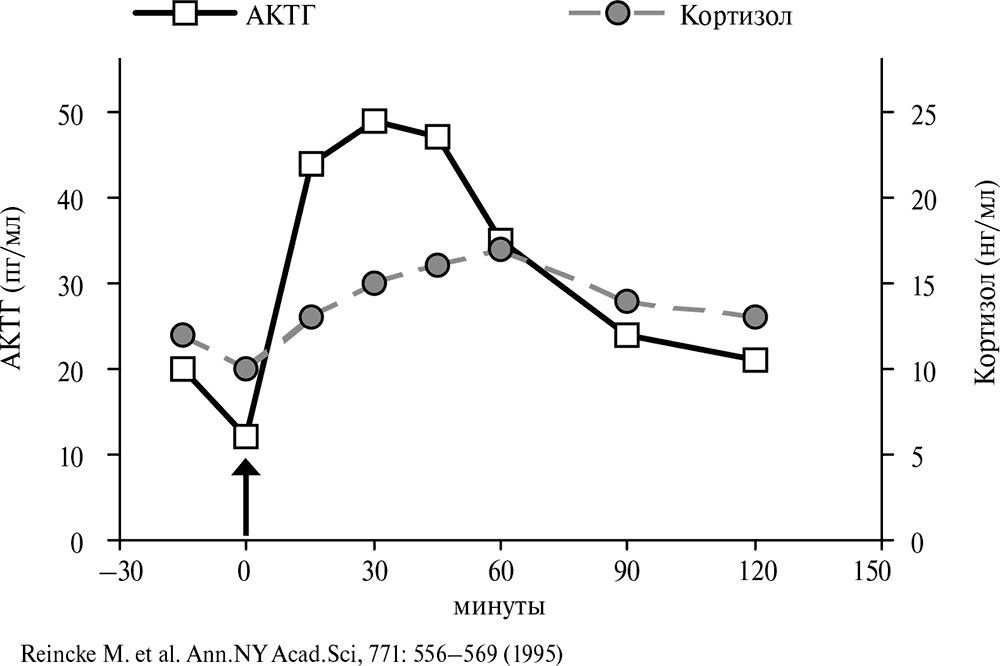
Рис. 4.17. Реакция человека на введение кортиколиберина[118]. По оси абсцисс отложено время. Стрелкой показан момент введения кортиколиберина. Обратите внимание на разные постоянные времени для АКТГ и кортизола
На рис. 4.18 показаны некоторые стрессорные реакции крысы на незнакомую обстановку. Следует обратить внимание на совпадение кривых для артериального давления, частоты сердечных сокращений и норадреналина, который попадает в кровь, главным образом выделяясь из нервных окончаний в мышцах. Сопоставьте динамику адреналина, АКТГ и кортикостерона.
Динамика некоторых стрессорных реакций на новую обстановку: крысу помещали в незнакомую большую пустую клетку на 5 мин. (показано прямоугольником на оси абсцисс)
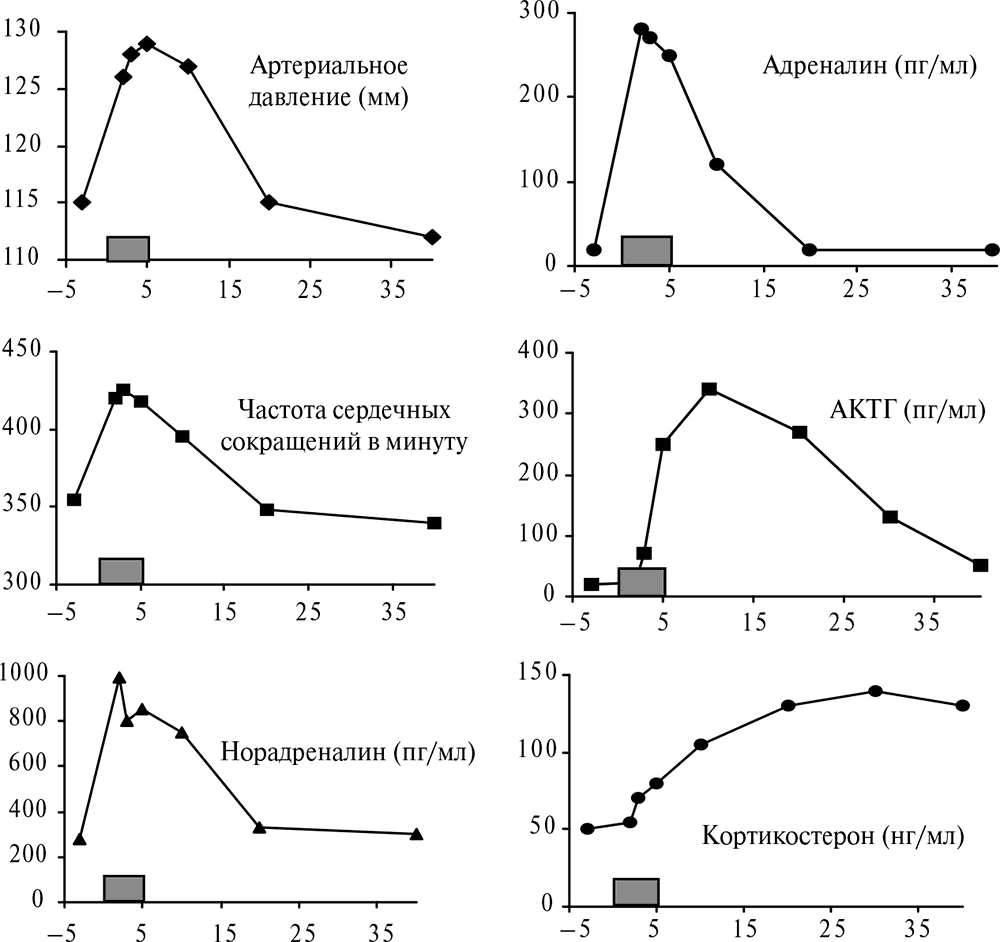
Рис. 4.18. Здесь показаны некоторые стрессорные реакции крысы на незнакомую обстановку. Следует обратить внимание на совпадение кривых для артериального давления, частоты сердечных сокращений и норадреналина, который попадает в кровь, главным образом выделяясь из нервных окончаний в мышцах. Сопоставьте динамику адреналина, АКТГ и кортикостерона
Принципиальным в регуляции стрессорной реакции является отсутствие гормона, который тормозит данную стрессорную реакцию. Поиск такого гормона вели многие исследовательские группы, и не одно десятилетие. На возможность наличия такого гормона указывало существование среди гипоталамических рилизинг-гормонов как либеринов, так и статинов. Либерины стимулируют синтез и секрецию гипофизарных гормонов, а статины (которые не рассматриваются в данной книге) их тормозят. Например, синтез и секреция таких гипофизарных гормонов, как гормон роста, пролактин и меланотропин, регулируется гипоталамическими либерином и статином. Таким образом, логично было бы предположить, что и АКТГ имеет свой гипоталамический статин.
Единственным механизмом торможения стрессорной реакции является механизм обратной связи. Он обеспечивается рецепторами глюкокортикоидных гормонов в центральной нервной системе
Активность поисков «кортикостатина» стимулируется тем, что такое вещество послужило бы основой для создания ценнейшего лекарственного препарата, который принес бы его производителям огромную прибыль. Многие болезни развиваются в результате того, что стрессорная реакция, в частности повышенный уровень глюкокортикоидов в крови, сохраняется и тогда, когда стимул, вызвавший ее, уже отсутствует. Эти болезни так и называются – болезни стресса. К их числу относится и депрессия, которая будет подробно рассмотрена в главе 5. Таким образом, открытие «кортикостатина» позволило бы понижать уровень стрессорных гормонов так же легко, как теперь с помощью глюкокортикоидов можно понижать интенсивность воспалительных процессов.
К сожалению, поиски «кортикостатина» можно уподобить ловле черного кота в темной комнате с периодическими возгласами «Ага, попался!». Было обнаружено множество гуморальных факторов, которые ослабляют действие кортиколиберина на гипофиз. Тем не менее среди них не оказалось ни одного вещества, которое бы тормозило синтез и секрецию АКТГ и выделялось спустя какое-то время после начала стрессорной реакции (что указывало бы на него как на фактор, тормозящий стресс).
Единственный механизм торможения стрессорной реакции – механизм отрицательной обратной связи. Глюкокортикоидные гормоны воздействуют на клетки гипофиза и гипоталамуса и тормозят в них синтез и секрецию АКТГ и кортиколиберина соответственно. Кроме того, в регуляции гипофиз-адреналовой системы по механизму отрицательной обратной связи большую роль играют другие структуры ЦНС, в первую очередь гиппокамп.
Нарушение механизмов регуляции по отрицательной обратной связи внутри гипофиз-адреналовой системы приводит к тому, что незначительные стрессорные стимулы или даже простая мышечная нагрузка вызывают стойкое и длительное повышение секреции глюкокортикоидных гормонов. Как всякое нарушение равновесия организма (а может быть, и больше, чем любое другое), длительно повышенный уровень секреции глюкокортикоидов ведет к возникновению заболеваний. Пагубные последствия нарушения торможения стрессорной реакции по механизму отрицательной обратной связи будут рассмотрены в главах 5 и 6.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
4. Другие гормоны
4. Другие гормоны Тироксин (или, точнее, тироксины) представляет собой низкомолекулярное соединение, состоящее из двух молекул тирозина, к которым присоединено несколько атомов йода. Поэтому нехватка йода в пище приводит в некоторых горных районах к тяжелой болезни
Половые гормоны
Половые гормоны До сих пор мы говорили об анатомическом проявлении циклических изменений в органах размножения. У лабораторных животных их можно наблюдать под микроскопом на препарированных органах, у человека их изучают в основном на трупах, например на органах людей,
Гормоны гипоталамуса
Гормоны гипоталамуса ЦНС оказывает регулирующее действие на эндокринную систему через гипоталамус. В клетках нейронов гипоталамуса синтезируются пептидные гормоны двух типов. Одни через систему гипоталамо-гипофизарных сосудов поступают в переднюю долю гипофиза, где
Гормоны гипофиза
Гормоны гипофиза В передней доле гипофиза (аденогипофизе) синтезируются тропные гормоны, стимулирующие синтез и секрецию гормонов периферических эндокринных желёз. По химическому строению гормоны гипофиза являются пептидами или гликопротеинами.Кортикотропин (АКТГ,
Гормоны надпочечников
Гормоны надпочечников Гормоны мозгового вещества надпочечников В мозговом веществе надпочечников в хромаффинных клетках синтезируются катехоламины – дофамин, адреналин и норадреналин. Непосредственным предшественником катехоламинов является тирозин. Норадреналин
Что такое гормоны?
Что такое гормоны? Гормонами называют биологически активные вещества, выделяемые железами внутренней секреции или скоплениями специализированных клеток организма и оказывающие целенаправленное действие на другие органы и ткани. Под контролем гормонов протекают все
Периферические гормоны
Периферические гормоны В этом разделе будут рассмотрены локализация, функции, регуляция синтеза и секреции гормонов периферических желез. Расположение основных желез в теле человека показано на рис. 2.3. Рис. 2.3. Схема расположения основных желез в теле человека Масса
Стероидные гормоны
Стероидные гормоны Все вышеперечисленные гормоны относятся к пептидам. Периферические гормоны, продуцируемые корой надпочечников и половыми железами, относятся к химическому классу стероидов.Стероиды отличаются от пептидов не только химически, но и физиологически.
Поведение при стрессе
Поведение при стрессе Вспомним, как формируется поведенческий акт (см. главу 2). Изменения в среде вызывают определенную потребность, для удовлетворения которой человек или животное должны либо попытаться возвратить среду к прежнему состоянию, либо приспособиться к
Универсальная форма поведения при стрессе – смещенная активность
Универсальная форма поведения при стрессе – смещенная активность Понятие смещенной активности было сформулировано Николасом Тинбергеном[103]. Он писал, что при смещенной активности энергия, накопленная внутри одной мотивации, разряжается в виде ФКД другой мотивации.
Гормоны коры надпочечников
Гормоны коры надпочечников В экспериментах на животных не было обнаружено отчетливого поведенческого эффекта кортикостероидов (т. е. глюкокортикоидов и минералокортикоидов), в противоположность другим гормонам гипофиз-адреналовой системы. В частности, ни скорость
Гормоны и депрессия
Гормоны и депрессия Если гуморальные факторы, модулирующие тревожные состояния, достаточно хорошо известны (табл. 5.1), то «гормон депрессии» остается загадкой. Не вызывает сомнения, что гормоны участвуют в патогенезе депрессивных состояний.Таблица 5.1. Гормоны при
Гормоны и социальный ранг
Гормоны и социальный ранг Какие гормоны определяют положение особи в иерархии? Это неизвестно. По всей вероятности, гормональный профиль не определяет, а только отражает позицию индивида в социальной структуре сообщества.Можно составить популяции из крыс только
Мужчины лучше действуют при стрессе
Мужчины лучше действуют при стрессе Услышав, что не нужно тревожиться, они, как подобает разумным женщинам, немедленно ударились в панику. Вашингтон Ирвинг На сайте «Антитеррор» (http://antiterror.condoleeza.ru/psych/adekvat.html) размещена следующая рекомендация. Чтобы действовать адекватно
Гормоны и мозг
Гормоны и мозг В определенном смысле, причина межполовых различий — не в том, что у женщин и мужчин гены поведения сами по себе разные. Допустим, у плейстоценового мужчины возникает ген, улучшающий чувство направления, но при этом ухудшающий социальную интуицию. Ему он