Глава 11. Типы окисления. Антиоксидантные системы
Глава 11. Типы окисления. Антиоксидантные системы
Все реакции с участием кислорода, протекающие в живом организме, называются биологическим окислением. Почти во всех клетках около 90 % потребляемого кислорода восстанавливается в цепи тканевого дыхания с участием цитохромоксидазы (окисление, сопряженное с фосфорилированием АТФ, выполняет энергетическую функцию). Однако в некоторых тканях содержатся ферменты, катализирующие окислительно-восстановительные реакции, в которых атомы кислорода включаются непосредственно в молекулу субстрата (свободное окисление, выполняет пластическую функцию). Хотя в таких специализированных реакциях потребляется лишь небольшая часть кислорода, поглощаемого клетками, эти реакции очень важны для организма.
Выделяют четыре типа реакций с участием кислорода (табл 11.1.).
Таблица 11.1. Типы окисления
Тип окисления Ферменты Основные продукты реакции оксидазный Оксидазы S + Н2О пероксидазный ФАД-зависимые оксидазы S + Н2О2 диоксигеназный Диоксигеназы SO2 монооксигеназный Монооксигеназы (гидроксилазы) SOH + H2OОксидазный тип окисления
Этот путь окисления осуществляется в процессе функционирования ЦТД. Терминальный фермент ЦТД, переносящий электроны непосредственно на кислород – цитохромоксидаза. Это основной путь потребления кислорода в организме. Он выполняет энергетическую функцию.
Пероксидазный тип окисления
Окисление субстрата путем дегидрирования. Два атома водорода переносятся на молекулу кислорода с образованием перекиси:
ФАД-зависимая оксидаза
SН2 + О2 ? S + Н2О2
В этой реакции энергия окисления выделяется в виде тепла. Реакции этого типа катализируют ФАД-зависимые оксидазы (аэробные дегидрогеназы), содержащие в качестве простетической группы ФАД или ФМН. В клетке около 80 % этих ферментов сосредоточено в пероксисомах. Пероксидазный путь окисления активно протекает в лейкоцитах, макрофагах и других фагоцитирующих клетках. Образующийся пероксид водорода Н2О2 – сильный окислитель, обезвреживающий патогенные бактерии (защитная функция).
Реакция пероксидазного окисления протекает в 2 стадии:
1. Анаэробная - происходит дегидрирование восстановленного субстрата SH2, при этом протоны и электроны переносятся на ФАД (ФАД + 2Н+ ? ФАДН2).
2. Аэробная - происходит окисление фермента (ФАДН2 ? ФАД) кислородом (самопроизвольный процесс).
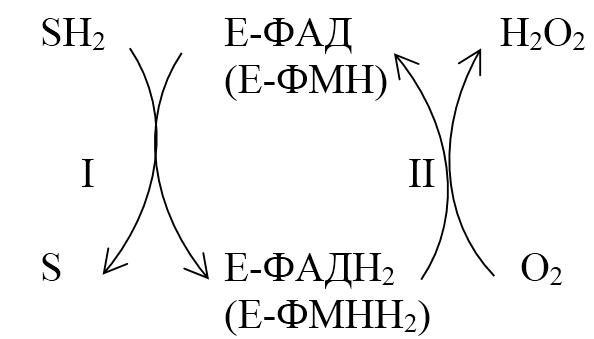
Биологическая роль оксидазного типа окисления:
1. защитная функция – в лейкоцитах и других фагоцитирующих клетках;
2. катаболизм биогенных аминов (фермент – моноаминооксидаза);
3. метаболизм аминокислот (ферменты – оксидазы D- и L-аминокислот);
4. катаболизм пуринов (фермент – ксантиноксидаза);
5. катаболизм глюкозы в растительных клетках (фермент – глюкозооксидаза).
Диоксигеназный тип окисления
В процессе диоксигеназного окисления в молекулу субстрата включаются оба атома кислорода:
Диоксигеназа
S + O2 ? SO2
Диоксигеназы катализируют разрыв двойной связи в ароматическом кольце. Например: гомогентизатоксидаза катализирует расщепление ароматического кольца гомогентизиновой кислоты с образованием малеилацетоацетата.
Монооксигеназный тип окисления
Монооксигеназы (гидроксилазы) катализируют включение в субстрат одного атома молекулы кислорода. Другой атом кислорода восстанавливается до воды. Для работы монооксигеназной системы необходим кроме неполярного субстрата (SH) донор атомов водорода – косубстрат (НАДФН+Н+, ФАДН2, аскорбиновая кислота):
Гидроксил
SH + НАДФН+Н++ О2 ? SОН + НАДФ+ + Н2О
Монооксигеназные реакции необходимы для:
1. специфических превращений аминокислот, например, для синтеза тирозина из фенилаланина (фермент – фенилаланингидроксилаза);
2. синтеза холестерола, желчных кислот в печени; стероидных гормонов в коре надпочечников, яичниках, плаценте, семенниках; витамина D3 в почках;
3. обезвреживания чужеродных веществ (ксенобиотиков) в печени.
Ферменты монооксигеназного пути окисления локализованы в мембранах эндоплазматического ретикулума (при гомогенизации тканей эти мембраны превращаются в микросомы – мембранные пузырьки). Поэтому монооксигеназный путь окисления называют микросомальным окислением.
Микросомальное окисление представляет короткую электронтранспортную цепь, включающую НАДФ, ФАД, ФМН, цитохром Р450.

Микросомальная система включает два фермента: цитохром Р450 и НАДФН-цитохром-Р450-редуктазу.
НАДФН-цитохром Р450 – редуктаза – флавопротеин, в качестве простетической группы содержит два кофермента ФАД и ФМН.
Цитохром Р450 – гемопротеин, содержит простетическую группу гем и участки связывания для кислорода и субстрата. Восстановленный цитохром Р450 имеет максимум поглощения при 450 нм. Выполняет две функции: связывание окисляемого субстрата и активация молекулярного кислорода.
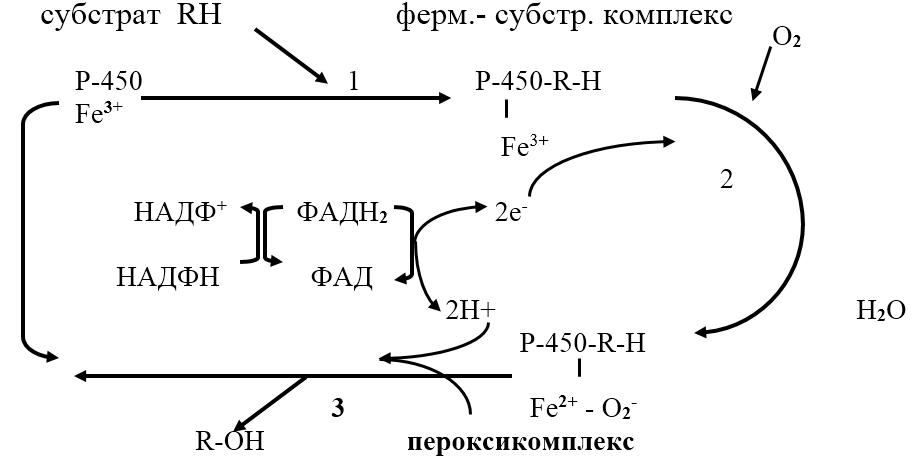
Рис. 11.1. Схема микросомального окисления
Микросомальное окисление протекает в несколько этапов:
1. связывание в активном центре цитохрома Р450 субстрата RН;
2. присоединение первого электрона и восстановление железа в геме до Fe2+; изменение валентности железа увеличивает сродство комплекса Р450 – Fe2+? RH к молекуле кислорода; присоединение второго электрона к молекуле кислорода и образование неустойчивого пероксикомплекса Р450–Fe2+? О2-? RH;
3. Fe2+ окисляется, при этом электрон присоединяется к молекуле кислорода; восстановленный атом кислорода (О2-) связывает два протона (донор протонов – НАДФН+Н+) и образуется 1 молекула воды; второй атом кислорода участвует в гидроксилировании субстрата RH; гидроксилированный субстрат ROH отделяется от фермента.
В результате гидроксилирования гидрофобный субстрат становится более полярным, повышается его растворимость и возможность выведения из организма с мочой. Так окисляются многие ксенобиотики, лекарственные вещества.
В редких случаях в результате гидроксилирования токсичность соединения увеличивается. Например, при окислении нетоксичного бензпирена (содержится в табачном дыму, копченостях) образуется токсичный оксибензпирен, который является сильным концерогеном, индуцирующим злокачественное перерождение клеток.
В митохондриях содержится монооксигеназная система, которая выполняет биосинтетическую функцию: синтез холестерола; стероидных гормонов (кора надпочечников, яичники, плацента, семенники); желчных кислот (печень); образование витамина D3 (почки).
Активные формы кислорода (свободные радикалы)
В организме в результате окислительно-восстановительных реакций постоянно происходит генерация активных форм кислорода (АФК) при одноэлектронном восстановлении кислорода (молекула имеет неспаренный электрон на молекулярной или внешней атомной орбите).
Источники АФК:
1. цепь тканевого дыхания (утечка электронов с восстановленного убихинона KoQH2 на кислород);
2. реакции, катализируемые оксидазами, гемопротеинами, цитохромом Р450;
3. реакции окисления в лейкоцитах, макрофагах и пероксисомах;
4. радиолиз воды;
5. под воздействием ксенобиотиков, пестицидов;
6. реакции самопроизвольного (неферментативного) окисления ряда веществ.
Супероксид-анион – является одним из наиболее широко распространенных в организме свободных радикалов:
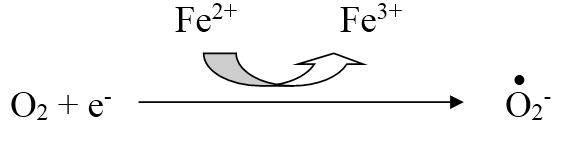
Он образуется в клетках болезнетворных бактерий и является повреждающим фактором для мембран клеток паренхиматозных органов человеческого организма. Для лейкоцитов и макрофагов супероксид-анион является фактором бактерицидности, с помощью которого клетки инактивируют патогенные микроорганизмы.
Другой путь образования свободных радикалов – взаимодействие кислорода с металлами переменной валентности. При этом образуется пероксидный радикал:
Fe2+ + O2 + H+ ? Fe3+ + •HO2
•O2- + Н+ ? •HO2
Взаимодействие супероксиданиона с пероксидным радикалом (1) или одноэлектронное восстановление супероксид-аниона (2) в водной среде приводят к образованию пероксида водорода
•O2- + •НО2 + Н+ ? Н2О2 + О2 (1)
•О2- + е- + 2Н+ ? Н2О2 (2)
Гидроксильный радикал ОН образуется при взаимодействии пероксида водорода с супероксид-анионом (1) либо с металлами (2):
Н2О2 + •О2- ? •ОН + ОН- + О2 (1)
Н2О2 + Fe2+ ? •ОН + ОН- + Fe3+ (2)
Кислородные радикалы обладают высокой реакционной способностью и легко вступают в химические реакции с органическими молекулами для приобретения недостающего электрона. Кислородные радикалы оказывают воздействие на различные структурные компоненты клеток: ДНК (повреждение азотистых оснований); белки (окисление аминокислотных остатков, образование ковалентных «сшивок»); липиды; мембранные структуры.
Активные формы кислорода могут отщеплять электроны от многих соединений, превращая их в новые свободные радикалы, и инициируют тем самым цепные окислительные реакции. Если в реакцию с АФК вступают ненасыщенные жирные кислоты плазматических мембран, говорят о перекисном окислении липидов.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава 7 ЗА ПРЕДЕЛАМИ ИММУННОЙ СИСТЕМЫ
Глава 7 ЗА ПРЕДЕЛАМИ ИММУННОЙ СИСТЕМЫ Эволюция по Ламарку, не отвергая дарвиновского естественного отбора, требует следующей причинно-следственной связи для «запоминания» приобретенного признака клетками в зародышевой линии животных. Измененные условия внешней среды
4.1. Типы взаимодействия
4.1. Типы взаимодействия Выделяют следующие типы взаимодействия между популяциями: «1) нейтрализм, при котором ассоциация двух популяций не сказывается ни на одной из них; 2) взаимное конкурентное подавление, при котором обе популяции активно подавляют друг друга; 3)
ГЛАВА 13 Кайнозой: наступление криоэры. Новые типы сообществ — тропические леса и травяные биомы. Эволюция млекопитающих и появление человека
ГЛАВА 13 Кайнозой: наступление криоэры. Новые типы сообществ — тропические леса и травяные биомы. Эволюция млекопитающих и появление человека Мезозой, как мы помним из главы 9, был термоэрой и отличался «райским» климатом: теплым и выровненным по всей Земле, с ослабленным
6. ТИПЫ ДВИЖЕНИЙ
6. ТИПЫ ДВИЖЕНИЙ Движения человека очень разнообразны, однако всё это разнообразие можно свести к небольшому количеству основных типов активности: обеспечение позы и равновесия, локомоция и произвольные движения.Поддержание позы у человека обеспечивается теми же
Глава 1 РАЗВИТИЕ НЕРВНОЙ СИСТЕМЫ ЧЕЛОВЕКА
Глава 1 РАЗВИТИЕ НЕРВНОЙ СИСТЕМЫ ЧЕЛОВЕКА ФОРМИРОВАНИЕ МОЗГА ОТ МОМЕНТА ОПЛОДОТВОРЕНИЯ ДО РОЖДЕНИЯ После слияния яйцеклетки со сперматозоидом (оплодотворения) новая клетка начинает делиться. Через некоторое время из этих новых клеток образуется пузырек. Одна стенка
Глава 7 ВЫСШИЕ ФУНКЦИИ НЕРВНОЙ СИСТЕМЫ
Глава 7 ВЫСШИЕ ФУНКЦИИ НЕРВНОЙ СИСТЕМЫ Общепризнано, что нервная высшая деятельность человека и животных обеспечивается целым комплексом совместно работающих мозговых структур, каждая из которых вносит в этот процесс свой специфический вклад. Это означает, что нервная
Антиоксидантные системы организма
Антиоксидантные системы организма В организме токсическое действие активных форм кислорода предотвращается за счет функционирования систем антиоксидантной защиты. В норме сохраняется равновесие между окислительными (прооксидантными) и антиоксидантными системами.
Типы нервной системы
Типы нервной системы Большое значение в патологии нервных заболеваний и лечении нервнобольных имеют типы нервной деятельности, разработанные академиком И. П. Павловым. В обычных условиях разные собаки по-разному реагируют на внешние раздражения, по-разному относятся к
ГЛАВА 1 АНАТОМИЯ ПОЛОВОЙ СИСТЕМЫ
ГЛАВА 1 АНАТОМИЯ ПОЛОВОЙ СИСТЕМЫ Органы, обеспечивающие физиологические процессы размножения (половые органы или гениталии), связаны между собой анатомически и функционально, поэтому о них говорят как о системе (половой системе). Их строение у самцов и самок значительно
Типы видообразования
Типы видообразования До сих пор наше внимание было сосредоточено главным образом на скоростях молекулярной и морфологической эволюции, и нам удалось выбрать количественные показатели, приемлемые для нескольких эволюционных процессов. Однако такие показатели, как
Глава шестая РЕАКЦИИ НЕРВНОЙ СИСТЕМЫ СОБАК В УСЛОВИЯХ ЭКСТРЕМАЛЬНЫХ ФАКТОРОВ
Глава шестая РЕАКЦИИ НЕРВНОЙ СИСТЕМЫ СОБАК В УСЛОВИЯХ ЭКСТРЕМАЛЬНЫХ ФАКТОРОВ Известно, что центральная нервная система играет ведущую роль как высший интегрирующий орган и ее функциональное состояние имеет решающее значение для общего состояния живых организмов.
Типы ритмов
Типы ритмов Золотистые водоросли демонстрируют суточный ритм, хотя их сутки и составляют 24,8 ч. Подобные ритмы называются циркадианными (от латинских слов circa — около и dies — день) или околосуточными. Цикл сна и бодрствования у человека, суточные колебания температуры
ГЛАВА III СТРОЕНИЕ ЗУБОЧЕЛЮСТНОЙ СИСТЕМЫ
ГЛАВА III СТРОЕНИЕ ЗУБОЧЕЛЮСТНОЙ СИСТЕМЫ Знание анатомо-топографических особенностей строения и функции зубочелюстной системы необходимо для правильного понимания вопросов профилактики и лечения различных стоматологических заболеваний у собак. Нормальное
ГЛАВА VIII БОЛЕЗНИ ЗУБОЧЕЛЮСТНОЙ СИСТЕМЫ
ГЛАВА VIII БОЛЕЗНИ ЗУБОЧЕЛЮСТНОЙ СИСТЕМЫ В наше время ветеринарная стоматология стала выделяться как отдельная, самостоятельная дисциплина, изучающая не только различные заболевания и отклонения в ротовой полости у животных, но и методы их диагностики, лечения и