В поисках генов видообразования
В поисках генов видообразования
Итак, постзиготическая изоляция возникает в результате фиксации несовместимых (конфликтующих) аллелей в разобщенных популяциях. Что же это за гены, изменения которых порождают такие конфликты? В принципе при скрещивании представителей двух давно разошедшихся популяций конфликтовать может что угодно с чем угодно. Но все-таки интересно было бы найти конкретные гены, ответственные за несовместимость. Для таких генов придумано броское название — «гены видообразования». Ясно, что в разных парах видов конфликтующие гены, скорее всего, будут разными. Несмотря на их несомненное присутствие у разошедшихся видов, идентифицировать их пока удается нечасто. Мы расскажем о нескольких таких удачных примерах.
Несколько генов видообразования нашли у дрозофил (Orr et al., 2004). Как правило, это гены, так или иначе связанные с размножением. Например, один из них, OdsH, вызывает гибридную стерильность (бесплодие) у самцов, полученных от скрещивания Drosophila simulans и D. mauritiana — видов, разделившихся 0,3–1,0 млн лет назад. Функция гена состоит в регуляции экспрессии ряда других генов, участвующих в сперматогенезе. Многие гены видообразования несут следы действия положительного отбора. По-видимому, это значит, что постзиготическая несовместимость часто развивается под действием разнонаправленного отбора (как в эксперименте с дрожжами), а не просто за счет пассивного накопления нейтральных различий.
Что касается млекопитающих, то у них пока описан только один такой ген — Prdm9, ответственный за стерильность мужского потомства при скрещивании двух видов (или подвидов, случай спорный) домовых мышей: Mus musculus и Mus domesticus. То, что где-то на 17-й мышиной хромосоме есть «ген гибридной стерильности», конфликтующий с несколькими другими генами при межвидовых скрещиваниях, было известно давно, но установить его идентичность удалось лишь в 2008 году. С тех пор ген Prdm9 активно изучают. При этом выяснилось много интригующих фактов. В частности, обнаружилась связь Prdm9 со стерильностью не только у гибридных мышей, но и у других животных. Например, у людей мутации этого гена приводят к мужскому бесплодию.
Функцию Prdm9 установили лишь в 2012 году. Оказалось, что ген отвечает за формирование «горячих точек рекомбинации» — мест, где хромосомы чаще всего рвутся, чтобы обменяться участками во время мейоза. В норме у мышей разрывы хромосом при подготовке к кроссинговеру происходят в нефункциональных частях генома, но, если работа Prdm9 нарушена, хромосомы начинают рваться где попало, в том числе в регуляторных областях жизненно важных генов. Мыши с такими генетическими дефектами бесплодны, потому что у них не образуются жизнеспособные половые клетки (Brick et al., 2012).
У растений выявлено около 40 генов видообразования. Как правило, это тоже гены, связанные с размножением — с созреванием пыльцы, ускорением или отсрочкой цветения, механизмами «узнавания» подходящей пыльцы тканями пестика (к этим механизмам относится и самонесовместимость, о которой мы говорили в главе 3). У растений признаки действия положительного отбора на гены видообразования тоже есть, но не такие четкие, как у дрозофил. Возможно, случайные процессы играют в видообразовании у растений более важную роль (Rieseberg, Blackman, 2010).
Один из интересных случаев связан с домашним рисом (см. главу 2). Согласно данным археологии и генетики, азиатский культурный рис Oryza sativa был одомашнен на юге Китая 9 тыс. лет назад (Molina et al., 2011). С тех пор было выведено много сортов, подразделяющихся на две большие группы: O. s. indica (длиннозерные сорта) и O. s. japonica (круглозерные).
«Индийские» и «японские» сорта разделились не менее 3–4 тыс. лет назад и с тех пор эволюционировали аллопатрически, т. е. выращивались в разных районах, почти не скрещиваясь друг с другом. За это время в их генофондах успели накопиться взаимно несовместимые мутации, что привело к частичной репродуктивной изоляции, а именно к снижению плодовитости гибридов indica и japonica. Это можно рассматривать как наметившееся разделение азиатского культурного риса на два вида.
Несовместимость indica и japonica определяется несколькими локусами, структура и функция которых активно изучаются. Китайским генетикам удалось в общих чертах расшифровать принцип действия одного из «локусов несовместимости» S5 (Yang et al., 2012). Локус включает пять белок-кодирующих генов: ORF1, ORF2, ORF3, ORF4 и ORF5 (от open reading frame, открытая рамка считывания — так по традиции обозначают плохоизученные гены с неизвестной функцией). У локуса S5 есть три варианта (аллеля), один из которых (S5i) характерен для большинства сортов indica, другой (S5j) — для japonica, а третий (S5n) — для некоторых сортов, которые дают нормальное плодовитое потомство при скрещивании как с индийскими, так и с японскими сортами. Было показано, что, если вставить в геном japonica ген ORF5 indica, получаются растения с пониженной плодовитостью. Если то же самое проделать с генами ORF3 и ORF4, плодовитость растений не снижается.
Этого недостаточно, чтобы понять, как работает локус S5 и почему аллели S5i и S5j плохо сочетаются друг с другом. Для выяснения этого вопроса авторы скрещивали в разных сочетаниях многочисленные сорта риса (как обычные, так и трансгенные), оценивали плодовитость гибридов, подсчитывали соотношение разных генотипов в гибридном потомстве и, конечно же, сравнивали нуклеотидные последовательности локуса S5 у разных сортов.
Выяснилось, что гены ORF1 и ORF2 одинаковы у всех сортов, а значит, не в них причина несовместимости. Ген ORF3 кодирует белок, похожий на белок теплового шока, — шаперон Hsp70. Такие белки защищают клетку от различных стрессов. У indica ген ORF3 в рабочем состоянии, у japonica в нем произошла делеция (выпало 13 нуклеотидов), и поэтому белок ORF3 утратил функциональность.
Белок ORF4, кодируемый геном ORF4, в норме располагается на мембране мегаспор (клеток, из которых у цветковых растений образуется зародышевый мешок, а после оплодотворения — семя). ORF4 является рецептором, т. е. реагирует на какое-то вещество, находящееся снаружи от клеточной мембраны, и передает сигнал внутрь клетки. У indica ORF4 испорчен мутацией, у japonica он в рабочем состоянии.
Наконец, ORF5 является ферментом (аспартатной протеазой) и в норме выделяется клеткой во внешнюю среду. Там он участвует в синтезе сигнального вещества, на которое реагирует рецептор ORF4. У indica ORF5 активен, у japonica — нет.
Таким образом, генотип indica можно обозначить как 3+4?5+, japonica — как 3?4+5?. Механизм действия этих генов, объясняющий пониженную плодовитость гибридов, показан на рисунке. Белки 5+ и 4+, действуя сообща, выступают в роли «убийц», а белок 3+ является «защитником».
Сигнальное вещество, синтезируемое при участии белка 5+, воспринимается рецептором 4+, что приводит (по неизвестной пока причине) к нарушению работы важной внутриклеточной структуры (эндоплазматической сети). Если в клетке есть белок-защитник 3+, клетка останется жива. Если же белок 3+ отсутствует, в клетке включится программа клеточной смерти (апоптоза), и клетка погибнет. Именно это и происходит с половиной будущих семян у гибридов indica и japonica. Погибают мегаспоры, унаследовавшие от гибридного родительского организма генотип japonica, в котором нет гена-защитника 3+, зато есть ген 4+, позволяющий белку 5+ довести клетку до самоубийства.
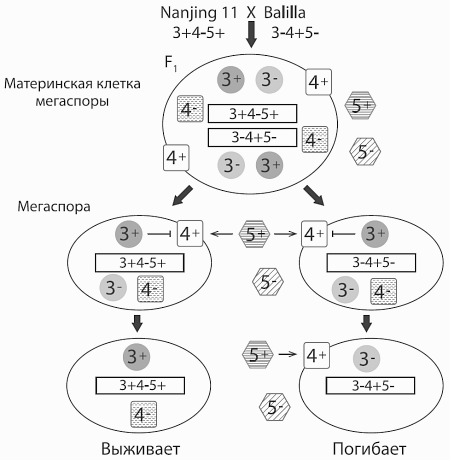
Схема, объясняющая пониженную плодовитость гибридного потомства от скрещивания сортов Nanjing 11 (indica, генотип 3+4?5+) и Balilla (japonica, генотип 3?4+5?). Материнская клетка (диплоидная) дает в результате мейоза четыре гаплоидные мегаспоры. Материнская клетка, как и все гибридное растение, гетерозиготна по трем рассматриваемым генам и поэтому содержит как рабочие (3+, 4+, 5+), так и нерабочие (3?, 4?, 5?) варианты трех белков. В результате мейоза из нее образуются гаплоидные мегаспоры двух типов: с генотипом indica и с генотипом japonica (генотипы не перекомбинируются, потому что все три гена расположены вплотную друг к другу на хромосоме). Поначалу в мегаспорах сохраняются все шесть белков, унаследованных от материнской клетки, но впоследствии в них остаются только белки, закодированные в геноме самой мегаспоры. При этом белок 5+, выделяющийся в межклеточное пространство, действует на все мегаспоры независимо от того, закодирован ли он в их геноме. Мегаспоры с генотипом japonica погибают, потому что на них действуют совместно оба белка-убийцы 5+ и 4+, а белка-защитника 3+ у них нет. Мегаспоры с генотипом indica выживают, потому что у них нет убийцы 4+ и есть защитник. Из Yang et al., 2012.
Что касается сортов, которые свободно скрещиваются и с indica, и с japonica, то у них могут быть разные генотипы, например, 3?4?5? или 3+4+5?. Несовместимость проявляется, только когда с носителем аллеля 5+ скрещивается растение с генами 3? и 4+. Тогда у половины мегаспор не окажется защитника (3+) от действующих совместно «убийц» 5+ и 4+.
Для диких родственников культурного риса, в том числе для предкового вида Oryza rufipogon, характерен генотип 3+4+5+, т. е. активны и оба «убийцы», и «защитник». Скорее всего, такой же генотип был и у первых одомашненных сортов риса. Вероятно, у диких предков все три гена зачем-то нужны (хотя мы пока не знаем зачем), а переход к «культурной» жизни на возделываемых полях сделал их излишними. Впоследствии у двух групп сортов, indica и japonica, закрепились мутации, выводящие из строя некоторые гены этого комплекса. Внутри каждой группы мутации были взаимно совместимыми, потому что несовместимые комбинации, такие как 3?4+5+, отсеивались отбором. Но отбор не проверял мутации, закрепившиеся в одной группе, на совместимость с мутациями, закрепившимися в другой. Так и возникла частичная постзиготическая несовместимость между сортами — в полном согласии с моделью Добжанского — Мёллера.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
В поисках гармонии
В поисках гармонии Биологи давно уже обратили внимание на экстремальные принципы. Заложенная в них идея оптимальности, экономии как нельзя лучше соответствует давнему представлению о совершенстве и целесообразности живой природы. Дарвиновская концепция эволюции и
В поисках "генов доброты"
В поисках "генов доброты" Мы уже знаем, что, если закапать человеку в нос окситоцин, у него повышаются доверчивость и щедрость. Еще мы знаем, что эти черты характера являются отчасти наследственными. Исходя их этих фактов, естественно предположить, что те или иные варианты
В поисках компромисса
В поисках компромисса Было время, когда многие биологи на полном серьезе допускали, что каждый признак любого организма имеет адаптивное значение, "для чего-то служит". Они рассуждали примерно так: "Хоть мы и не знаем, зачем этому жуку четыре щетинки на задней лапке (а не
2.3. Вопросы макроэволюции и видообразования
2.3. Вопросы макроэволюции и видообразования Поскольку приспособительные изменения популяций (микроэволюция) разительно отличаются от картины разнообразия органического мира (макроэволюция), постоянно идет спор о наличии в макроэволюционных процессах особых факторов,
Цепная реакция видообразования
Цепная реакция видообразования Теоретически видообразование может быть самоускоряющимся процессом. Появление новых видов создает новые ниши, которые могут быть освоены следующим «поколением» новых видов. Например, появление нового вида травоядных может
Для видообразования нужны популяции, а не отдельные особи
Для видообразования нужны популяции, а не отдельные особи Селекция — вот путь, которым, по мнению большинства ученых, волки были превращены в собак. Однако эволюционирует не отдельная особь, а популяция, поэтому для видообразования нужно было, чтобы на протяжении
Дифференциальная выживаемость необходима для видообразования
Дифференциальная выживаемость необходима для видообразования Еще один принцип эволюционного видообразования путем искусственного или естественного отбора — дифференциальная выживаемость. При искусственном отборе это означает, что селекционер одним животным дает
В поисках дома
В поисках дома E. coli по природе своей первопроходец. Задолго до того, как большинство других бактерий устроилось в человеке — хозяине, E. coli уже основала там жизнеспособную колонию. E. coli способна инфицировать младенца уже в процессе родов, воспользовавшись пальцами врача,
Типы видообразования
Типы видообразования До сих пор наше внимание было сосредоточено главным образом на скоростях молекулярной и морфологической эволюции, и нам удалось выбрать количественные показатели, приемлемые для нескольких эволюционных процессов. Однако такие показатели, как
В поисках пристанища
В поисках пристанища В лесу по земле всюду ползают крупные красноголовые муравьи с темным брюшком, на котором в том месте, где отходит стебелек, расположено золотистое пятно. Не спеша они пробираются по зарослям трав, заползают во всякие норки, щелочки и что-то ищут.
В поисках пристанища
В поисках пристанища Их будущееСудьбы самок, покинувших семьи, самые различные. Они могут уходить вместе с частью примкнувших к ним рабочими и обосновывать новую семью, чаще всего поблизости от старой, постепенно образуя содружественные колонии. У маленьких семей
В поисках пристанища
В поисках пристанища По лесной дороге, по тропинкам и, если приглядеться, всюду в лесу по земле ползают крупные рыжие муравьи с темным брюшком, на котором в том месте, где отходит стебелек, расположено золотистое пятно. Не спеша они пробираются по зарослям трав, заползают
В поисках нестабильности
В поисках нестабильности Объяснение паразитной теорией Черной Королевы полового размножения — прекрасный пример того, как в науке для решения одной проблемы приходится объединять вместе несколько разных подходов. Ведь идея о паразитах и половом размножении возникла у
В поисках яда
В поисках яда До XIX века сном безраздельно владели поэты и философы. Люди отправлялись в объятия Морфея, не задумываясь, что собой представляет этот крылатый бог, сын царицы вечного покоя Нюкты, то есть Ночи, и брат Танатоса, бога смерти.В начале века сформировалась