Рассказ Секвойи
Рассказ Секвойи
Есть такие места, о которых говорят, что каждый обязан их посетить, прежде чем умрет. Для меня такое место – Мюирский лес к северу от моста “Золотые Ворота”. На случай, если вы немного запоздали с посещением этого леса, советую выбрать его местом своего захоронения (впрочем, я не уверен, что это разрешено). Мюирский лес – это зеленый с коричневым храм тишины, неф, образованный самыми высокими на планете деревьями – секвойями Тихоокеанского побережья (Sequoia sempervirens), чья толстая кора гасит эхо, неизбежно возникающее в любом храме, построенном людьми. Представители близкого вида Sequoiadendron giganteum, которые растут в предгорьях Сьерра-Невады, обычно не такие высокие, но зато более массивные. Крупнейшее в мире живое существо, дерево “Генерал Шерман”, является гигантом более 30 метров в окружности и более 80 метров высотой. Предполагаемая масса дерева составляет 1260 тонн. Его возраст точно не установлен, но вообще этот вид знаменит тем, что живет дольше 3 тыс. лет. Возраст “Генерала Шермана” можно было бы установить с точностью до года, если бы мы могли его срубить[99]. Однако это непросто: одна кора имеет толщину около метра. Так что будем надеяться, что эта участь его никогда не постигнет, вопреки мнению Рональда Рейгана, который в бытность губернатором Калифорнии высказался о секвойях так: “Достаточно увидеть одну, чтобы судить обо всех”.
Как определить возраст дерева – даже настолько старого, как “Генерал Шерман”? Подсчитав годичные кольца на срезе. На этом основан метод дендрохронологии, с помощью которого археологи, работающие в масштабе столетий, могут точно датировать любой образец древесины.
Я собираюсь рассказать о методах, с помощью которых мы на протяжении нашего путешествия датировали образцы, размещая их на абсолютной временной шкале. Годичные кольца – очень точный инструмент, но он позволяет охватить лишь относительно небольшой временной промежуток. Возраст ископаемых определяют другими методами, основанными преимущественно на радиоактивном распаде.
Годичные кольца появляются вследствие того очевидного факта, что дерево в некоторые сезоны растет интенсивнее. Но точно так же дерево растет лучше в хороший год, чем в плохой – независимо от сезона. Поскольку удачные года сменяются неблагоприятными, по одному кольцу ничего нельзя сказать. Однако с течением лет на коре образуется рисунок из широких и узких колец, одинаковый у всех деревьев на достаточно большой территории. Дендрохронологи составляют каталоги этих рисунков. И затем можно датировать деревянный фрагмент, например, затянутого илом корабля викингов.
Тот же принцип используется и в каталогах мелодий. Допустим, в голове крутится мелодия, и вы не можете вспомнить название. Как ее найти? Есть разные способы, и самый простой – код Парсонса. Для этого нужно представить мелодию в виде ряда подъемов (up) и спадов (down). Первая нота обозначается звездочкой, потому что она, очевидным образом, не может быть ни выше, ни ниже предыдущей. Вот, например, образец мелодии Londonderry Air, или Air from County Derry, который я только что набрал на сайте Melodyhound:
*UUUDUUDDDDDUUUUUDDDUD
Аппарат Melodyhound верно определил мелодию: она известна в Америке под названием Danny Boy (по нескольким словам, вставленным в песню в XX веке). На первый взгляд удивительно, как можно идентифицировать мелодию с помощью короткой последовательности символов, которые к тому же указывают только на направление градиента, не обозначая ни расстояния между нотами, ни их длительность. Но это работает. И по тем же причинам рисунка годичных колец оказывается достаточно для идентификации.
В недавно срубленном дереве внешнее кольцо соответствует современности. А о прошлом можно судить, отсчитывая кольца внутрь. Поэтому с помощью рисунка годичных колец современных деревьев, для которых известна дата вырубки, можно проставлять абсолютные даты для других деревьев. Обнаруживая наложения – то есть рисунки вблизи сердцевины молодого дерева, соответствующие рисунку внешних слоев старшего дерева, – можно датировать кольца старших деревьев. Последовательно соединяя такие наложения, мы можем точно датировать даже очень старые деревья – теоретически даже ископаемый лес Аризоны. Для этого нужен непрерывный ряд промежуточных звеньев. Благодаря технике наложения можно составить каталог признаков и пользоваться им для датирования образцов древесины, превосходящих по возрасту самые старые деревья, которые мы видели живыми. Кстати, изменчивость толщины колец можно использовать не только для датирования, но и для реконструкции климатических и экологических условий, относящихся ко временам, когда метеорологических записей никто не вел.
Разрешающая способность дендрохронологии ограничивается относительно коротким промежутком времени. Но рост дерева – это не единственный природный процесс, для которого характерна цикличность. В принципе, для датирования можно использовать любой такой процесс – нужно лишь воспользоваться техникой соединения перекрывающихся последовательностей. И некоторые из природных процессов позволяют проводить датирование на гораздо более длинных интервалах по сравнению с дендрохронологией. Так, осадки откладываются на морском дне неравномерно, образуя линии, аналогичные годичным кольцам. Эти линии можно подсчитать и затем идентифицировать рисунки по образцам, извлеченным глубинными цилиндрическими зондами.
Другой пример, с которым мы познакомились в “Эпилоге к рассказу Эпиорниса”, – палеомагнитное датирование. Как мы знаем, магнитное поле Земли время от времени внезапно претерпевает инверсию. Северный магнитный полюс на несколько тысяч лет становится Южным. Затем они снова меняются местами. За последние 10 млн лет это произошло 282 раза. Хотя я употребил слово “внезапный”, внезапны такие события лишь в геологическом масштабе. Вот было бы весело, если бы полюса, меняясь местами, разворачивали все самолеты и корабли в противоположную сторону. Однако на самом деле “переключение” занимает несколько тысяч лет и представляет собой очень сложный процесс. Следует заметить, что Северный магнитный полюс в любом случае редко совпадает с географическим Северным полюсом (вокруг которого вращается Земля). Обычно он блуждает по полярной области. В настоящее время Северный магнитный полюс расположен возле острова Батерст на севере Канады, примерно в 2 тыс. км от географического Северного полюса. В период “переключения” наступает время “междуцарствия”: возникают помехи, иногда приводящие к появлению нескольких магнитных северных или южных полюсов. Когда поле стабилизируется, иногда оказывается, что бывший Северный магнитный полюс оказался возле географического Южного полюса, и наоборот. Затем наступает период стабильности, когда магнитные полюса блуждают вокруг географических. Это может продолжаться в течение миллиона лет, пока не придет время для следующего “переключения”.
В геологических масштабах тысяча лет – почти ничто. Время, потраченное на “переключение”, незначительно по сравнению со временем вблизи одного из географических полюсов. Природа ведет автоматическую запись таких событий. Некоторые минералы в расплавленной вулканической породе ведут себя как крошечные компасы. Когда порода остывает, “стрелки” превращаются в запись магнитного поля Земли в момент отвердевания (благодаря некоторым другим процессам явление палеомагнетизма можно наблюдать и в осадочных породах). После “переключения” “стрелки” начинают указывать противоположное направление. Это напоминает историю с годичными кольцами – однако здесь интервал составляет не год, а примерно миллион лет. Узоры можно сопоставлять, выстраивая непрерывную хронологию магнитных переключений. С помощью этого метода нельзя определить абсолютный возраст, потому что, в отличие от годичных колец, линии откладываются через разные промежутки времени. Однако мы по-прежнему можем собирать характерные узоры из разных мест. И если для одного из таких мест доступен какой-либо метод абсолютного датирования (см. ниже), узоры магнитных линий можно использовать как код Парсонса, отыскивая тот же временной интервал в других местах. Как и в случае с годичными кольцами и другими методами датирования, картина складывается из фрагментов, собранных в различных местах.
Годичные кольца хороши для датирования относительно молодых образцов. Датировки давних событий неизбежно окажутся менее точными, и их устанавливают с помощью радиоактивного распада.
Все вещества состоят из атомов. Существует более 100 видов атомов, соответствующих числу химических элементов. Большинство веществ представляют собой не чистые элементы, а соединения, то есть два или более атомов различных элементов, связанных вместе, как в карбонате кальция, поваренной соли или угарном газе. Связывание атомов в соединения происходит благодаря электронам, которые представляют собой крошечные частицы, вращающиеся по орбите (на самом деле это просто метафора: реальное их поведение гораздо сложнее) вокруг ядра атома. Ядро огромно по сравнению с электроном, но чрезвычайно мало по сравнению с орбитой электрона. Наша рука, состоящая главным образом из пустоты, встречает сопротивление, ударяясь о кусок железа, тоже состоящий главным образом из пустоты. Причина в том, что силы, связывающие атомы в двух твердых телах, при взаимодействии не дают им проходить друг сквозь друга. Как следствие, железо или камень кажутся нам монолитными – а мозг услужливо помогает в оформлении этой иллюзии.
Давно известно, что химическое соединение можно разъединить на составляющие и затем собрать снова, получив то же или другое соединение с выделением или поглощением энергии. Такие взаимодействия между атомами и составляют химию. Однако до XX века сам атом считался неделимым. Его считали наименьшей частицей. Атом золота, согласно взглядам того времени, был частичкой золота, качественно отличающейся от атома меди, который представлял собой частицу меди. Современные представления изящнее. Мы знаем, что атомы золота, меди, водорода и других элементов представляют собой различные комбинации фундаментальных частиц – аналогично тому, как гены лошади, салата, человека или бактерии являются различными комбинациями четырех “букв” ДНК. Точно так же, как химические соединения являются комбинациями, составленными из конечного набора примерно сотни атомов, каждое ядро атома оказалось комбинацией двух фундаментальных частиц – протонов и нейтронов. Ядро атома золота не “сделано” из золота. Как и все другие ядра, оно из протонов и нейтронов. Ядро железа отличается от ядра золота не потому, что оно из “железного” вещества, а потому, что содержит 26 протонов (и 30 нейтронов), а не 79 протонов (и 118 нейтронов), как ядро золота. На уровне атома не существует никакого “вещества” со свойствами золота или железа. Есть лишь комбинации протонов, нейтронов и электронов. Впрочем, физики на этом не останавливаются и утверждают, что даже протоны, нейтроны и электроны состоят, в свою очередь, из кварков. Но мы не будем слишком углубляться в физику.
Протоны и нейтроны имеют примерно одинаковый размер, они гораздо больше электрона. В отличие от нейтрона, электрически нейтрального, каждый протон имеет одну единицу электрического заряда (который произвольно считается положительным). Этот заряд уравновешивает отрицательный заряд одного электрона, который находится на орбите вокруг ядра. Протон может превратиться в нейтрон, если поглотит электрон, отрицательный заряд которого нейтрализует положительный заряд протона. Нейтрон, в свою очередь, может превратиться в протон, избавившись от единицы отрицательного заряда – электрона. Такие преобразования являются примерами ядерных реакций. Химические реакции не затрагивают ядро.
Ядерные реакции приводят к его изменениям. Обычно они сопровождаются гораздо более значительным обменом энергии, чем химические реакции. Поэтому ядерное оружие при равной массе разрушительнее обычных (химических) взрывчатых веществ. Попытки алхимиков превратить один химический элемент в другой провалились лишь потому, что они пытались сделать это с помощью химических, а не ядерных реакций.
У каждого химического элемента определенное число протонов в ядре атома и равное ему число электронов на орбите вокруг ядра: 1 – у водорода, 2 – у гелия, 6 – у углерода, 11 – у натрия, 26 – у железа, 82 – у свинца, 92 – у урана. Атомное число в значительной степени определяет свойства элемента. Нейтроны почти не влияют на химические свойства элемента, однако определяют его массу и участвуют в ядерных реакциях.
Число нейтронов в ядре обычно примерно равно числу протонов (или немного больше). В отличие от числа протонов, которое фиксировано для каждого элемента, число нейтронов варьирует. Обычный углерод имеет шесть протонов и шесть нейтронов, что в сумме дает массовое число 12 (массой электронов можно пренебречь, а нейтрон весит примерно столько же, сколько протон). Поэтому его называют углеродом-12.
У углерода-13 один дополнительный нейтрон, а у углерода-14 их два. При этом у каждого по шесть протонов. Такие “версии” химического элемента называются изотопами. Причина, по которой изотопы называются углеродом, в том, что у них одинаковое атомное число (6) и, следовательно, одинаковые химические свойства. Если бы ядерные реакции были открыты раньше химических, возможно, изотопы назывались бы по-разному. Иногда изотопы ведут себя настолько странно, что вполне заслуживают индивидуальных названий. У обычного водорода нет нейтронов. Водород-2, который имеет один протон и один нейтрон, называется дейтерием, а водород-3 с одним протоном и двумя нейтронами – тритием. Все они в химическом отношении ведут себя как водород. Например, дейтерий при взаимодействии с кислородом образует так называемую тяжелую воду, которую применяют в производстве водородных бомб.
Таким образом, изотопы различаются лишь числом нейтронов. Некоторые изотопы нестабильны: это значит, что их ядро с высокой вероятностью может в любой момент превратиться в ядро другого типа. Другие изотопы стабильны: вероятность превращения их ядер близка к нулю. Нестабильные изотопы также называют радиоактивными. У свинца 4 стабильных изотопа и 25 описанных нестабильных изотопов. У урана – очень тяжелого металла – нестабильны (то есть радиоактивны) все изотопы.
Радиоактивность – вот ключ к абсолютному датированию горных пород и окаменелостей. Как происходит превращение нестабильных радиоактивных элементов? Это может происходить по-разному, но есть два основных способа: альфа-распад и бета-распад. При альфа-распаде ядро теряет альфа-частицу, состоящую из двух протонов и двух нейтронов. В результате массовое число уменьшается на четыре единицы, атомное – на две (соответствующие двум потерянным протонам). Элемент превращается в элемент, имеющий на два протона меньше. Так, уран-238 (92 протона и 146 нейтронов) превращается в торий-234 (90 протонов и 144 нейтрона).
Бета-распад происходит иначе. Один нейтрон в исходном ядре превращается в протон, выбрасывая бета-частицу, которая представляет собой единицу отрицательного заряда, или один электрон. Массовое число ядра при этом не меняется, потому что общее число протонов и нейтронов остается неизменным (массой электронов можно пренебречь). Однако атомное число увеличивается на 1, поскольку в ядре становится протоном больше. Натрий-24 в результате бета-распада превращается в магний-24. Массовое число остается прежним – 24, а атомное число увеличивается с 11 (натрий) до 12 (магний).
Третий вид превращения – нейтронно-протонное замещение. Блуждающий нейтрон ударяет в ядро, выбивает один протон и занимает его место. Как и при бета-распаде, массовое число при этом не меняется. Однако атомное число уменьшается на 1 из-за потери протона (атомное число – это число протонов в ядре).
Четвертый способ радиоактивного превращения, который приводит к аналогичным изменениям атомного и массового чисел, – электронный захват. Он представляет собой как бы бета-распад наоборот.
При бета-распаде нейтрон превращается в протон, испуская электрон. А при электронном захвате, напротив, протон, захватывая электрон, превращается в нейтрон. Атомное число уменьшается на 1, а массовое число остается неизменным. Калий-40 (атомное число 19) превращается в аргон-40 (атомное число 18).
Кроме описанных, есть множество других способов превращения одних ядер в другие.
Один из основных принципов квантовой механики – невозможность точно предсказать, когда распадется ядро нестабильного элемента. Но мы можем измерить статистическую вероятность этого события, причем такая вероятность будет характерной для конкретного изотопа. Стандартной мерой является период полураспада. Чтобы измерить период полураспада радиоактивного изотопа, нужно взять образец вещества и подсчитать, за какое время его половина превратится во что-либо другое. Период полураспада стронция-90 составляет 28 лет. Если мы возьмем сто граммов стронция-90, то 28 лет спустя у нас останется лишь пятьдесят граммов. Остальная половина превратится в иттрий-90 (который, в свою очередь, превращается в цирконий-90). Значит ли это, что еще через 28 лет у нас совсем не останется стронция? Разумеется, нет. Останется 25 граммов стронция. Еще через 28 лет количество стронция снова уменьшится вдвое и составит 12,5 грамма. Теоретически оно никогда не достигнет нуля. Поэтому используется понятие периода полураспада.
Период полураспада углерода-15 составляет 2,4 секунды. Через 2,4 секунды от исходного образца остается половина. Еще 2,4 секунды спустя остается четверть, еще через 2,4 секунды – восьмая часть, и так далее. Период полураспада урана-238 составляет почти 4,5 млрд лет. Это примерный возраст Солнечной системы. Поэтому от всего урана-238, который присутствовал на Земле в момент ее формирования, сейчас осталась примерно половина. Замечательное и очень полезное свойство радиоактивности заключается в том, что периоды полураспада различных элементов охватывают огромный временной диапазон, от долей секунд до миллиардов лет.
Итак, мы подошли к основной мысли. Тот факт, что каждый радиоактивный изотоп имеет определенный период полураспада, позволяет датировать горные породы. Вулканические породы нередко содержат радиоактивные изотопы, например калий-40. Он превращается в аргон-40 (период полураспада – 1,3 млрд лет). Теоретически это точные “часы”. Однако измерять содержание калия-40 в горной породе бессмысленно: мы не знаем, сколько его было вначале. Вместо этого нужно оценить отношение калия-40 к аргону-40. К счастью, если калий-40 в кристаллической породе распадается, то аргон-40 (который представляет собой газ) остается в кристалле. Если в кристалле содержание калия-40 и аргона-40 одинаково, то можно заключить, что половина исходного калия-40 распалась. Следовательно, с момента формирования кристалла прошло 1,3 млрд лет. Если аргона-40 вдвое больше, чем калия-40, то с момента формирования кристалла прошло 2,6 млрд лет. А если, напротив, аргона-40 вдвое меньше, можно сделать вывод, что кристаллу 650 млн лет.
Момент кристаллизации, который в случае вулканических пород соответствует моменту остывания лавы, представляет нулевую точку отсчета. После этого исходный изотоп начинает распадаться, а образованный остается “захваченным” в кристалле. Теперь остается измерить соотношение двух изотопов, найти период полураспада исходного изотопа в справочнике и вычислить возраст кристалла. Как я говорил, окаменелости обычно находят в осадочных породах, в то время как пригодные для датирования кристаллы обычно встречаются в вулканических. Поэтому сами окаменелости приходится датировать косвенно, на основе вулканических пород, между которыми залегает интересующий нас слой.
Здесь есть одна трудность: первичным продуктом распада нередко становится другой нестабильный изотоп. Аргон-40, первичный продукт распада калия-40, стабилен. Но уран-238, распадаясь, проходит не менее четырнадцати нестабильных промежуточных стадий, которые включают девять альфа-распадов и семь бета-распадов. Конечной стадией является стабильный изотоп свинец-206. Самый длинный период полураспада в этом ряду (4,5 млрд лет) относится к первому переходу, от урана-238 к торию-234. У одного из промежуточных переходов, от висмута-214 к таллию-210, период полураспада составляет всего двадцать минут – и это не самый быстрый (то есть самый вероятный) переход. Последующие переходы занимают время, пренебрежительно малое по сравнению с первичным. Поэтому для датирования горной породы наблюдаемое отношение урана-238 к свинцу-206 нужно оценивать, исходя из периода полураспада в 4,5 млрд лет.
Уран-свинцовый и калий-аргоновый методы, в рамках которых периоды полураспада оцениваются миллиардами лет, используются для датирования очень древних ископаемых. Для молодых пород эти методы слишком грубы. Для них нужны изотопы с более короткими периодами полураспада. К счастью, в нашем распоряжении целый ряд “часов”, и для каждой породы нужно выбрать подходящие. Более того, различные “часы” можно использовать для перепроверки.
Самые быстрые радиоактивные “часы” обычно основаны на применении углерода-14. Таким образом, мы вернулись к рассказчику: древесина – один из главных материалов, который археологи датируют с помощью углерода-14. Углерод-14 распадается на азот-14 с периодом полураспада 5730 лет. Углеродные “часы” необычны тем, что они используются для датирования мертвых тканей, а не окружающих их вулканических пород, как в других случаях. Датирование углеродом-14 играет важную роль в изучении относительно недавних событий – моложе большинства ископаемых.
Большая часть углерода в мире представлена в виде стабильного изотопа углерод-12. Примерно одна миллион-миллионная часть углерода представлена нестабильным изотопом углерод-14. Поскольку период полураспада углерода измеряется тысячами лет, весь углерод-14 на Земле давно превратился бы в азот-14, если бы не возобновлялся. К счастью, некоторое количество атомов азота-14, самого распространенного в атмосфере газа, непрерывно превращается, в результате бомбардировки космическими лучами, в углерод-14. Скорость образования углерода-14 примерно постоянна. Большая часть углерода в атмосфере (углерода-14 и более распространенного углерода-12) химически связана с кислородом в виде углекислого газа. Этот газ поглощается растениями, которые используют атомы углерода для построения тканей. Растения не делают различий между углеродом-14 и углеродом-12 (их интересуют химические, а не ядерные свойства атомов). Поэтому оба изотопа одинаково хорошо усваиваются растениями.
Растения служат пищей животным, которых, в свою очередь, едят другие животные. Поэтому углерод-14 (в определенной пропорции к углероду-12) распространяется во всей пищевой цепи. По сравнению с периодом полураспада углерода-14 это происходит довольно быстро. Эти два изотопа присутствуют во всех живых тканях примерно в том же соотношении, что и в атмосфере: один к миллиону миллионов. Конечно, они иногда превращаются в атомы азота-14. Но постоянная скорость их превращения компенсируется непрерывным обменом с постоянно обновляемым через пищевую цепь атмосферным углекислым газом.
Однако в момент смерти организма все меняется. Мертвый хищник выпадает из пищевой цепи. Мертвое растение больше не получает углекислого газа из атмосферы. Мертвое травоядное больше не ест. Углерод-14 в трупе животного или в мертвом растении продолжает превращаться в азот-14, но запасы его больше не пополняются из атмосферы. Таким образом, соотношение углерода-14 и углерода-12 в мертвых тканях начинает снижаться с периодом полураспада 573° лет. Для нас важность этого процесса заключается в том, что мы получаем возможность узнать время смерти животного или растения, измерив соотношение углерода-14 и углерода-12. (Именно так ученые доказали, что Туринская плащаница не имеет отношения к Иисусу: она изготовлена в средневековье.) Датирование углеродом-14 является замечательным инструментом для определения возраста относительно недавних образцов. Однако для совсем древних событий этот метод не годится, поскольку за относительно недолгое время почти весь углерод-14 превращается в углерод-12, а того, что остается, недостаточно для точных измерений.
Существуют и другие методы абсолютного датирования. Постоянно появляются новые. Это позволяет охватить огромный временной диапазон. Кроме того, разные методы можно использовать для перепроверки: если датировка подтверждается несколькими методами, с ней сложно спорить.
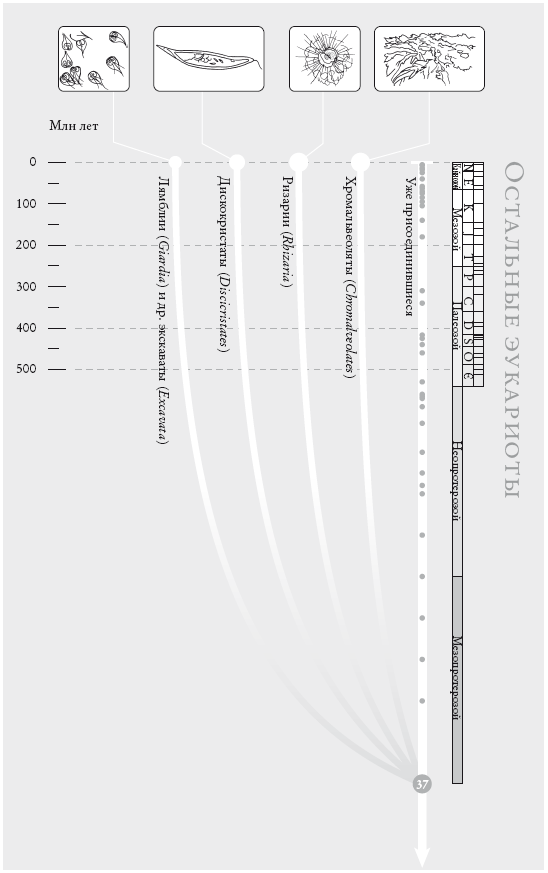
Остальные эукариоты. Филогения оставшихся эукариот (ок. 50 тыс. описанных видов) имеет очень низкое разрешение. Затемненные линии указывают на высокий уровень неопределенности. Ветвь хромальвеолят часто делят на ветви хромист (гетероконт) и альвеолят.
На рис. (слева направо): кишечная лямблия (Giardia lamblia), Euglena acus, фораминифера (Globigerina), Ecklonia radiata.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
3. Секвойи
3. Секвойи Для беседы о секвойях я приглашу вас, читатель, пойти со мной в Ялтинский городской сад. Я очень люблю этот тщательно устроенный сад, в котором приезжий найдет целый ряд замечательных растений.Мне неоднократно приходилось показывать этот сад северянам и
3. Секвойи
3. Секвойи Для беседы о секвойях я приглашу вас, читатель, пойти со мной в Ялтинский городской сад. Я очень люблю этот тщательно устроенный сад, в котором приезжий найдет целый ряд замечательных растений.Мне неоднократно приходилось показывать этот сад северянам и
Рассказ Евы
Рассказ Евы Есть впечатляющая разница между «родословными деревьями генов» и «родословными деревьями людей». В отличие от человека, который происходит от двух родителей, у гена есть только один родитель. Каждый из Ваших генов должен был быть получен или от Вашей матери,
Рассказ Taq
Рассказ Taq Достигнув нашего самого древнего свидания, собрав в нашем странствии всю жизнь, которую знаем, мы имеем возможность рассмотреть ее разнообразие. На самом глубинном уровне разнообразие жизни является химическим. Профессии, которыми заняты наши
Рассказ Stw 573
Рассказ Stw 573 Не думаю, что есть смысл придумывать причины, в силу которых ходить на двух ногах – это здорово. Будь так, шимпанзе делали бы то же самое, не говоря уже о других животных. Нет причины, по которой бег на двух или четырех конечностях быстрее или удобнее.
Рассказ Орангутана
Рассказ Орангутана Возможно, заявление о наших давних связях с Африкой было поспешным. Что если наши предки покинули Африку около 20 млн лет назад и поселились в Азии, а 10 млн лет назад вернулись в Африку?Если так, то современные человекообразные обезьяны, включая тех,
Рассказ Ревуна[18]
Рассказ Ревуна[18] Новые гены появляются не из воздуха. Они образуются при дупликации прежних генов. После этого каждый из них идет своим путем, приобретая мутации и подвергаясь действию естественного отбора и дрейфа генов. Обычно мы не видим, как это происходит, но,
Рассказ Айе-айе
Рассказ Айе-айе Один британский политик как-то описал конкурента (который позднее стал лидером партии) как человека, “в котором есть что-то ночное”. При взгляде на айе-айе складывается именно такое впечатление, и это не случайно: она ведет целиком ночной образ жизни. Из
Рассказ Шерстокрыла
Рассказ Шерстокрыла Шерстокрыл из Юго-Восточной Азии мог бы рассказать нам, каково это – парить во воздуху ночного леса. Но для нас, пилигримов, у него приготовлена гораздо более приземленная история. Мораль ее в том, что составленная нами схема с сопредками, рандеву и
Рассказ Мыши
Рассказ Мыши Из тысяч грызунов домашняя мышь (Mus musculus) может поведать кое-что особенное: ни один другой вид млекопитающих, кроме нашего собственного, мы не изучали так интенсивно. Именно на мышах, а не на пресловутых морских свинках держатся медицинские, физиологические и
Рассказ Бобра
Рассказ Бобра “Фенотип” – это то, что находится под влиянием генов. В целом под фенотипом понимают все, что относится к телу. Но есть тонкости, вытекающие из этимологии. Phamo по-гречески означает “показывать”, “обнаруживать”, “выявлять”, “выражать”, “раскрывать”.
Рассказ Гиппопотама
Рассказ Гиппопотама В школе, изучая греческий, я узнал, что “гиппос” означает “лошадь”, а “потамос” – “река”. Выходило, что гиппопотамы – “речные лошади”. Позднее, забросив греческий и занявшись зоологией, я узнал, что гиппопотамы не имеют отношения к лошадям. В
Рассказ Тюленя
Рассказ Тюленя В большинстве естественных популяций число самцов и самок примерно одинаково. На то есть эволюционные причины, и о них рассказал замечательный специалист по статистике и эволюционной генетике Рональд Э. Фишер. Представьте себе популяцию, количество в
Рассказ Броненосца
Рассказ Броненосца С зоологической точки зрения Южная Америка сродни Мадагаскару: как и Мадагаскар, она откололась от Африки – но не с восточной, а с западной стороны. Произошло это примерно тогда же или чуть позднее. Как и Мадагаскар, в течение почти всего времени
Рассказ Секвойи
Рассказ Секвойи Есть такие места, о которых говорят, что каждый обязан их посетить, прежде чем умрет. Для меня такое место – Мюирский лес к северу от моста “Золотые Ворота”. На случай, если вы немного запоздали с посещением этого леса, советую выбрать его местом своего
Рассказ Taq
Рассказ Taq Итак, мы встретили практически все существующие формы жизни. Теперь можно окинуть взглядом открывшееся разнообразие. На самом глубоком уровне разнообразие жизни является химическим. Профессии, которыми владеют наши пилигримы, охватывают широкий диапазон