Глава 8. Любовь и атавизмы Какие гены делают млекопитающих млекопитающими?
Глава 8. Любовь и атавизмы
Какие гены делают млекопитающих млекопитающими?
Среди многих тысяч младенцев, каждый год рождающихся в Токио и его окрестностях, большинство не привлекают особого внимания. В декабре 2005 года, после сорока недель и пяти дней беременности, женщина по имени Маюми спокойно родила девочку Эмико (имена членов семьи изменены по этическим соображениям). Маюми было 28 лет, во время беременности и работа ее крови, и показания УЗИ были совершенно нормальными. Сами роды и их последствия тоже были обычными – конечно, насколько «обычным» и «стандартным» событием можно считать рождение первого ребенка в семье. Маюми и ее муж Хидео, работавший на бензоколонке, конечно, испытывали совершенно нормальный для таких случаев трепет, когда акушерка очистила ротик маленькой Эмико от слизи и добилась от нее первого крика. Медсестры взяли у Эмико кровь для стандартного анализа, и, опять-таки, все оказалось нормальным. Затем у Эмико пережали и обрезали пуповину – дорожку жизни, соединявшую младенца с материнской плацентой, и вскоре пуповина отсохла, а оставшийся маленький кусочек почернел и естественным способом отвалился, оставив на животике пупок. Через несколько дней Хидео и Маюми с Эмико на руках покинули госпиталь в Чибе, пригороде Токио. Все шло так, как следует.
Через 36 дней после родов у Маюми началось маточное кровотечение. Подобные кровотечения в послеродовой период случаются у многих женщин, но еще через три дня к этому добавилась сильная лихорадка. Чтобы нормально ухаживать за новорожденной Эмико, пара не стала сразу обращаться в больницу, и Маюми пару дней потерпела дома. Но в течение последующей недели кровотечения стали неконтролируемыми, и семья вернулась в больницу. Врачи решили, что что-то не так с кровью, так как она не хотела свертываться. Они решили дождаться результатов анализов крови Маюми.
Новости были плохи. Положительный результат дал тест на беспощадный рак крови – ОЛЛ (острый лимфобластный лейкоз). В то время как большинство раковых заболеваний обусловлены нарушениями ДНК – клетка удаляет или ошибается в копировании А, Ц, Г или Т и потом восстает против организма – рак Маюми имел более сложное происхождение. Ее ДНК претерпела транслокацию под названием «филадельфийская хромосома» (по городу, в котором она была открыта в 1960 году). Транслокация имеет место в случаях, когда непарные хромосомы по ошибке вступают в кроссинговер и обмениваются участками ДНК. И в отличие от мутационных «опечаток», которые могут произойти с любыми видами, эта ошибка, как правило, поражает высших животных со специфическими генетическими особенностями.
Участки ДНК, отвечающие за изготовление белка – гены – у высших животных занимают очень маленькую часть всей цепочки ДНК, не больше одного процента. Дрозофилисты Моргана предположили, что гены чуть ли не натыкаются друг на друга в хромосомах, будучи нанизанными на них столь же плотно, как натыканы на карте Алеутские острова у берегов Аляски. В действительности же гены – это драгоценные редкие острова Микронезии, разбросанные в пространствах хромосомного Тихого океана.
Итак, чем же занимаются все эти дополнительные участки ДНК? Ученые долго предполагали, что ничем, и пренебрежительно называли их «мусорной ДНК». Неблагозвучное название преследует эти участки до сих пор. Так называемая мусорная ДНК на самом деле содержит тысячи важных участков, которые включают, выключают гены и регулируют их иным образом – «мусор» управляет генами. К примеру, пенисы шимпанзе и других приматов покрыты короткими, размером с ноготь, бугорками (так называемыми шипами). У людей же нет таких «колючек», потому что за последние пару миллионов лет мы потеряли 60 тысяч символов регуляторной «мусорной ДНК» – ДНК, которая могла бы побудить отдельные гены (которые у нас до сих пор есть) создавать шипы. Кроме пощады влагалищам, эта потеря притупляет мужские ощущения во время секса и таким образом продлевает половой акт: это, как подозревают специалисты, способствует тому, что люди образуют пары и остаются моногамными. Другая мусорная ДНК борется с раком, то есть сохраняет нашу жизнь в каждый конкретный момент.
Ученые, к своему удивлению, нашли мусорную, или, как сейчас говорят, «некодирующую», ДНК – внутри самих генов. Клетки кодируют ДНК в РНК добуквенно точно, не пропуская ни одного символа. Но с полной РНК-рукописью в руке клетки прищуриваются, слюнявят красный карандаш и начинают редактировать – столь же беспощадно, как Гордон Лиш резал произведения Раймонда Карвера[46]. Это редактирование состоит в основном из вырезания ненужной РНК и сшивания остальных кусочков вместе, чтобы произвести матричную РНК как таковую. По непонятной причине исключаемые части называют «интронами», а оставляемые – «экзонами». Оставим это на совести ученых… К примеру, сырая РНК со всеми экзонами (прописные буквы) и интронами (строчные) может читаться как: абвгДеежзИйКлмнОпрСТуфхцчшщъыЬэюя. Отредактируем, оставив лишь экзоны, и прочтем: ДИКОСТЬ.
В организмах низших животных вроде насекомых, червей и прочих неприятных тварей содержится лишь пара коротких интронов: если же интроны работают слишком долго или их становится слишком много, клетки запутываются и уже не могут образовывать длинную связную цепочку. Клетки млекопитающих здесь выступают более способными: мы можем просеивать целые страницы ненужных интронов и никогда не потеряем главную нить мысли, которую выражают экзоны. Но эта способность имеет и свои недостатки. Так, РНК-редактирование у млекопитающих – занятие долгое и неблагодарное: человеческий ген в среднем содержит 8 интронов, каждый состоит в среднем из 3500 символов – это в 30 раз длиннее, чем у окружающих их экзонов. Ген для производства самого большого человеческого белка, титина, содержит 178 фрагментов, всего 80 тысяч оснований, тщательно скрепленных вместе. Еще более нелепо растянувшийся ген – дистрофин, Джексонвилл[47] человеческой ДНК – содержит 14 тысяч оснований закодированной ДНК среди 2,2 миллиона оснований ненужных интронов. Лишь одна транскрипция занимает 16 часов. Сплайсинг в итоге производит невероятное количество энергии, и любая ошибка может разрушить важные белки. Одно из генетических расстройств заключается в том, что неправильное сращивание в клетках человеческой кожи стирает все канавки и завитки на кончиках пальцев, оставляя их совершенно гладкими. Ученые назвали этот дефект «болезнью иммиграционных задержек», так как люди с такой мутацией тратят много нервов при переходах границы. Другие нарушения, связанные с расщеплением, более существенны: ошибки в построении дистрофина могут вызвать дистрофию мышц.
Животные мирятся с этой возней и опасностью, так как интроны дают клеткам разнообразие. Определенные клетки могут сейчас или потом пропустить экзон, полностью или частично оставить на месте интрон или же отредактировать РНК другим способом. Таким образом, существование интронов и экзонов дает клеткам свободу для экспериментов. Они могут производить различную РНК в разное время или же настраивать белки для всяческих изменений в организме[48]. Уже по этой причине млекопитающие научились смиряться с существованием огромного количества длинных интронов.
Однако случай с Маюми показал, что толерантность может иметь неприятные последствия. Длинные интроны способствуют тому, что непарные хромосомы запутываются, так как между ними нет экзонов, чтобы беспокоиться по поводу прерывания. «Филадельфийская хромосома» возникает между двумя интронами – один на хромосоме 9, второй на хросомосоме 22 – которые обладают очень большой длиной, что повышает шансы этих отрезков войти в контакт друг с другом. Сначала наши толерантные клетки не рассматривают это соединение как нечто существенное, поскольку оно затрагивает «лишь» интроны, которые скоро будут удалены. Но на самом деле это очень важно. В клетках Маюми соединились два гена, которые никогда не должны были соединяться. Гены, которые в тандеме формируют чудовищный гибридный белок, который не может правильно выполнять работу ни того, ни другого гена. Результатом этого стала лейкемия.
Врачи прописали Маюми химиотерапию, но рак обнаружился на поздней стадии, и ей по-прежнему было очень плохо. По мере того как Маюми становилось хуже, врачи начали думать: «А что будет с Эмико?» ОЛЛ – раковое заболевание, которое распространяется быстро, но не очень. Маюми практически точно уже была больна, когда носила Эмико. Могла ли девочка «заразиться» раком от матери? Рак у беременных – не такая уж и редкость, один случай заболевания приходится примерно на тысячу беременностей, но ни один из врачей никогда не видел зараженный раком плод. Плацента – орган, соединяющий мать с ребенком – мешает любому из подобных вторжений, поскольку, кроме снабжения ребенка питательными веществами и удаления отходов, этот орган также является частью иммунной системы ребенка, блокируя микробы и чужеродные клетки.
Однако плацента – это не гарантия спасения: врачи не советуют беременным женщинам иметь дело с кошачьим туалетом, потому что токсоплазма может проникнуть в плод через плаценту и разрушить его мозг. После ряда исследований и консультаций со специалистами врачи определили, что в некоторых редких случаях – после первого известного случая в 1860-х годах таковых было зафиксировано всего несколько десятков – мать и плод получали раковое заболевание одновременно. Как именно передаются эти недуги, пока выяснить не удалось, однако поскольку мать, плод и плацента так тесно связаны, механизмы передачи и воздействия болезней будут связаны столь же тесно. Возможно, в подобных случаях плод заражает раком мать. Возможно, они оба подвергаются воздействию неизвестных канцерогенов. Возможно, это всего лишь ужасное совпадение: встречаются два случая сильной генетической предрасположенности к раку. Однако врачи, работавшие в 2006 году в Чибе, имели инструмент, которого были лишены предыдущие поколения: генетическое секвенирование. И по мере того как случай Маюми-Эмико прогрессировал, эти врачи использовали генетическое секвенирование, чтобы на первых порах хотя бы решить вопрос: может ли мать передать раковое заболевание своему ребенку. Более того, эта поистине детективная работа пролила свет на некоторые функции и механизмы ДНК, уникальные для млекопитающих черты, которые послужили плацдармом для изучения генетических особенностей млекопитающих.
Конечно, врачи из Чибы не представляли, что их работа будет иметь столь далеко идущие последствия. Их непосредственными интересами были лечение Маюми и уход за Эмико. Благодаря их поддержке, Эмико чувствовала себя хорошо. Действительно, малышка не понимала, почему ее отобрали от мамы, а проведение химиотерапии заставило отказаться от грудного вскармливания, столь необходимого мамам и детям всех видов млекопитающих. Так что, конечно же, малютка Эмико испытывала лишения. Однако она росла и развивалась в соответствии с возрастом и успешно проходила все медосмотры. Казалось, что с ее здоровьем все было по-прежнему нормально.
* * *
Сказанное ниже может здорово напугать молодых мам, но… плод во многом напоминает паразита. После зачатия крошечный эмбрион проникает внутрь своего хозяина (мамы) и укореняется там. Он начинает манипулировать материнскими гормонами, чтобы получать пищу для себя. Он заставляет маму заболевать и маскируется от ее иммунной системы, которая в противном случае может его уничтожить. Словом, делает все, что принято у паразитов. И это мы еще даже не говорили о плаценте.
В мире животных плацента является практически уникальной чертой млекопитающих[49]. Некоторые эксцентричные млекопитающие, отделившиеся от других очень давно (как утконосы), откладывают яйца подобно рыбам, рептилиям, птицам, насекомым, да и практически всем прочим живым существам. Но из примерно 2150 видов млекопитающих 2000 имеют плаценту, включая самых распространенных и успешных зверей вроде грызунов, летучих мышей и человека. Плацентарные млекопитающие вначале были совсем неприметными существами, а затем распространились и в небесах, и в море, и во всех остальных нишах от тропиков до полюсов – и это стало возможным в том числе и потому, что плацента дала им (дала нам!) – существенную поддержку в выживании.
Пожалуй, основное преимущество состоит в том, что плацента позволяет матерям носить своих живых, растущих детенышей прямо внутри себя. Она не беспокоится о том, тепло ли ребенку внутри утробы, в случае опасности может убежать вместе с ним – преимущества, которых лишены существа, мечущие икру в воду или несущие яйца в гнездах. В жизни плода остается гораздо больше времени, чтобы формировать и развивать столь энергоемкие органы, как мозг: способность плаценты выводить наружу отходы жизнедеятельности плода также помогает развитию мозга, ведь благодаря этому эмбрион не плавает в токсичной среде. Более того, поскольку она вкладывает столько энергии в развитие своего малыша – не говоря уже о том, что она в буквальном смысле связана с ним с помощью плаценты – мама млекопитающего чувствует порыв нянчить и воспитывать своих детей, иногда в течение многих лет (ну или шпынять их – тоже в течение многих лет). Такой период длится чрезвычайно долго по сравнению с другими животными, и детеныши млекопитающих отвечают взаимностью: у них формируется необычно сильная привязанность к матерям. В каком-то смысле за формирование этих чувств отвечает именно плацента, превращающая млекопитающих в заботливых существ.
Эта безоблачная картинка становится несколько жуткой, если вспомнить, что плацента, по всей вероятности, происходит от наших старых знакомых – ретровирусов. С биологической точки зрения эта связь действительно имеет смысл. Закрепляться на клетках – это выдающаяся способность вирусов: они сливают свои «конверты» (наружную оболочку) с клеткой, перед тем как ввести в нее свой генетический материал. Когда шарик эмбриональной клетки попадает в матку и укореняется там, эмбрион тоже частично связывается с клетками матки, используя специальные связующие белки. А ДНК, которую для построения этих белков используют приматы, мыши и другие млекопитающие, состоит из тех же генов, которые приходится использовать ретровирусам, чтобы прикреплять и соединять свои «конверты» с клеткой. Более того, матка плацентарных млекопитающих при своей работе в значительной степени опирается на другие вирусоподобные ДНК, используя специальный прыгающий ген под названием MER20, чтобы переключать 1500 генов в клетках матки. В случае с обоими органами кажется, что мы еще раз собрали удобный генетический материал от паразита и адаптировали его к собственным нуждам. В качестве бонуса, вирусные гены плаценты даже обеспечивают дополнительный иммунитет, так как присутствие ретровирусных белков (даже вытеснение или оттеснение их на второй план) отпугивает других микробов от проникновения в плаценту.
Важной частью иммунной функции плаценты является и то, что она фильтрует любые клетки, которые могут попытаться внедриться в плод, в том числе и раковые клетки. К сожалению, другие черты плаценты, напротив, делают ее привлекательной для рака. Плацента производит гормоны роста, чтобы способствовать энергичному делению клеток плода, и некоторые виды рака также прекрасно развиваются на этих гормонах. Плацента, кроме того, впитывает огромное количество крови и откачивает питательные вещества, которые могли бы пригодиться плоду. Это означает, что разновидности рака крови наподобие лейкемии могут укрыться внутри плаценты и процветать. Раковые заболевания генетически запрограммированы метастазироваться, как меланома, вызывающая рак кожи, и могут вместе с кровью скользить по всему организму; они находят плаценту весьма гостеприимной.
На деле меланома оказалась самой распространенной формой рака, которую мать и плод получают одновременно. Первый зафиксированный случай совместного заболевания раком был описан в 1866 году в Германии: блуждающая меланома случайным образом пустила корни в печени у матери и в коленке у ребенка. И мать, и ребенок умерли в течение девяти дней. Другой ужасный случай произошел с 28-летней жительницей Филадельфии, имя которой осталось зафиксировано врачами лишь как «Р. Мак-К.». Эта история началась с тяжелого солнечного ожога в апреле 1960 года. Вскоре после этого между ее плечами возникла бородавка диаметром примерно один сантиметр. Она кровоточила всякий раз, как женщина до нее дотрагивалась. Врачи удалили бородавку, и никто не вспоминал вплоть до мая 1963 года, когда женщина была уже несколько недель как беременна. Во время осмотра врачи заметили узелок под кожей на животе. К августу стало очевидным, что узелок растет быстрее, чем живот беременной, а по всему телу больной начали появляться другие болезненные узелки. К январю поражения распространились на ее конечности и лицо, и врачи решили проводить кесарево сечение. Мальчик появился на свет здоровым: почти три килограмма весом. Но брюшная полость матери была покрыта десятками опухолей, некоторые из которых были черного цвета. Неудивительно, что роды окончательно забрали оставшиеся силы у матери. Через час после родов ее пульс упал до 36 ударов в минуту, и хотя врачи пытались всячески реанимировать ее, она умерла в течение нескольких недель.
А что же произошло с ребенком Мак-К.? Поначалу была надежда, что все обойдется. Несмотря на широко распространившийся рак, доктора не увидели ни одной опухоли в матке или плаценте матери – местах ее контакта с сыном. И хотя мальчик был слабым, тщательное исследование каждой складочки на его теле в поисках подозрительных родинок результата не принесло. Однако врачи не могли проверить, что происходит внутри организма. Через 11 дней на коже новорожденного начали появляться маленькие темно-синие пятна. После этого состояние мальчика резко ухудшилось. На теле появлялись все новые опухоли, убившие ребенка за семь недель.
У Маюми была лейкемия, а не меланома, но в каком-то смысле в Чибе повторилась филадельфийская драма сорокалетней давности. В больнице состояние Маюми ухудшалось с каждым днем, ее иммунная система была ослаблена после трех недель химиотерапии. В конце концов она подхватила бактериальную инфекцию и слегла с энцефалитом – воспалением головного мозга. У нее начались судороги и конвульсии – результат паники и перебоев в деятельности мозга; сердце и легкие также давали сбои. Несмотря на все мероприятия по реанимации, Маюми умерла через два дня после того, как подхватила инфекцию.
Несчастья на этом не закончились: в октябре 2006 года, через девять месяцев после похорон жены, Хидео пришлось вернуться в госпиталь с Эмико. У когда-то здоровой и крепкой девочки была жидкость в легких и, что более тревожно, кроваво-красная ссадина, уродующая правую щеку и подбородок. На МРТ эта преждевременно развивающаяся щека выглядела неестественно большой – такой же, как крохотный мозг Эмико (надуйте свою щеку настолько туго, пока хватает воздуха, и ее размер все равно не сравнится с тем, что было у маленькой девочки). Врачи из Чибы диагностировали саркому (рак соединительной ткани), предполагая, что она находится внутри щеки. Но в памяти был случай с Маюми, поэтому медики проконсультировались с экспертами в Токио и Англии и решили изучить ДНК опухоли, чтобы посмотреть, что там можно найти.
Там оказалась филадельфийская хромосома. И не только она. Напомним, что этот кроссинговер имеет место между двумя чрезвычайно длинными интронами, 68 000 символов на одной хромосоме и 200 000 на другой (для сравнения: эта глава содержит чуть больше 30 000 символов). Плечи двух хромосом могли пересечься в одной из многих тысяч точек. Но в ДНК опухолей Маюми и Эмико хромосомы пересеклись в одной и той же точке, даже в одном и том же символе. И это не было случайным. Если не считать места размещения, рак Эмико был практически таким же, как и у матери.
Но кто кого заразил? Ученым раньше никогда не приходилось решать эту проблему. Даже случай с Мак-К. был противоречивым, потому что смертельные опухоли появились только после наступления беременности. Врачи подняли анализ крови, взятый у Эмико при рождении, и определили, что рак там присутствовал уже тогда. Дальнейшие генетические тесты показали, что в нормальных (не опухолевых) клетках Эмико не было филадельфийской хромосомы. То есть девочка не унаследовала никаких предрасположенностей к этому раку – он появился в сороканедельный промежуток между зачатием и родами. Более того, нормальные клетки Эмико содержали, как и ожидалось, ДНК и от матери, и от отца. Но в клетках опухоли на ее щеке не было ДНК Хидео: только Маюми. Это бесспорно доказывало, что Маюми передала рак Эмико, а не наоборот.
Ученые могли торжествовать, но это чувство было приглушено. Как часто случается в медицинских исследованиях, самые интересные случаи возникают из самых ужасных страданий. Практически в каждом из предыдущих случаев, когда плод и мать заболевали раком одновременно, смерть обоих наступала быстро, обычно в течение года. Маюми уже умерла, и когда врачи прописали химиотерапию 11-месячной Эмико, они, безусловно, понимали, что шансов ничтожно мало.
Генетики, изучавшие этот случай, корпели над совсем иной проблемой. Распространение рака в этом случае по сути являлось трансплантацией клеток от одного человека к другому. Если бы Эмико трансплантировали орган больной матери или же пересадили материнские ткани на щеку, организм отверг бы их как чужеродные. Тем не менее рак неожиданно пустил корни, не вызвав срабатывания защитных систем плаценты или соответствующей реакции со стороны иммунной системы. Как? Ученые в итоге нашли ответ с помощью участка ДНК, далекого от филадельфийской хромосомы – в области под названием ГКГС.
* * *
Еще во времена Линнея биологи занимались увлекательным делом, стараясь перечислить все черты, которые делают млекопитающих млекопитающими. В соответствии с происхождением термина (от лат. mamma — грудь) начать следует с выкармливания детенышей. Грудное молоко не только служит младенцу пищей, но и внедряет в его организм десятки генов, в основном в кишечный тракт, но, возможно, и в такие места, как мозг. Мы ни в коем случае не хотим пугать будущих матерей, но, похоже, искусственное молоко, даже с таким же составом углеводов, жиров, белков, витаминов и прочих веществ, просто не может улучшить ДНК младенца подобным образом.
Другие важные черты млекопитающих – это волосы («прически» есть даже у китов и дельфинов), уникальное строение внутреннего уха и челюстей, а также наша странная привычка пережевывать пищу (к примеру, рептилии так не делают). Но на микроскопическом уровне единственное место, где можно проследить происхождение млекопитающих, это ГГКС, главный комплекс гистосовместимости. ГГКС есть практически у всех позвоночных – это набор генов, помогающих иммунной системе. Однако этот комплекс особенно важен именно для млекопитающих. Это один из наиболее богатых генами участков ДНК: около ста генов, упакованных на небольшом пространстве. И так же, как в случае с механизмами редактуры интронов и экзонов, мы обладаем более сложным ГГКС[50], чем другие живые существа. Некоторые из этой сотни генов имеют более тысячи самых разных вариаций в человеческих организмах, обеспечивая практически неограниченное число комбинаций, которые могут наследоваться. ГГКС существенно различается даже у близких родственников, а между случайными людьми различия в этом наборе генов в сотни раз больше, чем между прочими участками ДНК. Ученые иногда говорят, что люди более чем на 99 % генетически идентичны. Однако ГГКС это никак не касается.
У белков ГГКС есть две основные задачи. Во-первых, некоторые из них собирают случайные молекулы изнутри клетки и помещают их на клеточную стенку в качестве своеобразного дисплея. Этот «дисплей» позволяет другим клеткам, в особенности иммунным клеткам-«палачам», получать информацию о том, что происходит внутри клетки. Если «палач» видит, что ГГКС собрал только нормальные молекулы, он не обращает внимания на клетку. Если же он видит нечто аномальное – фрагменты бактерий, раковые белки, другие признаки чего-то противо естественного – то может атаковать. Различие ГГКС млекопитающих в этом случае приходится весьма кстати, потому что за различными белками ГГКС закреплены обязанности предупреждать об опасностях. Соответственно, чем разнообразнее эти белки, тем с большим количеством опасностей организм может бороться. А самое главное – то, что, в отличие от других признаков, ГГКС-гены не мешают друг другу. Мендель первым определил доминантные признаки, случаи, когда одни версии генов «побеждают» остальные. В случае с ГГКС все гены работают независимо друг от друга, и ни один ген не скрывает другой. Они кооперируются; они кодоминируют.
Во-вторых (это предназначение можно назвать более философским), ГГКС позволяет нашим организмам разграничивать «свое» и «чужое». Монтируя белковые фрагменты, гены ГГКС вызывают появление крохотных пучков на поверхности каждой клетки. Поскольку живые существа имеют уникальную комбинацию генов ГГКС, каждый из этих пучков обладает уникальной компоновкой цветов и завитков. Все чужеродные элементы, попадающие в организм (к примеру, клетки животных или других людей), конечно, обладают набором генов ГГКС, которые образуют их собственные уникальные пучки. Наша иммунная система работает так аккуратно, что может отличить эти пучки от своих, и – даже если эти клетки не содержат никаких признаков заболеваний или паразитов – отправляет войска для истребления захватчиков.
Уничтожение чужаков – это, как правило, хорошо. Но подобная бдительность ГГКС имеет и побочный эффект: наши тела отвергают трансплантируемые органы, пока реципиенты не принимают наркотики для подавления иммунной системы. Порой и это не помогает. Пересадка органов от животных могла бы решить проблему хронической нехватки донорских органов во всем мире, но животные имеют столь аномальные (для нас) комплексы гистосовместимости, что человеческие тела незамедлительно их отвергают. Человеческий организм даже разрушает ткани и кровеносные сосуды вокруг пересаженных животных органов, подобно тому, как отступающие солдаты поджигают поля, чтобы врагу не осталось пропитания. Абсолютно парализовав иммунную систему, врачи добивались того, что больные могли прожить пару недель с сердцем или печенью обезьяны, но в итоге ГГКС всегда брали верх.
По тем же причинам ГГКС усложнил эволюцию млекопитающих. По логике самка млекопитающего должна атаковать плод внутри нее как чужеродное образование, так как половина ДНК, ГГКС и прочих компонентов организма ей не принадлежит. К счастью, плацента сглаживает этот конфликт, ограничивая доступ к плоду. Кровь попадает в плаценту, но не проникает непосредственно к плоду, потому что плацента пропускает только питательные вещества. В результате ребенок, подобный Эмико, должен оставаться совершенно независимым, невидимым для иммунных клеток Маюми, и эти клетки никогда не должны проникнуть в организм Эмико. Даже если бы некоторые из них преодолели плацентарную преграду, собственная иммунная система Эмико смогла бы опознать чужие элементы ГГКС и уничтожить их.
Но когда ученые тщательно исследовали ГГКС зараженных раком клеток крови Маюми, они обнаружили нечто, что могло бы вызвать восхищение своим умом, не будь оно столь зловещим. У человека ГГКС расположен в коротком плече шестой хромосомы. Специалисты обнаружили, что это плечо в раковых клетках Маюми было даже короче, чем нужно, так как из клеток был удален ГГКС. Какая-то неизвестная мутация просто стерла его из своих генов. Она оставила эти клетки функционально незаметными снаружи, так что ни плацента, ни иммунная система Эмико не смогли классифицировать или опознать их. Организм Эмико не имел возможности изучить эти клетки и доказать, что они чужеродные, а тем более зараженные раком.
В целом ученые смогли свести заражение Маюми раком к двум причинам: филадельфийская хромосома, которая сделала клетки злокачественными, и мутация ГГКС, сделавшая клетки невидимыми и позволившая им проникнуть в щеку Эмико и укорениться там. Шансы на осуществление каждой из этих причин были низки; шансы на то, что и то, и другое произойдет в одних и тех же клетках, в одно время, в организме женщины, которая оказалась беременной, – бесконечно низкими. Низкими, но не нулевыми. Как следствие, ученые теперь подозревают, что в большинстве случаев, когда раковое заболевание передавалось от матери к ребенку, действие ГГКС прекращалось или нарушалось подобным образом.
* * *
Если пойти еще дальше, то ГГКС может помочь пролить свет на еще один аспект истории Хидео, Маюми и Эмико, на тему, которая уходит корнями к первым дням существования млекопитающих. Развивающийся плод должен дирижировать целым оркестром генов внутри каждой клетки, побуждая одни участки ДНК «играть» громче и «приглушая» другие. На ранних сроках беременности наиболее активные гены – это те, которые млекопитающие унаследовали от яйцекладущих, ящероподобных предков. Пролистав учебник биологии, мы будем неприятно удивлены, как странно похожи эмбрионы птиц, ящериц, рыб, людей и прочих существ в самом начале своего существования. У людей даже есть рудиментарные жаберные щели и хвост – самые что ни есть атавизмы из нашего животного прошлого.
Через пару недель плод приглушает рептильные гены, превращается в совокупность генов, уникальных для млекопитающих, и совсем скоро начинает напоминать существо, которое уже можно назвать в честь бабушки. Впрочем, даже на этой стадии, если правильные гены замолчат или изменятся, могут появиться атавизмы (так называемые генетические пережитки). К примеру, некоторые люди рождаются с дополнительными сосками, как у свиноматки[51]. Большинство лишних сосков натыкано на «молочной линии», которая идет вертикально вниз по туловищу, но они могут появиться и совсем в других местах, вплоть до пяток. Другие атавистичные гены заставляют людей покрываться шерстью по всему телу, включая щеки и лоб. Ученые даже могут различить такие случаи атавизма, как, извините за выражение, «собачья морда» и «обезьянья морда», в зависимости от толщины, цвета и других характеристик волос. У младенцев с пропущенным фрагментом на кончике пятой хромосомы развивается так называемый синдромом кошачьего крика (от англ. cri-du-chat), названный так из-за кошачьего писка и воя, который издают страдающие этим синдромом дети.
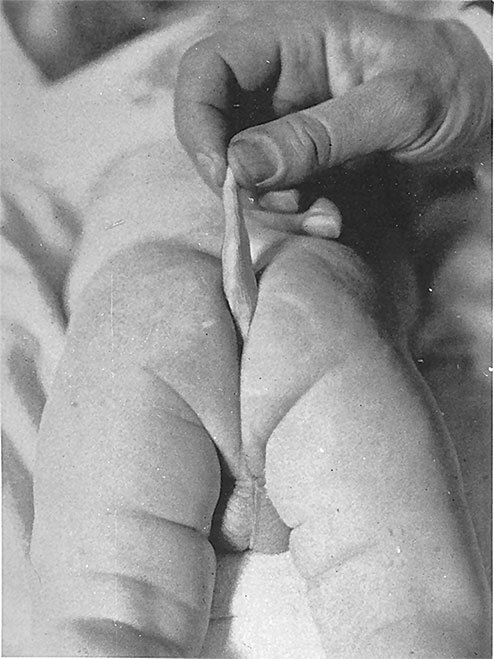
Крепкий и здоровый мальчик родился с хвостом: это генетический возврат к нашему обезьяньему прошлому (Ян Бондесон, “A Cabinet of Medical Curiosities”, публикуется по разрешению правообладателя)
Некоторые малыши рождаются и с хвостами. Эти хвосты, обычно находящиеся над ягодицами, содержат мускулы и нервы и достигают 13 сантиметров в длину и 2,5 – в толщину. Иногда появление хвоста является побочным эффектом рецессивного генетического расстройства, вызывающего анатомические проблемы по всему телу, однако нередки и случаи, когда хвост появляется у ребенка, в остальном совершенно нормального. Педиатры сообщают, что такие мальчики и девочки могут сворачивать свои хвостики вверх, подобно слоновьему хоботу, и что хвост непроизвольно сокращается, когда малыш кашляет или чихает[52]. Опять-таки, у всех плодов в шестинедельном возрасте есть хвосты, но обычно на восьмой неделе они исчезают: клетки хвоста отмирают, и организм поглощает лишнюю ткань. Хвосты, которые сохраняются до самого рождения, обычно возникают в результате спонтанных мутаций, однако некоторые дети с хвостами имеют хвостатых родственников. Большинство таких безвредных придатков удаляется сразу после рождения, но некоторые не беспокоят своих хозяев и во взрослом возрасте.
У всех нас есть другие атавизмы, которые спокойно спят внутри организма, ожидая подходящего генетического сигнала для пробуждения. Известно, что есть один генетический атавизм, которого не избежал никто из нас. Примерно через сорок дней после зачатия внутри носовой полости человека развивается трубка длиной примерно в пятую часть миллиметра, с разрезом на каждом конце. Эта зачаточная структура, вомероназальный орган, распространена среди млекопитающих, которым помогает ориентироваться в пространстве. Этот орган действует как дополнительный нос, причем может уловить не только те запахи, что ощущает любое обладающее обонянием существо (дым, гнилая пища и др.), – он способен определять феромоны. Феромоны – это завуалированные ароматы, которые действуют подобно гормонам; однако в то время как гормоны дают нашим телам инструкции изнутри, феромоны сообщают информацию (по крайней мере своеобразные «подмигивания» и «многозначительные взгляды») другим представителям нашего вида.
Поскольку феромоны могут способствовать социальным взаимоотношениям, в особенности интимным контактам, выключение вомероназального органа (ВНО) у некоторых млекопитающих может иметь неприятные последствия. В 2007 году специалисты из Гарвардского университета генетически перепрограммировали несколько самок мыши, отключив их ВНО. Когда эти мыши находились в одиночестве, практически ничего не изменилось, животные вели себя нормально. Однако когда их поместили вместе со здоровыми мышами, подопытные животные набросились на них как римляне на сабинянок. Они залезали на самок и, несмотря на отсутствие необходимого «инструмента», начинали двигать бедрами вперед и назад. Необычные самки даже пищали так же, как самцы, в момент оргазма испуская ультразвуки, которые до этого были зафиксированы только у мужских особей.
Люди в меньшей степени полагаются на запах, чем прочие млекопитающие. В течение нашей эволюции мы потеряли или изменили около 600 общих для млекопитающих генов, отвечающих за обоняние. Поэтому тем более поразительно, что наши гены все еще формируют ВНО. Ученым даже удалось обнаружить у плода нервы, посылающие сигналы из этого органа в мозг, и проследили, как сигналы проходят туда и обратно. Тем не менее по необъяснимым причинам наши организмы, тратя силы и ресурсы на создание и «подключение» органа, в итоге пренебрегают этим шестым чувством, и через 16 недель оно начинает увядать. К взрослому возрасту способность ощущать феромоны настолько сходит на нет, что большинство специалистов спорят даже о том, есть ли у человека ВНО, не говоря уже о полноценном его функционировании.
Споры о человеческом ВНО вписываются в контекст более масштабного и не менее приметного исторического спора о предполагаемых связях между ароматами, сексуальностью и поведением. В конце XIX века один из самых эксцентричных друзей Зигмунда Фрейда, доктор Вильгельм Флисс, утверждал, что именно в носу кроется самый мощный сексуальный потенциал во всем организме. Его теория «назального невроза» была ненаучной мешаниной из нумерологии, рассказов о мастурбации и менструации, схем гипотетических «генитальных точек» внутри носа и опытов, которые включали в себя втирание кокаина в слизистые оболочки подопытных людей и мониторинг их либидо. Неспособность реально объяснить хоть какой-то аспект человеческой сексуальности никак не влияла на популярность Флисса: напротив, его работа повлияла на Фрейда, и тот позволил Флиссу лечить своих пациентов (поговаривают, что и самого Фрейда), прописывая им мастурбацию. Идеи Флисса в конце концов умерли, но псевдонаучная сексология по-прежнему процветает и будет процветать. В последние лет 20 торговцы продали очень много парфюмерии и туалетной воды, обогащенной феромонами, которые якобы могут издавать аромат, который будет настоящим сексуальным магнитом (дышите, дышите!). В 1994 году ученый, работающий на американскую армию, просил у военно-воздушных сил 7,5 миллиона долларов на разработку «гей-бомбы». Его предложение описывало «неприятный, но совершенно несмертельный» вид вооружения. Над вражескими войсками (состоящими преимущественно из мужчин) должны были распыляться феромоны, и их запах должен был как-то – детали, по крайней мере в воображении ученого, были весьма фрагментарны – вызвать у солдат такую вспышку похоти, что они побросали бы свое оружие и начали оргию вместо войны. Нашим же солдатам, одетым в противогазы, оставалось бы просто окружить врага[53].
Отбросив в сторону парфюмерию и гей-бомбы, отметим, что влияние феромонов на поведение человека доказано и признанными научными работами. Сорок лет назад ученые определили, что феромоны могут скорректировать менструальные циклы живущих вместе женщин, приведя их примерно к одинаковым датам (нет, это не городская легенда). И в то время как мы противимся тому, чтобы сводить человеческую любовь к взаимодействию химических веществ, практика показывает, что грубая человеческая похоть – или, говоря более сдержанно, влечение – во многом обусловлена в том числе и запахом. Авторы старых трудов по антропологии, не говоря уже о самом Чарльзе Дарвине, удивлялись, что у представителей неразвитых обществ никогда не было привычки целоваться: потенциальные любовники не ласкали, а обнюхивали друг друга. Впоследствии шведские врачи провели несколько экспериментов, перекликавшихся с опытами гарвардцев над самками мышей. Врачи подвергали действию феромона из мужского пота представителей трех групп: мужчин-гетеросексуалов, женщин-гетеросексуалов, мужчин-гомосексуалистов. Во время этого эксперимента мозг женщин и мужчин-гомосексуалистов показал признаки умеренного возбуждения, а у мужчин-гетеросексуалов этого не наблюдалось. Логично последовавший за этим обратный эксперимент показал, что феромоны из женской мочи могут возбудить мужчин-гетеросексуалов и женщин-лесбиянок, но не гетеросексуальных женщин. Это значит, что мозг людей с различной сексуальной ориентацией по-разному реагируют на запахи представителей своего и чужого пола. Это не является доказательством того, что у человека сохранился ВНО, но заставляет предположить, что мы в какой-то мере сохранили способность чувствовать феромоны, вероятно, генетически переложив эти обязанности на наш «основной» нос.
Возможно, самым простым доказательством того, что запахи могут влиять на сексуальное возбуждение, можно получить с помощью нашего старого знакомого – ГГКС. Нравится вам это или нет, наше тело афиширует свой ГГКС всякий раз, когда мы просто поднимаем руку. В подмышечной впадине человека содержится большое количество потовых желез, и, смешиваясь с выделяемой водой, солью и жиром, феромоны разъясняют, какие гены ГГКС имеются у людей для защиты от заболеваний. Эти сигналы ГГКС поступают в ваш нос, где местные клетки могут проанализировать, насколько ГГКС другого человека отличается от вашего собственного. Это помогает при оценке потенциального партнера, поскольку вы можете примерно определить, насколько здоров будет ваш общий ребенок. Помните, что гены ГГКС не препятствуют друг другу: они кодоминируют. Соответственно, если ГГКС мамы и папы существенно различается, ребенок унаследует их общую сопротивляемость болезням. Чем больше сопротивление генетическим дефектам, тем здоровее ребенок.
Эта информация просачивается в наш мозг на подсознательном уровне, но может дать о себе знать, когда мы вдруг посчитаем случайного прохожего необъяснимо сексуальным. Это невозможно установить без тестирования, но если провести исследования, с большой вероятностью окажется, что его/ ее ГГКС существенно отличается от нашего. В различных экспериментах, когда женщинам давали понюхать футболки, в которых спали незнакомые им мужчины, участницы называли самыми сексуальными тех обладателей футболок, чей ГГКС больше всего отличался от их собственного. Справедливости ради отметим, что другие исследования показали: в тех местностях, где генетическое разнообразие само по себе велико (к примеру, в некоторых регионах Африки), наличие существенных различий в ГГКС не подразумевает сексуального влечения. Однако ГГКС-привлекательность наблюдается в районах с генетически более однородным населением – это показали эксперименты в штате Юта. Это открытие также может помочь объяснить, почему нам противна даже мысль о сексуальных отношениях с братьями или сестрами: сходство наших ГГКС значительно выше среднего.
С другой стороны, бессмысленно сводить всю любовь к химикатам: это гораздо более сложный процесс. Но мы не так далеко ушли от наших друзей млекопитающих, как это можно себе представить. Химические вещества могут воспламенить и поддерживать любовь, а самые мощные из них – феромоны, которые рекламируют ГГКС. Если два человека из генетически однородного региона – как Хидео и Маюми – встретят друг друга, влюбятся и решат завести ребенка, то (насколько мы можем объяснить это биологически) их гистосовместимые комплексы захотят что-то с этим сделать. Еще более актуальной эту ситуацию делает то, что исчезновение этих общих ГГКС позволило раку практически уничтожить Эмико.
Фактически выживаемость как матерей, так и детей с одновременно приобретенным раком остается крайне низкой, несмотря на то что медицина с 1866 года сделала большой скачок вперед. Но, в отличие от материнского, организм Эмико хорошо отреагировал на лечение, в том числе потому, что врачи смогли подобрать химиотерапию, подходящую к ДНК ее опухоли. Эмико в отличие от большинства детей, больных тем же типом рака, даже не понадобились мучительные трансплантации костного мозга. Эмико и сейчас (тьфу-тьфу-тьфу) жива, ей уже почти десять лет, она живет в Чибе.
Мы не считаем рак инфекционным заболеванием. Тем не менее близнецы могут передать рак друг другу еще в утробе матери; донорские органы могут передать рак органам реципиента; и рак действительно может передаваться от матерей к неродившимся детям, несмотря на защищающую плод плаценту. Вместе с тем случай с Эмико доказывает, что даже запущенный рак, обнаруженный у плода, не обязательно смертелен. Такие случаи, кроме того, расширили наше представление о роли ГГКС в образовании злокачественных опухолей, и показывают, что плацента более проницаема, чем представляют себе некоторые ученые. «Я склоняюсь к мысли, что, возможно, клетки в небольшом количестве проходят [через плаценту] постоянно, – говорит генетик, который работал с семьей Эмико. – Изучая очень редкие случаи в медицине, можно узнать очень много».
Более того, другие дотошные ученые установили, что большинство, если вообще не каждый из нас носит в себе тысячи скрытых клеток от наших матерей, тайком забравшихся к нам «на борт» еще с тех пор, когда мы были эмбрионами, и схоронившихся в наших жизненно важных органах. Каждая мать также практически гарантированно хранит внутри себя несколько клеток-«подарочков» от каждого из своих детей. Подобные открытия извлекают новые увлекательные грани нашей биологии. Как подумал один ученый: «Что представляет собой наше психологическое “я”, если наш мозг не полностью наш собственный?» Более того, эти данные показывают, что даже после смерти матери или ребенка клетки от одного организма продолжают жить в другом. Это другая сторона связи между материнским и детским организмами, которая делает млекопитающих особенными существами.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава 3.1. Реинтродукция в природу выращенных в неволе крупных хищных млекопитающих
Глава 3.1. Реинтродукция в природу выращенных в неволе крупных хищных млекопитающих Материал и методика Метод разрабатывался в вольерных (100 м2) и в полевых условиях, на выращенных в неволе 22 взрослых волках (Canis lupus cubanensis Ognev), разделенных на 4 группы. I группа — 2 ›, II группа —
Какие перемены наступают у впадающих в зимнюю спячку млекопитающих?
Какие перемены наступают у впадающих в зимнюю спячку млекопитающих? С физиологической точки зрения зимняя спячка млекопитающих характеризуется ослаблением всех функций жизнедеятельности организма (см. таблицу) до того минимума, который позволил бы им пережить
Что делают для стимуляции противоракового иммунитета.
Что делают для стимуляции противоракового иммунитета. — Наверное, это еще не умеют? — Да, в отношении раковых антигенов не умеют. — А что же делают, чтобы стимулировать противораковый иммунитет? Когда произносишь слово «история», возникают представления
Какие особенности анатомии верблюда делают его идеально приспособленным к условиям пустынь и сухих степей?
Какие особенности анатомии верблюда делают его идеально приспособленным к условиям пустынь и сухих степей? Ряд особенностей анатомии верблюда делает его уникально приспособленным к жизни в пустыне. В верблюжьем горбе содержится большое количество жира (в двух горбах
Почему вы так упорно путаете любовь с физиологией? Я полагаю, что любовь – это чувство , ей чужды всякие гормоны и инстинкты, об них никто не думает, когда влюбляется
Почему вы так упорно путаете любовь с физиологией? Я полагаю, что любовь – это чувство, ей чужды всякие гормоны и инстинкты, об них никто не думает, когда влюбляется А собственно, никто и не спорит с тем, что любовь – это чувство. Это и для нас в первую очередь чувство!
Глава 3. Ручные гены{3}
Глава 3. Ручные гены{3} В июле 2004 года, пока мы с моими коллегами добывали в Арктике первые образцы тиктаалика, Рэнди Дан, молодой сотрудник моей лаборатории, трудился в поте лица в Чикаго над генетическими экспериментами с зародышами акул и скатов. На морских пляжах нередко
Глава 1: Гены. Энтузиасты. ДНК
Глава 1: Гены. Энтузиасты. ДНК Bondeson, Jan. A Cabinet of Medical Curiosities. – W. W. Norton, 1999.* В этой книге есть замечательная глава о материнских впечатлениях, в том числе о мальчике-рыбе из Неаполя.Дарвин, Чарльз. Происхождение видов путем естественного отбора. М.: Просвещение, 1989.Henig, Robin Marantz. T e
Глава 8: Любовь и атавизмы
Глава 8: Любовь и атавизмы Bondeson, Jan. A Cabinet of Medical Curiosities. W. W. Norton, 1999.* Великолепный раздел о человеческих хвостиках из книги, полной шокирующих и жутких сюжетов из истории анатомии.Isoda, T., Fo r d A., et al. Immunologically Silent Cancer Clone Transmission from Mother to Of spring // Proceedings of the National Academy of Sciences of the United States of
Глава 14. Любовь во времена палеолита
Глава 14. Любовь во времена палеолита Половое поведение и эволюция человека Изучение полового поведения приматов представляет интерес в аспектах эволюции человека. Некоторые авторы исходили из неверных представлений о подавляющей роли секса и неупорядоченных половых
Глава 5 Женская любовь: будь моим малышом
Глава 5 Женская любовь: будь моим малышом Доктор Г.-У. Лонг устал от перешептываний. Его коллеги-медики делились друг с другом историями о пациентах, имевших разнообразные сексуальные проблемы. Существовали труды и книги о сексе, но написаны они были исключительно для
Глава 6 Мужская любовь: это моя территория!
Глава 6 Мужская любовь: это моя территория! Как и Маркус Хайнрихс до начала своих экспериментов, вы можете сомневаться в том, что одно вещество (а хоть бы и несколько) способно послужить источником такого сложного явления, как человеческая любовь. Подобная идея умаляет
Глава 7 Любовь – наркотик?
Глава 7 Любовь – наркотик? Привязанность двух людей бывает сильной и захватывающей, однако химическая природа того клея, который удерживает их вместе дольше первых нескольких дней горячей страсти, совсем не та, о которой говорится в викторианских романах или в рекламе
Глава 9 Новый взгляд на любовь
Глава 9 Новый взгляд на любовь Представленная нами гипотеза может кому-то показаться довольно мрачной. Любовь – это зависимость, причем не в образном, а в прямом смысле слова. Некоторые из нас от природы склонны к внебрачному сексу. Даже пингвины на полюсе, те самые, из