Глава 23. Обмен аминокислот. Динамическое состояние белков организма
Глава 23. Обмен аминокислот. Динамическое состояние белков организма
Значение аминокислот для организма в первую очередь заключается в том, что они используются для синтеза белков, метаболизм которых занимает особое место в процессах обмена веществ между организмом и внешней средой. Аминокислоты непосредственно участвуют в биосинтезе большого количества других биологически активных соединений, регулирующих процессы обмена веществ в организме, таких как нейромедиаторы и гормоны. Аминокислоты служат донорами азота при синтезе всех азотсодержащих небелковых соединений, в том числе нуклеотидов, гема, креатина, холина и др.
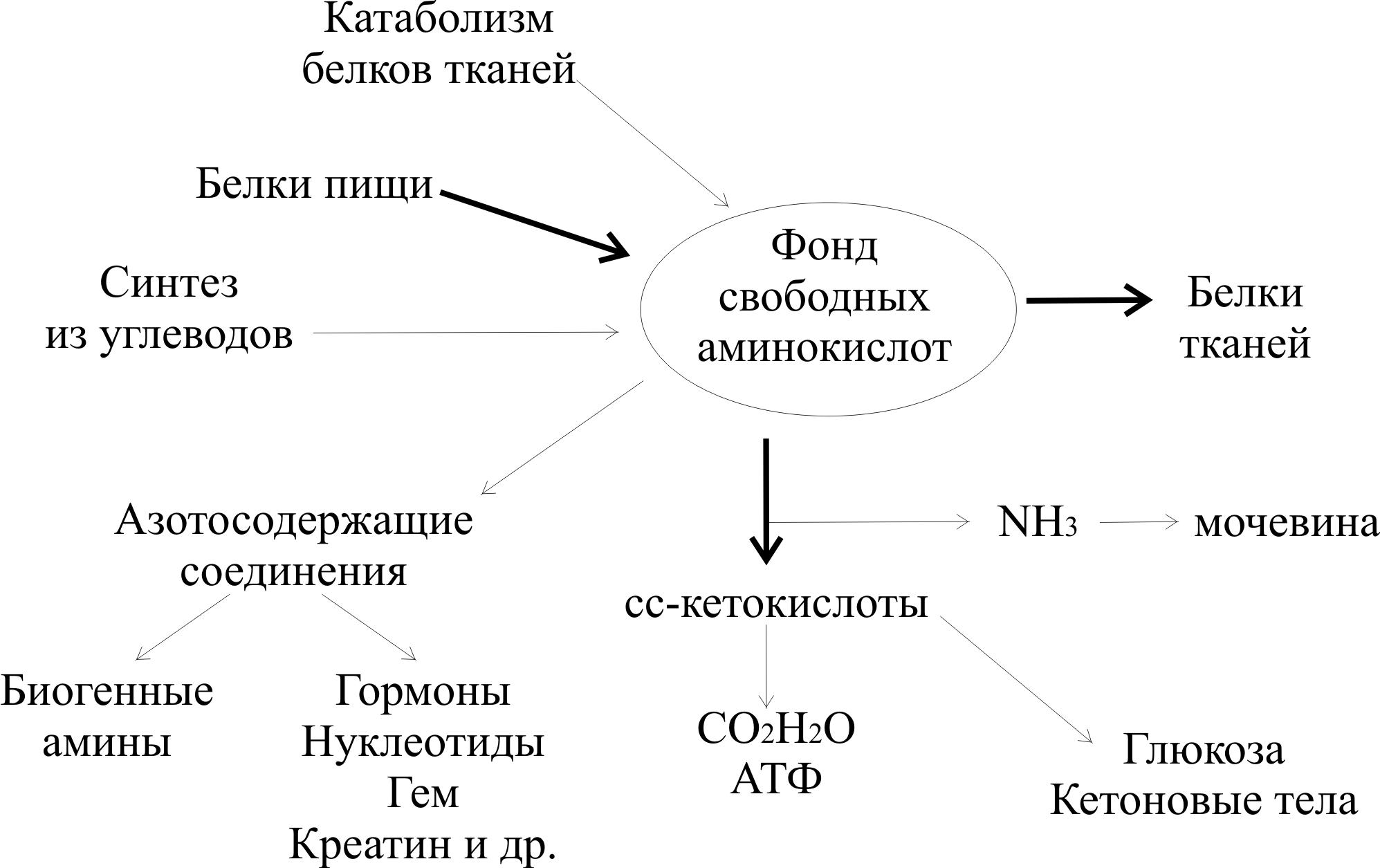
Рис. 23.1. Общая схема метаболизма аминокислот в организме
Катаболизм аминокислот является источником энергии для синтеза АТФ. Энергетическая функция аминокислот становится значимой при голодании, некоторых патологических состояниях (сахарный диабет). Именно обмен аминокислот осуществляет взаимосвязь многообразных химических превращений в живом организме.
Большая часть аминокислот входит в состав белков, количество которых в организме взрослого человека составляет примерно 15 кг.
Какой-либо специальной формы депонирования аминокислот и белков, подобно глюкозе или жирным кислотам не существует. Поэтому резервом аминокислот могут служить все функциональные и структурные белки тканей, но преимущественно белки мышц. В организме человека в сутки распадается на аминокислоты около 400 г белков, примерно такое же количество синтезируется. Поэтому тканевые белки не могут восполнять затраты аминокислот при их катаболизме и использовании на синтез других веществ. Период полураспада белков различен – от нескольких минут до нескольких суток. Первичными источниками аминокислот не могут служить и углеводы, так как из них синтезируется только углеродная часть молекулы, а аминогруппа поступает от других аминокислот. Следовательно, основным источником аминокислот организма служат белки пищи.
Показателем, отражающим интенсивность аминокислотного обмена, является азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством выделяемого азота (преимущественно в виде мочевины и аммонийных солей).
Переваривание белков в желудочно-кишечном тракте
Переваривание белков начинается в желудке под действием ферментов желудочного сока. За сутки его выделяется до 2,5 литров и он отличается от других пищеварительных соков сильно кислой реакцией, благодаря присутствию свободной соляной кислоты, секретируемой обкладочными клетками слизистой желудка.
Секреция соляной кислоты представляет активный транспорт, осуществляемый протонной АТФ-азой с затратой АТФ.
Роль соляной кислоты:
1. денатурирует белки;
2. стерилизует пищу;
3. вызывает набухание труднорастворимых белков;
4. активирует пепсиноген;
5. создает рН-оптимум для действия пепсина;
6. способствует всасыванию железа;
7. вызывает секрецию секретина в двенадцатиперстной кишке.
В желудочном соке содержатся протеолитические ферменты пепсин, гастриксин и реннин. Главным из них является пепсин. Он вырабатывается главными клетками слизистой желудка в виде профермента пепсиногена. Активация его осуществляется соляной кислотой (медленная) и аутокаталитически пепсином (быстрая) путем отщепления фрагмента полипептидной цепи с N-конца (частичный протеолиз). При этом происходит изменение конформации молекулы и формирование активного центра. Пепсин действует при значениях рН 1,5–2,5 и является эндопептидазой с относительной специфичностью действия, расщепляющей пептидные связи внутри белковой молекулы.
Кроме пепсина в желудочном соке содержится фермент гастриксин, проявляющий протеолитическую активность при рН 3,0–4,0. По-видимому, именно он начинает переваривание белков.
В желудочном соке грудных детей содержится фермент реннин, который имеет большое значение для переваривания белков у грудных детей, т.к. катализирует створаживание молока (превращение растворимого казеиногена в нерастворимый казеин), в результате чего замедляется продвижение нерастворимого казеина в двенадцатиперстную кишку и он дольше подвергается действию протеаз.
Образовавшиеся в результате действия пепсина в желудке полипептиды поступают в двенадцатиперстную кишку, куда выделяется сок поджелудочной железы. Панкреатический сок имеет щелочную реакцию (рН 7,5–8,2), что обусловлено высоким содержанием бикарбонатов. Кислое содержимое, поступающее из желудка нейтрализуется, и пепсин теряет свою активность.
В панкреатическом соке содержатся протеолитические ферменты трипсин, химотрипсин, карбоксипептидаза и эластаза, которые вырабатываются также в виде проферментов. Трипсиноген активируется энтерокиназой (вырабатывается клетками слизистой двенадцатиперстной кишки), переходит в активный трипсин, который активирует все остальные ферменты поджелудочного и кишечного сока. Клетки поджелудочной железы защищены от действия протеаз тем, что ферменты желудочного сока образуются в виде неактивных предшественников, а в панкреас синтезируется особый белок-ингибитор трипсина. В полости ЖКТ протеазы не контактируют с белками клеток, поскольку слизистая оболочка покрыта слоем слизи, а каждая клетка содержит на наружной поверхности плазматической мембраны полисахариды, которые не расщепляются протеазами. Разрушение клеточных белков ферментами желудочного или кишечного сока происходит при язвенной болезни.
Переваривание продуктов протеолиза пищевых белков в тонком кишечнике осуществляется с помощью амино-, ди-, и трипептидаз, которые функционируют преимущественно пристеночно.
Таким образом, конечными продуктами переваривания белков в ЖКТ являются свободные аминокислоты, которые всасываются.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава 2. Молекулярная архитектура белков
Глава 2. Молекулярная архитектура белков Не будем скрывать: покончив с первой главой, авторы (а возможно, и читатель) испытали некоторое облегчение. В конце концов цель ее заключалась лишь в том, чтобы дать читателю сведения, необходимые для понимания последующих глав,
Глава 13 Постсовременное состояние эволюционной биологии
Глава 13 Постсовременное состояние эволюционной биологии Пер. А. СамородоваВ предыдущих двенадцати главах мы рассмотрели многообразие аспектов эволюции жизни. Подобное рассмотрение, конечно, никоим образом не может быть всеобъемлющим, но это и не было моей целью. Так или
Глава 496. Почему кодируемых аминокислот двадцать? (XII)
Глава 496. Почему кодируемых аминокислот двадцать? (XII) Неискушенному Читателю может показаться, что элементы машины генетического кодирования описаны в предыдущей главе настолько детально, что к концу чтения он стал даже как-то утомляться, чувствуя, что несколько
Глава 2. Строение и функции белков
Глава 2. Строение и функции белков Белки – высокомолекулярные азотсодержащие органические соединения, состоящие из аминокислот, соединенных в полипептидные цепи с помощью пептидных связей, и имеющие сложную структурную организацию.История изучения белковВ 1728 г.
Глава 25. Метаболизм отдельных аминокислот
Глава 25. Метаболизм отдельных аминокислот Метаболизм метионина Метионин – незаменимая аминокислота. Метильная группа метионина – мобильный одноуглеродный фрагмент, используемый для синтеза ряда соединений. Перенос метильной группы метионина на соответствующий
Роль печени в обмене аминокислот и белков
Роль печени в обмене аминокислот и белков Печень играет центральную роль в обмене белков и других азотсодержащих соединений. Она выполняет следующие функции:1. синтез специфических белков плазмы: - в печени синтезируется: 100 % альбуминов, 75 – 90 % ?-глобулинов, 50 %
Обмен свободных аминокислот в головном мозге
Обмен свободных аминокислот в головном мозге Аминокислоты играют важную роль в метаболизме и функционировании ЦНС. Это объясняется не только исключительной ролью аминокислот как источников синтеза большого числа биологически важных соединений, таких как белки,
Глава 496. Почему кодируемых аминокислот двадцать? (XII)
Глава 496. Почему кодируемых аминокислот двадцать? (XII) Неискушенному Читателю может показаться, что элементы машины генетического кодирования описаны в предыдущей главе настолько детально, что к концу чтения он стал даже как-то утомляться, чувствуя, что несколько
Глава пятая СОСТОЯНИЕ СОБАК ПРИ ДВУХМЕСЯЧНОЙ ФИКСАЦИИ
Глава пятая СОСТОЯНИЕ СОБАК ПРИ ДВУХМЕСЯЧНОЙ ФИКСАЦИИ В начале двухмесячных опытов состояние собак, несмотря на многие индивидуальные отклонения, изменялось по закономерностям, отмеченным при 20-суточных
Глава 5 Современное состояние биосферы Земли
Глава 5 Современное состояние биосферы Земли 5.1. Границы биосферы Биосфера является одним из трех (гидросфера, атмосфера и литосфера) компонентов климатической системы. Ее можно уподобить тонкой пленке, покрывающей поверхность нашей планеты. Плотность органического
Глава 10 Состояние почв и лесов Приморья
Глава 10 Состояние почв и лесов Приморья 10.1. Общая характеристика По данным разнообразных исследований, доминирующими загрязнителями атмосферы являются автомобильный транспорт, предприятия электроэнергетики и многочисленные котельные. Из основных веществ в списке
16. Обмен веществ и превращение энергии. Энергетический обмен
16. Обмен веществ и превращение энергии. Энергетический обмен Вспомните!Что такое метаболизм?Из каких двух взаимосвязанных процессов он состоит?Где в организме человека происходит расщепление большей части органических веществ, поступающих с пищей?Обмен веществ и
Глава 7. Специфическое динамическое действие пищи
Глава 7. Специфическое динамическое действие пищи 7.1. Вводные замечания У большинства организмов можно выделить состояние голода, при котором используются эндогенные пищевые ресурсы (эндотрофия), и состояние сытости после потребления экзогенных пищевых веществ
Глава 7. Специфическое динамическое действие пищи
Глава 7. Специфическое динамическое действие пищи 7.1. Вводные замечания У большинства организмов можно выделить состояние голода, при котором используются эндогенные пищевые ресурсы (эндотрофия), и состояние сытости после потребления экзогенных пищевых веществ
СОСТОЯНИЕ ИММУНОБИОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ ОРГАНИЗМА ЧЕЛОВЕКА ПРИ ПОЛНОМ ДЛИТЕЛЬНОМ ГОЛОДАНИИ Ю. С. НИКОЛАЕВ, В. А. СКОРИК-СКВОРЦОВА (Москва)
СОСТОЯНИЕ ИММУНОБИОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ ОРГАНИЗМА ЧЕЛОВЕКА ПРИ ПОЛНОМ ДЛИТЕЛЬНОМ ГОЛОДАНИИ Ю. С. НИКОЛАЕВ, В. А. СКОРИК-СКВОРЦОВА (Москва) Изучение состояния иммунобиологической реактивности организма в период длительного полного голодания и последующего