Глава 4. Хорошая профессия: конформатор
Глава 4. Хорошая профессия: конформатор
Еще при составлении общего плана книги у авторов возникли разнообразные сомнения по поводу этого заголовка. Перед мысленным взором возникают другие заголовки: «Жаргону — нет!», «О конформаторах, фиттингах и интерфейсах». И горько, горько сознавать авторам статей с такими заголовками, что в то время, как лучшая часть научной общественности самоотверженно борется за очищение научно-технического лексикона от плевелов — англицизмов, латинизмов и т. д., находятся отдельные отщепенцы, которые не только продолжают низкопоклонствовать перед иноязычной терминологией, но и пытаются расширить круг научных понятий за счет сомнительных нововведений, совершенно чуждых нашему великому языку.
Вот такого сорта совместное видение посетило нас в какой-то момент. Стыдливо спрятав глаза, мы принялись было соображать, чем бы заменить термин «конформатор», который, как нам только что казалось, вполне правильно отражает понятие «человек, занимающийся исследованием возможных конформаций молекулы». Не называть же его, в самом деле, начисто скомпрометированным словом «конформист»! Но с другой стороны, ни одна из десятков официальных научных специальностей, перечисленных, например, в длинном списке, опубликованном Высшей аттестационной комиссией, нам не подошла: сказалась извечная проблема «на стыке наук», жалобы на которую мы уже неоднократно приносили читателю. А уж если ВАК не в состоянии помочь… Короче говоря, мы собрали остатки профессионального мужества и очертя голову решили и далее употреблять как в литературной, так и в устной речи слово «конформатор».
В конце концов, любому патриоту своей профессии будет близким и понятным желание конформаторов каким-то образом самоутвердиться, постараться выделить свою специальность среди прочих. В особенности простительно это авторам научно-популярной книги, которые в силу стечения обстоятельств уже довольно давно превратились в профессиональных конформаторов. Что же до всяких там галлицизмов, засоряющих язык, то нам остается уповать на поддержку и солидарность Пушкина, отказавшегося в свое время описать наряд Евгения Онегина, ехидно заявив:
…Но «панталоны», «фрак», «жилет» —
Всех этих слов на русском нет,
А вижу я, винюсь пред вами,
Что уж и так мой бедный слог
Пестреть гораздо б меньше мог
Иноплеменными словами,
Хоть и заглядывал я встарь
В Академический словарь.
Гибкость белковой молекулы
Может показаться, что мы уделяем слишком уж большое внимание вопросам терминологии. В конце концов, не столь важно, как называется та или иная научная специализация и тем более профессия людей, работающих в этой области. Важно другое: в чем состоит их деятельность и какие результаты получены к настоящему времени?
Мы подошли к рассказу о том, как решается задача теоретического отыскания пространственной структуры белков и пептидов. Именно решается, то есть находится в стадии решения. Давайте наконец взглянем, что же удается рассчитать бравым конформаторам?
Формулировка, заметьте, несколько настораживающая. Как видно, не столь уж хорошо обстоят дела, если приходится рассчитывать то, что удается, вместо того, что хотелось бы. Как еще говорят, ищем не там, где потеряли, а там, где светло.
Ну что ж, есть, по-видимому, доля справедливости и в таком предположении. Действительно, хотелось бы конформаторам решать задачи гораздо большего масштаба, представляющие непосредственный интерес для выяснения животрепещущих молекулярно-биологических проблем, но это им пока не по зубам. Однако, подчеркнем еще раз, именно пока. Поскольку в будущем, мы твердо надеемся, эти задачи разрешить все же удастся. А путь в это (по-видимому, все же не очень отдаленное) будущее, путь к чтению третичной, пространственной структуры белковой молекулы по ее аминокислотной последовательности приходится нащупывать сейчас на самых разнообразных направлениях, рассматривая множество мелких, частных задач, решение которых несет нам — и то далеко не всегда — только очень малую крупицу полезных сведений о способе и механизмах, лежащих в основе самопроизвольной пространственной укладки молекул белков.
Продвижение вперед идет очень маленькими, очень неуверенными шажками, временами возникающие неумеренные надежды сменяются горькими разочарованиями. Порой конструктивный, «рабочий» пессимизм перерастает в отчаяние: нет-нет кто-нибудь из конформаторов выскажется в том смысле, что взялись мы-де за принципиально неразрешимую задачу, что все это слишком сложно и для наших маломощных вычислительных машин, и для наших примитивных умов…
Позвольте, последнее ведь где-то уже было. Ну конечно, Г. Уэллс, «Машина времени». Путешественник во времени рассказывает о том, как его машина, позволяющая перемещаться в прошлое и будущее, попала в руки морлоков — отдаленных обезьяноподобных потомков человека, обитающих под землей. «Морлоки даже разбирали машину по частям, стараясь своим слабым разумом понять ее назначение».
Пытаясь своим слабым разумом понять назначение… Нет, нет, это только минутная депрессия. Как ни скромны итоги каждой очередной попытки, они все же хоть немножко прибавляют уверенности в конечном успехе, становятся еще одним кирпичиком, использованным при возведении здания теории третичной структуры. Общие контуры этого здания еще совершенно неясны, но о некоторых деталях можно кое-что уже сказать.
Начнем с самой элементарной проблемы: гибкости белковой цепи. Можно предположить, что в зависимости от того, какие именно аминокислотные остатки входят в те или иные ее участки, должна различаться также и гибкость этих участков. В принципе гибкость белковой молекулы обусловлена возможностью вращения отдельных ее частей вокруг некоторых валентных связей.
При таком вращении происходит взаимное сближение или удаление каких-то атомов, что и определяет их притяжение или отталкивание в зависимости от разделяющего их расстояния, сорта атомов, наличия электрического заряда, — словом, смотри предыдущую главу. В силу межатомного взаимодействия, и прежде всего именно в силу атом-атомного отталкивания, вращение вокруг отдельных связей оказывается более или менее «заторможенным»: существуют такие положения, при которых энергия отталкивания очень велика.

Поскольку же ближайшее атомное окружение связей, вокруг которых возможно вращение, может быть разным у различных аминокислотных остатков, естественно, неодинаковой оказывается также и степень «заторможенности».
Внутримолекулярные ситуации, при которых межатомное отталкивание велико, не могут реализоваться в действительности (почему именно, мы уже говорили) и называются стерически запрещенными. Это означает, что в результате вращения вокруг определенной связи две разделяемые ею части молекулы могут принимать друг относительно друга не все возможные положения, допускаемые таким вращением, а лишь некоторые из них, так называемые «стерически разрешенные». И конечно, можно ожидать, что наборы стерически разрешенных положений будут различаться от остатка к остатку.
Если рассмотреть элементарное звено белковой цепи, соответствующее некоторому аминокислотному остатку (так называемую дипептидную единицу), окажется, что вращения в главной цепи возможны вокруг двух связей:
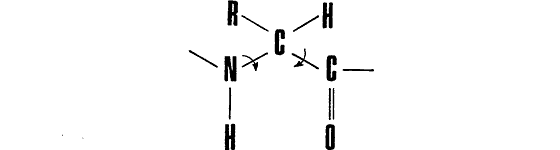
(Буквой R здесь обозначена боковая цепь аминокислотного остатка.)
Сразу же можно указать на исключение из этого правила — остаток пролина:
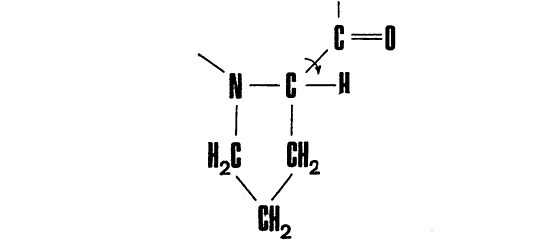
в котором вращение вокруг связи N ? С невозможно: определенный угол поворота зафиксирован жестким кольцом. В месте включения этого остатка белковая цепь оказывается, таким образом, более жесткой.
Напротив, у остатка глицина доля стерически разрешенных конформаций высока, поскольку роль бокового радикала выполняет «маленький» атом водорода. И если пролин — наименее гибкий остаток, то глицин — наиболее гибкий из всех двадцати.
Все это, повторяем, можно сообразить сразу, безо всяких расчетов, лишь взглянув на химические формулы. А вот точное определение степени и, главное, характера гибкости каждого остатка, его возможности принимать определенные конформации, — это уже требует расчета. И именно описание «конформационной гибкости» отдельных остатков оказалось первой задачей теоретического конформационного анализа белков, задачей, которая была разрешена без особого труда, хоть и не обошлось в среде конформаторов без споров о том, какой из остатков более, а какой менее гибкий. Споры эти, между прочим, как две капли воды напоминали перебранку, подслушанную двумя героями И. Ильфа и Е. Петрова в месткоме некоего учреждения:
«— …Лыжная вылазка проведена недостаточно. А почему, товарищи? Потому что Зоя Идоловна проявила недостаточную гибкость.
— Как? Это я недостаточно гибкая? — завопила ужаленная в самое сердце Зоя.
— Да, вы недостаточно гибкая, товарищ!
— Почему же я, товарищ, недостаточно гибкая?
— А потому, что вы, товарищ, совершенно негибкая.
— Извините, я чересчур, товарищ, гибкая.
— Откуда же вы можете быть гибкая, товарищ?»
И еще мною часов спустя из дальней комнаты слышались голоса:
— Я, товарищ, чересчур гибкая!
— Какая же вы гибкая, товарищ?
До такого накала страстей среди конформаторов, правда, не доходило, но смысл некоторых дискуссий о расчетных оценках конформационной подвижности различных аминокислотных остатков, вне всякого сомнения, можно было бы передать примерно теми же выражениями:
— А я вам говорю, товарищ, что дипептидная единица аспарагина более гибкая, чем аланина!
— Откуда же она может быть гибкая, когда она совершенно негибкая, товарищ?
(Не следует считать пространное отступление исключительно порождением желчного нрава авторов: напротив, оно скорее относится к разряду лирических воспоминаний. Ведь конформационные расчеты дипептидных единиц и споры на эту тему отшумели, по меркам современной молекулярной биологии, очень давно, лет пять тому назад, и, стало быть, представляют собой незабвенное босоногое детство теоретического конформационного анализа пептидов и белков. А об этой идиллической поре, когда казалось, что значительная часть проблемы поиска третичной структуры белка сводится к расчету стабильных структур дипептидных единиц аминокислотных остатков, авторам всегда приятно вспомнить. Тем более что и сейчас нет-нет, да и появится в каком-нибудь научном журнале статья, рассказывающая об очередном варианте расчета какой-либо дипептидной единицы. Непосредственность и эмоциональность, сопровождающие зачастую подобные статьи, близки и понятны чутким сердцам авторов: никому, и даже самым суровым из конформаторов, не хочется расставаться с детством.)
Конформационные расчеты дипептидных единиц — первые робкие попытки подступиться к третичной структуре — принесли все же значительную пользу. На их основе удалось классифицировать основные типы поворотов, изгибов остова белковой цепи в месте включения отдельных аминокислотных остатков. Группа итальянских исследователей даже поспешила назвать такого рода классификацию стереохимическим кодом третичной структуры белка. Что же, стремление придумать еще один молекулярно-биологический код (именно код, это так хорошо звучит!) можно было бы только приветствовать, но использование именно этого термина в данной ситуации неуместно. Под кодированием, как мы помним, обычно понимают способ преобразования определенной информации, а здесь ни о чем подобном речи нет. Правильнее говорить о стереохимическом или конформационном алфавите, на котором может быть записана третичная структура, да и то с известной осторожностью: расчеты дипептидных единиц показывают, что такой алфавит описывает структуру лишь приближенно, с точностью до какого-то интервала «разрешенных» межатомными взаимодействиями значений углов внутреннего вращения.
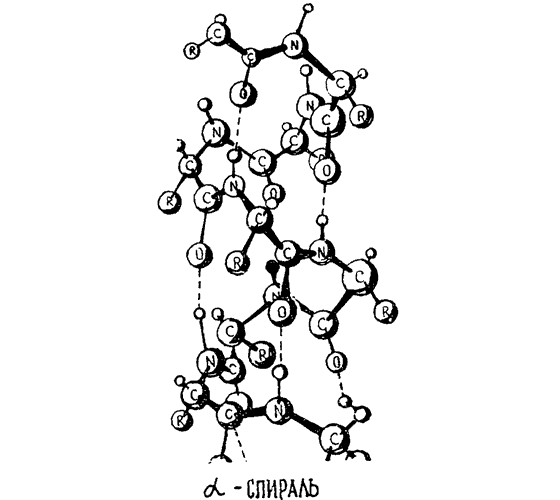
Для большинства остатков характерны два основных типа изгиба остова белковой цепи, или, точнее говоря, два типа сравнительно стабильных конформаций.
Третий основной тип конформаций остова менее стабилен — по данным расчета, ему соответствуют довольно высокие значения энергии. Ну и, разумеется, есть исключения из общего правила «трех конформаций»: остаток глицина, конформационная подвижность которого, как уже говорилось, намного больше, чем у прочих остатков, и пролин, для которого возможны лишь два основных типа конформаций.
Если в полипептидной цепи какой-нибудь из этих типов конформаций повторяется у всех остатков подряд, получаются периодические структуры, найденные Л. Полингом, — о них уже неоднократно вспоминалось в предыдущих главах. Два самых стабильных типа конформаций соответствуют вытянутой слоисто-складчатой структуре (?-структуре) и правозакрученной ?-спирали; третья, менее стабильная, конформация порождает левозакрученную ?-спираль. И действительно, как показывает эксперимент, цепочки полипептидов гораздо охотнее сворачиваются в виде именно правой ?-спирали. Причем в правую форму сворачиваются полипептиды, образованные остатками L-аминокислот; если же для их построения использованы D-аминокислоты, более стабильной становится левая ?-спираль. И это обстоятельство также подтверждено расчетом.
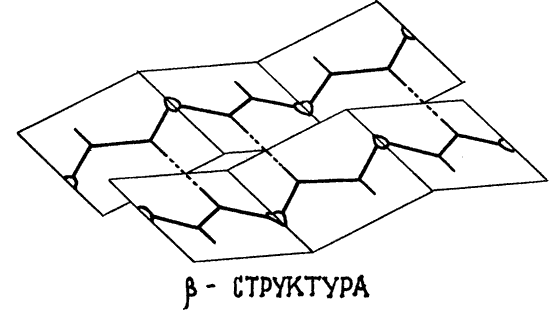
(Между прочим, уже на основании этих результатов можно было бы высказать кое-какие соображения по поводу асимметрии аминокислот, образующих белки; мы, однако, отложим этот вопрос до следующей главы, а сейчас продолжим разговор о расчете пространственной структуры белков.)
Итак, расчет позволил классифицировать возможные способы изгиба остова полипептидной цепи, характерные для отдельных аминокислотных остатков. Помимо этого, оказалась возможной такая же точно классификация конформаций боковых радикалов всех остатков — разработка конформационного алфавита третичных структур белков была тем самым полностью завершена. «Победа!» — следовало бы воскликнуть конформаторам, но, повторяем, иллюзиям детства суждено было рассеяться очень скоро.
Подсчитали — прослезились
Горестный перечень разочарований, постигших конформаторов на этапе, завершившемся созданием конформационного алфавита, начнем с замечания о том, что этот алфавит оказался довольно громоздким: по объему символов он скорее напоминает китайскую азбуку, чем какую-либо из европейских. В самом деле, рассмотрим внимательно остаток аминокислоты аргинина:
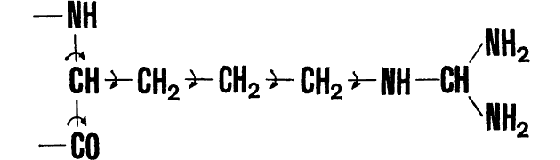
Как мы уже писали, возможны три типа стабильных конформаций пары углов внутреннего вращения в основной полипептидной цепи; кроме того, каждый из углов внутреннего вращения в боковой цепи (а их всего четыре — напоминаем, что вращение возможно вокруг каждой одинарной связи) может в любой из этих ситуаций принимать одно из трех «разрешенных» значений. А это значит, что всего остаток аргинина может иметь 3·3·3·3·3 = 243 сравнительно устойчивых конформации!
Правда, для других аминокислот (за исключением лизина) это число заметно поменьше, но все же общее количество подлежащих рассмотрению типов конформаций всех остатков приближается к тысяче.
Допустим, однако, что число возможных конформаций каждого остатка в среднем всего десять. Каков же окажется объем вычислений, соответствующих задаче расчета структуры белковой молекулы — пусть даже не очень большой, всего-то из ста аминокислотных остатков?
Вспомним, что наша задача будет состоять в том, чтобы из всех возможных конформаций молекулы выбрать ту, которой соответствует наименьшая энергия внутримолекулярных взаимодействий, и что сосчитать эту энергию на основе попарно-аддитивного приближения в принципе не очень сложно. Дело только за тем, чтобы прилежно перебрать все конформации молекулы, представляющие собой все возможные сочетания конформаций образующих ее остатков, каждый раз вычисляя величину соответствующей энергии внутримолекулярных взаимодействий, и по завершении этой нехитрой работы мы будем точно знать наиболее стабильную конформацию.
Ну что ж, в прилежании биологам как будто нельзя отказать, можно бы, кажется, и приняться за дело. Каждый остаток, значит, может принимать одно из десяти состояний, а всего остатков — сто. Если состояния отдельных остатков пронумеровать цифрами от 0 до 9, каждая конформация всей молекулы может быть условно обозначена каким-то стозначным числом:
937052… 362.
Предположим теперь, что вычисление энергии внутримолекулярных взаимодействий в каждой конформации занимает одну секунду. Это, конечно, чудовищный обман — с учетом всех обстоятельств такой расчет должен длиться часами или даже сутками на самой современной машине. Но не будем тем не менее мелочными, итак, одна секунда. Следовательно, для перебора всех возможных конформаций стоостаточной белковой молекулы нам понадобится 10?10?10… ?10 = 10100 секунд.
Если бы авторы были драматургами и писали пьесу из жизни конформаторов (в отличие от популярных ныне драм и комедий из жизни студентов, сталеваров и строителей такая пьеса, несомненно, была бы трагедией), последнее утверждение предшествовало бы авторской ремарке «немая сцена». В самом деле, мы опять упираемся в астрономические цифры, которым невозможно даже подобрать наглядного сравнения. Право же, временами кажется, что определение «астрономические» не имеет никакого отношения к очень большим цифрам и что с гораздо большим основанием их следовало бы называть «молекулярно-биологическими». Ведь цифры типа 10100 и т. п., то и дело фигурирующие даже в нашем сравнительно лаконичном повествовании, в обычной записи не уместились бы в одну, а то и в две, и в три строки!
Ибо что в действительности представляет собой промежуток времени в 10100 секунд, необходимый, как мы только что выяснили, для расчета третичной структуры молекулы белка? Трудно даже ответить, что он собой представляет в сравнении, скажем, с сутками, в которых всего-то около 81 тысячи секунд (попробуйте как-нибудь сосчитать до 81 тысячи — сами убедитесь). Пусть даже для простоты счета не 81, а 100 тысяч — то есть 105. Тысяча суток — это примерно три года, 108 секунд, триста лет; тем самым это всего лишь 1010 секунд — величина, которую по-прежнему невозможно сколько-нибудь наглядным образом сопоставить с интересующими нас 10100… (Правда, вот пример из «Занимательной алгебры» Я. Перельмана: невероятно огромное число пшеничных зерен, которое попросил в награду легендарный изобретатель шахмат, составляет 264 — 1, то есть около 1019. Возведя это число в пятую степень, мы приблизимся к 10100, но опять-таки только в чисто математическом смысле: понимание истинных масштабов такой величины по-прежнему лежит за границами постижимого.)
Выходит, повторяется прежняя ситуация: схема расчета третичной структуры формулируется вполне ясно, но ничуть не менее ясно и то, что реализовать эту схему практически совершенно немыслимо. И опять перед молекулярными биологами (точнее, перед той их частью, которую мы уже привыкли именовать конформаторами) возникает вопрос: что же делать? Неужели и попарно-аддитивному расчету окончательно недоступны интересующие их задачи?
Профессиональная амбиция толкает нас на запальчивое восклицание:
— Конечно, доступны!
Но — что поделать! — единственным абсолютно убедительным аргументом, подтверждающим такое мнение, может явиться успешный расчет третичной структуры молекулы какого-нибудь белка. До сих пор этого не удалось сделать никому. И все же смеем утверждать: дело к этому идет.
Уже рассчитаны структуры нескольких биологических пептидов — этаких сверхминиатюрных белочков, по «белковым» меркам просто обрывков: 3, 8, 9, 10 остатков… Но ведь это уже молекулы, содержащие до полутора сотен атомов! Расчет каждого такого соединения был очень труден, временами, казалось, выполнялся на пределе возможностей теоретического конформационного анализа, но, самое главное, давал верные результаты, соответствующие имеющейся экспериментальной информации о пространственной структуре молекулы. Даже в этих сравнительно простых случаях решить задачу простым перебором всех мыслимых конформаций оказалось невозможным — слишком уж велико их число. Зато удалось установить некоторые способы исключения из рассмотрения части структур, в отношении которых можно с уверенностью утверждать, что они не могут войти в число наиболее стабильных.
Словом, как пишут журналисты, специализирующиеся на производственной тематике, накоплен большой положительный опыт, и можно надеяться, что рано или поздно конформаторы разрешат проблему «молекулярно-биологических» чисел. В конце концов, удается же карточному шулеру средней руки составить нужную ему в данный момент игры комбинацию из 52 карт колоды, а ведь для полного перебора всех возможных комбинаций из 52 карт требуется не менее 1068 операций (по оценке У. Эшби, виднейшего английского кибернетика, который в соответствии со своими профессиональными склонностями называет числа такого порядка комбинаторными). Конечно, конформаторам, за плечами которых всего несколько лет исследований, далеко до шулеров, опирающихся на многовековой опыт своей почтенной специальности, но ведь лиха беда начало…
Срочно требуются квалифицированные ясновидцы
Что ж, подумает иной читатель, конформатор — профессия, может быть, и впрямь хорошая, да уж больно хлопотная. Шарахнулся из огня квантовой механики — попал в полымя другой, тоже малообнадеживающей задачи. И вообще в разговорах на эти темы слова «расчет», «задача» постепенно становятся доминирующими, и все реже вспоминается конечная цель, ради которой весь этот расчет затеян. А ведь интересуют-то нас проблемы не вычислительные, а молекулярно-биологические.
Увы, эти упреки не лишены оснований. Действительно, чем дальше мы говорим о попытках расчетных подходов к определению третичной структуры белка, тем больше приходится упоминать о делах чисто вычислительных, то есть отвлекаться проблемами, не относящимися к существу дела. Наверное, и в самом деле будет уместным ограничиться тем, что мы уже рассказали, ибо смысл, основа подхода уже ясны, а решающие успехи, как ни больно в этом признаваться, еще не достигнуты. Многое сделано на этом пути, многое делается именно сейчас, и у нас, конформаторов, как будто нет оснований сомневаться, что расчет третичной структуры белка рано или поздно осуществить все же удастся.
И тем не менее наше повествование о конформаторах и их усилиях на поприще поисков третичной структуры еще далеко не закончено. Конечно, сравнительно корректному физическому расчету в попарно-аддитивном приближении, не говоря уже о квантовохимических расчетах, такая задача пока недоступна. Но это еще вовсе не повод для того, чтобы сидеть сложа руки у безбрежного моря конформаций (напоминаем: 10100) и ждать подходящей вычислительной погоды. Возможно, имеет смысл попытаться нащупать пути разрешения проблемы с помощью более грубых или эмпирических приемов.
Например, совсем недавно прогнозы погоды, выдаваемые профессионалами-метеорологами на вполне научной основе, доставляли гораздо больше удовольствия любителям непритязательных острот, чем людям, которых действительно интересовало, какая же погода будет завтра. Метеорологи ссылались на те же трудности, что ныне конформаторы: в принципе они могут составить уравнения, описывающие развитие атмосферных процессов с очень большой точностью, и даже на срок, значительно превышающий сутки, но какой от этого прок, если их решение требует такого объема вычислений, что точное предсказание погоды на завтра будет получено через недели, месяцы или даже годы!
В самое последнее время положение метеорологов резко улучшилось благодаря широкому применению ЭВМ, хотя любители позлословить насчет эффективности радио- или телепрогнозов погоды все еще не испытывают недостатка в удобных поводах. Продолжая начатое сравнение, мы будем, однако, иметь в виду не современную метеорологию, а метеослужбу, скажем, начала века и вообще прошлых лет, когда ни о каком использовании ЭВМ не было и помина, а досадные ошибки в прогнозах случались намного чаще.

Люди, интересующиеся прогнозами погоды вовсе не по причине праздного любопытства, — моряки, земледельцы, путейцы, — конечно же, нередко страдали от таких ошибок; поэтому даже самые просвещенные из них, не чуждые метеорологической науке, тем не менее охотно пользовались советами бывалых людей, «методы» которых на первый взгляд могут вызвать лишь улыбку; «грач в феврале прилетел — будет дружная весна», «ласточки низко летают — к дождю», «красный закат — значит, похолодает» и т. п. И это еще, можно сказать, точно формулируемые признаки сравнительно с такими, как «поясницу ломит — быть грозе», или просто «чую, сынок, чую»…
Конечно, собрание всяческих подобных этим примет не заменяло научной метеорологии, но как часто они оказывались полезными в тех случаях, когда метеорология была беспомощна!
Точно так же и молекулярные биологи, с надеждой и сочувствием следившие за усилиями конформаторов, пытавшихся нащупать подходы к расчету третичной структуры белка в попарно-аддитивном приближении, начали убеждаться, что ждать придется еще долго.
В то же время для очень многих целей часто нужно было иметь хоть какое-нибудь представление о третичной структуре белков, для которых известна только аминокислотная последовательность. Пусть даже это будет описание очень приближенное, указывающее лишь на какие-то основные элементы пространственной организации глобулы. Пусть методы, используемые для такого предсказания, окажутся эмпирическими, не вполне надежными. Но если они хоть как-то будут «работать», позволяя хотя бы в самом первом приближении читать аминокислотную последовательность на языке пространственной структуры молекулы, — это все же намного лучше, чем ничего!
Вот одна из простейших, казалось бы, проблем: как на основании первичной структуры белковой молекулы ответить на вопрос о том, имеет ли ее глобула (этот термин также используют, говоря о пространственной структуре) округлую форму, близкую к сферической, или несколько вытянутую, скажем, сигарообразную? Оказалось, что приближенный ответ на этот вопрос возможен на основании очень простых рассуждений, которые мы сейчас воспроизведем, пояснив лишь предварительно необходимый для этого новый термин: прилагательное «гидрофобный». С этим понятием связаны некоторые физико-химические эффекты, весьма важные для формирования и существования белковой глобулы.
Части читателей, возможно, появление этого термина в таком контексте покажется странным: как известно, гидрофобия, или водобоязнь, — научное медицинское название бешенства, и словосочетание «гидрофобные взаимодействия», которое появится чуть ниже, вызывает необычные ассоциации.
Но речь пойдет о водобоязни совсем иного рода: о хорошо знакомом каждому из нас «нежелании» жирных веществ смачиваться водой. Физическая природа этого явления вкратце такова. На поверхности контакта воды с жиром в прилегающем водном слое образуется упорядоченная, так называемая «льдоподобная» структура. Известно, что образование льда — процесс, требующий затраты энергии; с другой же стороны, как мы помним, всякая система стремится занять положение, которому соответствует наименьшая энергия. В рассматриваемом случае это означает стремление всемерно ограничить поверхность контакта воды с жирным или — давайте начнем пользоваться введенным термином — гидрофобным веществом.
Капля воды, нанесенная на пластинку парафина, не растекается по ней, а съеживается в округлую чечевичку, и, наоборот, капля жира в тарелке супа стремится принять ту же чечевицеобразную форму, чтобы вода и жир соприкасались поменьше. Можно, конечно, спросить, почему та же водная капля на пластинке парафина не соберется в шарик, тогда она почти совсем не будет соприкасаться с парафином. Вспомним, однако, что для этого ей придется приподнять свой центр тяжести, а это тоже затрата энергии, уже не компенсируемая тем выигрышем, который получается за счет дальнейшего ограничения площади соприкосновения.
Итак, гидрофобность многих веществ — парафина, масел, бензина, полиэтилена — явление, хорошо известное нам из повседневного опыта; к сказанному можно было бы еще добавить, что гидрофобные вещества совершенно нерастворимы в воде, что естественным образом следует из приведенных рассуждений и столь же хорошо подтверждается известными всем примерами.
Какова же химическая природа гидрофобных веществ? Из интересующих нас классов соединений важнейшими являются два: вещества, содержащие длинные фрагменты типа… ?СН2?СН2?СН2? … то есть так называемую алифатическую часть (напомним, что парафины имеют общую формулу СН3(СН2)n СН3), и циклические ароматические соединения, содержащие кольца типа
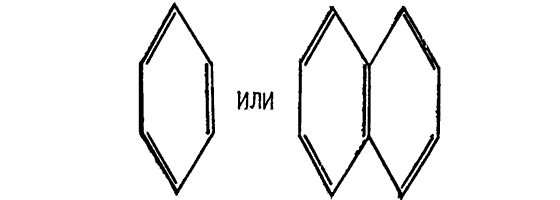
(попробуйте растворить в воде нафталин!).
Именно такие элементы структуры содержатся в боковых радикалах некоторых аминокислотных остатков: валина, лейцина, изолейцина, пролина (алифатические цепи), фенилаланина, триптофана (ароматические циклы). Соприкосновение этих боковых групп с водой энергетически «невыгодно», поэтому вполне вероятно предположить, что в белковой глобуле они будут стремиться разместиться внутри глобулы, а наружу будут выставлены хорошо гидратируемые (как бы смачиваемые водой) радикалы. Например, боковой радикал серина представляет собой остаток метилового спирта, боковой радикал аспарагиновой кислоты — остаток уксусной кислоты; оба вещества, как все знают, прекрасно растворяются в воде. Большой гидрофильностью (этот термин, что совершенно очевидно, означает свойство, противоположное гидрофобности) отличаются также остатки аргинина, глутаминовой кислоты, треонина.
Итак, по соображениям стабильности глобулярной структуры гидрофобные остатки должны локализоваться внутри, образуя как бы жирную каплю, защищенную от доступа воды наружным слоем гидрофильных остатков. Такое расположение остатков следует, впрочем, уже из самого факта растворимости белков в воде: будь неполярные остатки снаружи, белки бы в воде не растворялись. Впервые гипотеза о существовании подобного «гидрофобного ядра» глобулы была высказана советскими учеными С. Бреслером и Л. Талмудом еще в 1949 году, когда о пространственном строении белковых молекул не было известно почти ничего. Впоследствии именно такой способ размещения боковых цепей различной природы в глобулах ряда белков был подтвержден рентгеноструктурным анализом, а стремление гидрофобных остатков собраться вместе даже породило не вполне удачный термин «гидрофобные взаимодействия», прочно вошедший в словарь молекулярной биологии.
Одно из следствий описанного строения белковой глобулы можно наблюдать довольно часто — всякий раз, когда вы готовите яичницу. При высокой температуре третичная структура белков разрушается вследствие теплового движения, и гидрофобные радикалы, ранее скрытые от воды гидрофильной «рубашкой», оказываются в контакте с водой. Молекулы белка теряют растворимость, и совершенно прозрачный и вязкий яичный белок (опять эта игра слов!) становится плотной непрозрачной массой. (Вспомним, что прозрачность — неотъемлемое свойство всякого истинного раствора.)
Закончив это кулинарное отступление — почти совершенно, впрочем, неизбежное в любом не слишком лаконичном рассказе о строении белков, — вернемся к вопросу, с которого мы начали: можно ли по аминокислотной последовательности белка предсказать, будет ли его глобула близка по форме сфере или какой-нибудь вытянутой фигуре?
Оказывается, с учетом всего, что мы уже знаем о характере размещения гидрофобных и гидрофильных остатков в глобуле, на этот вопрос можно ответить. Впервые такая возможность была указана американским биофизиком Г. Фишером (по слухам, исходящим из непроверенных молекулярно-биологических источников, отцом экс-чемпиона мира по шахматам). Симпатичная наука стереометрия, которая для многих (в том числе и для авторов) служила причиной некоторых затруднений при обучении в средней школе, утверждает, например, что поверхность шара меньше поверхности сигарообразного тела того же объема. С другой стороны, поскольку на поверхности белковой глобулы расположены гидрофильные остатки, а внутри — гидрофобные, это означает, что уже простое сопоставление числа тех и других может служить мерой уклонения формы глобулы от сферической, а с помощью несложных расчетов, доступных тем немногим, кто не окончательно забыл школьный курс геометрии, можно оценить степень вытянутости глобулы.
Кстати, для этого даже не нужно знать текст аминокислотной последовательности белковой цепи — достаточно общего аминокислотного состава молекулы. (Здесь наступило время покаяться в допущенной неточности! Ведь ранее мы утверждали, что третичная структура глобулы определяется системой внутримолекулярных взаимодействий, совершенно игнорируя влияние растворителя — воды. Не вдаваясь в подробности, скажем лишь, что изощренные конформаторы-расчетчики умеют учитывать и взаимодействие молекулы белка с водой.)
Конечно, представление о глобуле как о правильном геометрическом теле очень приблизительно: поверхность глобулы может быть изрезана различными неровностями, иметь изогнутую форму, короче — напоминать произведение лауреата выставки абстрактной скульптуры. (Непонятно, кстати, почему изображения структур белковых молекул — того же миоглобина или лизоцима — до сих пор не послужили ни одному скульптору-абстракционисту в качестве «натуры».) И уж, разумеется, оценки с помощью гипотезы «гидрофобного ядра» никаких подробностей структуры не сообщают. Но, повторяем, на конформационном безрыбье…
Словом, если завтра в какой-нибудь газете появится объявление «Срочно требуются квалифицированные ясновидцы», можно не сомневаться, что наряду с тысячами возмущенных столь откровенным розыгрышем читателей найдутся немногие, которые на всякий случай все же позвонят по телефону, указанному в объявлении, и поинтересуются, удалось ли отделу кадров найти хоть одного стоящего ясновидца. Кстати, если удалось, нельзя ли ему поработать по совместительству еще в одном учреждении. А в ответ на резонный вопрос начальника отдела кадров, кого же, собственно, представляет невидимый собеседник, почти наверняка раздастся уклончивое: «Вообще-то нас интересует пространственная структура белков…»
Спорт находчивых и мужественных
Как мы только что убедились, очень грубое предсказание общих очертаний белковой глобулы — дело сравнительно нетрудное. Однако многовековая история колдовства, ведовства и черной магии учит, что запросы потребителей на рынке предсказаний непрерывно растут: если рядовому авгуру в Древнем Риме приходилось, самое большее, отвечать, будут ли всемогущие боги благосклонны к участникам завтрашней битвы, то главе современных гадалок мадам Солей (Франция) доводится, по слухам, консультировать новоиспеченных премьер-министров относительно предполагаемого персонального состава будущего кабинета. Недаром мадам Солей вынуждена (по тем же слухам) прибегать к активной помощи компьютеров!

Поведение молекулярных биологов в этом смысле ничуть не отличается от поведения прочих потребителей предсказаний. Ученые хотят знать не просто форму глобулы, но и, например, схему размещения в белковой цепи участков периодических структур: ?-спирали и ?-структуры. Конечно, прорицателю, работающему по старинке, такая задача не под силу; современные же предсказатели, вооруженные до зубов всевозможными математическими премудростями, добились в ее решении значительных успехов, о которых стоит поговорить подробнее.
Самые распространенные приемы предсказаний локализации регулярных структурных участков в аминокислотной последовательности базируются на тщательном изучении третичных структур белков, исследованных рентгенографически. Уже простой подсчет остатков различных типов, входящих в ?-спиральные участки, участки ?-структуры и нерегулярные части молекулы, показывает, что существуют, например, остатки, заметно чаще встречающиеся именно в спиральных фрагментах — аланин, валин, фенилаланин, лизин и т. д. Если в какой-то части аминокислотной последовательности белка встречается скопление этих остатков, можно предположить, что в глобуле эта часть спирализована.
Приведенный тип обобщения — наиболее примитивный; на самом деле обработка информации об аминокислотных последовательностях, принадлежащих участкам различных типов вторичных структур, велась с использованием весьма совершенных методов математической статистики, начиная с установления зависимостей, подобных рассмотренным, для различных комбинаций пар, троек и т. д. остатков и кончая весьма сложными процедурами, базирующимися на так называемой теории распознавания образов. Очевидно, однако, что при всей математичности такой подход является чисто эмпирическим и по существу своему очень близок упоминавшимся народным приметам (разумеется, это говорится отнюдь не в укор, тем более что на этом пути были получены очень хорошие результаты).
Тенденция того или иного остатка к образованию спирали может быть получена и из другого источника: экспериментального исследования синтетических полипептидов, образованных из аминокислот лишь одного определенного типа — полиаланина, полизина и т. п. Хорошо известно, что часть полиаминокислот приобретает в растворе форму ?-спирали, другие же не обнаруживают склонности к ее образованию. К первым относятся, например, полиаланин, полифенилаланин, полилейцин, ко вторым — полисерин, политреонин. Информация, полученная таким путем, может использоваться для разработки самостоятельных методов распознавания спиральных участков белковых структур или в качестве дополняющей в только что рассмотренных методах.
Наконец, ряд «предсказательных» подходов использует то обстоятельство, что атомы внутри белковой глобулы расположены достаточно плотно, так что внутри не остается никакого свободного пространства, и в то же время без напряжений, без «налезания» одного атома на другой.
Зная строение остова ?-спирали, можно, опираясь на эти представления (иногда дополняемые требованием определенного чередования гидрофобных и гидрофильных остатков), указать те участки аминокислотной последовательности, которые могут принять форму ?-спиралей, причем боковые радикалы на их поверхности будут расположены плотно и без напряжений. Оценки такого рода выполняются обычно с помощью объемных молекулярных моделей, в которых атомы представлены шариками того или иного, своего для каждого атома, диаметра.
Отметим, наконец, что в практике предсказаний спиральных участков (и вообще участков структуры определенного типа) очень часто описанные подходы используются не в «чистом», а в комбинированном виде.
Мы столь подробно останавливаемся на этих методах по двум причинам. Во-первых, многие из них оказались довольно эффективными; во-вторых, предсказание локализации вторичных структур в белках с известной аминокислотной последовательностью ныне стало излюбленным занятием очень многих специалистов в области структуры белка. Число предложенных методов перевалило за тридцать, а в обсуждении тех или иных преимуществ каждого из них стали появляться нотки соперничества. Так что вполне естественной оказалась мысль проведения мирового чемпионата по предсказанию участков регулярной структуры: пусть преимущество того или иного метода решается не в бесплодной полемике авторов на страницах специальных журналов, а в честной спортивной борьбе! Правда, соревнования по таким предсказаниям еще никто никогда не проводил, но ведь и бобслей, к примеру, появился совсем недавно, а нынче этот вид спорта уже прочно входит в программу Олимпийских игр.
Инициатором соревнований оказался западногерманский кристаллограф Г. Шульц из Планковского института медицинских исследований в Гейдельберге. Им была установлена пространственная структура молекулы фермента аденилкиназы; перед тем как ее обнародовать, Г. Шульц разослал всем предсказателям регулярных структур предложение участвовать в организуемом им конкурсе на лучшее распознавание (на основании первичной аминокислотной последовательности) участков ?-спирали, ?-структуры и резких изгибов белковой цепи молекулы аденилкиназы. Сам он, естественно, фигурировал в роли арбитра.
На старт вышли одиннадцать участников. Говоря о числе участников, мы имеем в виду количество методов предсказаний, а не предсказателей, поскольку многие методы предлагались двумя авторами или наоборот: одни и те же авторы представили по нескольку методов.
Участники (на этот раз имеются в виду авторы методов) должны были определить положения ?-спиралей, участков ?-структуры и изгибов цепи и результаты выслать Г. Шульцу.
И вот наступил день подведения итогов (впоследствии они были опубликованы в известном английском научном журнале «Нейчур»). О, как нам хотелось бы в совершенстве владеть роскошным праздничным жаргоном спортивных комментаторов, пишущих об очередной блестящей победе советских фигуристов! Но нет, конечно же, это было бы неуместным, тем более что никакого публичного провозглашения имен победителей не последовало, а выявление их оказывается возможным лишь на основе неофициального подсчета очков.
Вот, например, результаты по классу ?-спирали. Аденилкиназа — белок с относительно высоким содержанием спиральных участков: из 193 аминокислотных остатков, образующих молекулу, 105 входят в спиральные участки. Советские ученые О. Птицын и А. Финкельштейн сумели правильно указать 79 из них (не обнаружив, следовательно, 26); кроме того, 12 неспиральных остатков ими были ошибочно определены как спиральные. Другой советский участник, В. Лим, достиг еще большего числа правильных предсказаний — 82, однако ценой также и большего количества ошибок — 29. Лучшие среди зарубежных участников, американцы П. Чоу и Дж. Фасман, имеют результат 70 и 14 соответственно.
Если победителей определять на основании общего числа ошибок («недопредсказанных» и «перепредсказанных» остатков), то места в классе ?-спирали распределятся следующим образом: О. Птицын и А. Финкельштейн — 38, П. Чоу и Дж. Фасман — 49, В. Лим — 52. Заметим, что некоторые методы дали 78, 87 и даже 98 ошибок! Для сравнения интересно указать, что утверждению о полной спирализации молекулы аденилкиназы соответствовало бы 88 ошибкам, а метод, заключающийся в определении «спиральности» или «неспиральности» каждого остатка с помощью бросания монетки (орел — решка), в среднем привел бы к 96,5 ошибки.
В классе предсказания ?-структур среди лидеров встречаем те же фамилии: О. Птицын и А. Финкельштейн — 16 ошибок, В. Лим — тоже 16, П. Чоу и Дж. Фасман — 33 ошибки. Изгибы пептидной цепи наиболее удачно угадали американцы А. Бэрджесс и Г. Шерага (27 ошибок), незначительно опередившие тех же П. Чоу и Дж. Фасмана (28 ошибок). Советские ученые в предсказаниях этого класса не участвовали.
Разумеется, наше легкомысленное описание этого по-настоящему интересного и полезного соревнования следует воспринимать как шутку, хотя, конечно, мы не будем протестовать против объявления данного вида спорта олимпийским или против включения его под номером 50 в таблицу «Спортлото». Кстати, и состав советской олимпийской сборной как будто уже определился. В то же время молекулярным биологам не до шуток: проблема третьего этапа биологического кодирования — «первичная структура — третичная структура» — ждет своего решения. Хотя, как мы видели, корректное физическое рассмотрение задачи о формировании третичной структуры белка провести пока не удается, эта проблема все же начинает становиться все более понятной и решение ее становится все ближе. Так что будем надеяться на скорый и решительный успех конформаторов — людей редкой профессии и, увы, нелегкой судьбы.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
ГЛАВА I
ГЛАВА I Задачи обработки земли.Обработка земли преследует две главные, на первый взгляд противоположные, цели: во-первых, она должна стремиться создать такое соотношение благоприятствующих росту растений условий, при котором можно было бы получить самую богатую
ГЛАВА II
ГЛАВА II Самостоятельность растений по отношению к земледелию. Среди наших земледельцев вплоть до сего времени господствует убеждение, что для получения хорошего урожая достаточно только позаботиться, чтобы почва содержала необходимое количество питательных веществ и
ГЛАВА III.
ГЛАВА III. Задачи и план настоящего труда. Уже десять с лишним лет при обработке земли я руководствуюсь принципом, что самый верхний слой почвы надо оставлять на поверхности для того, чтобы он обогатился перегноем. Это имеет большое значение, так как дает возможность
ГЛАВА V.
ГЛАВА V. Влияние обработки на образование слоя плодородной почвы. Какое значение для земледелия будет иметь учение, утверждающее, что при обработке верхний слой почвы надо оставлять на поверхности? Обогатит ли вообще новая система обработки перегноем почву, в частности
ГЛАВА V
ГЛАВА V Питательные для растений веществаРастения, которые мы намерены разводить, только тогда будут расти хорошо и дадут желательный урожай, когда мы, принимая во внимание их самостоятельность (см. гл. II), рациональной обработкой приготовим в почве достаточное
ГЛАВА VI.
ГЛАВА VI. Источники питания растений: атмосфера и почва.Из перечисленных в предыдущей главе питательных для растений веществ меньшая часть находится в атмосфере, большая — в почве.Атмосфера состоит из газов, среди которых находятся твердые тела в пылеобразном состоянии
Глава I
Глава I Восемь лет назад я написал небольшую книгу «Аксиомы биологии»[1], в конце которой высказал предположение, что возможно создание общей теории эволюции последовательно реплицирующихся систем. Завершил я книгу словами: «Под эту категорию попадают не только объекты
Глава 3
Глава 3 Описание метода лечебной кинологии и результатов исследования В предыдущих главах описывались теоретические аспекты метода лечебной кинологии. Постараемся схематически описать практический аспект методологии. Как уже отмечалось, данный метод находится на
Экология окружающей среды: социальный фактор — медицина, профессия на грани кризиса, причины
Экология окружающей среды: социальный фактор — медицина, профессия на грани кризиса, причины Именно терапевты, хирурги, биологи, представители производственной медицины — все они несут ответственность за здоровье населения и поддерживают особые отношения не только
Медицина — профессия опасная. Причины опасности Медицинская статистика во Франции
Медицина — профессия опасная. Причины опасности Медицинская статистика во Франции Информационные данные, взятые из досье Хартии врачей, дают представление о состоянии медицинской практики на протяжении последних 10 лет и позволяют сделать оценку развития и всех
Глава 2. ДНК
Глава 2. ДНК На стене паба “Орел” в Кембридже висит синяя мемориальная доска, установленная в 2003 году в честь пятидесятилетия одного случая, когда разговоры в этом пабе приняли не совсем обычный оборот. Во время обеда 28 февраля 1953 года два завсегдатая “Орла”, Джеймс
ГЛАВА 5
ГЛАВА 5 С помощью Пам Смарт мне удалось разработать более простую и эффективную методику работы с людьми, испытывающими фантомные ощущения в отсутствующих конечностях, чем та, которая была описана в пятой главе.Мы провели серию опытов с людьми, у которых были
Хорошая примета
Хорошая примета «Будет удачным бивак!» — подумал я, увидев тропинку, по которой сновали рыжие степные муравьи Формика пратензис. Но муравьиная тропинка в тугае — еще не муравейник. Его надо найти, что не так просто в густых зарослях колючего лоха, чингиля и шиповника. Туда
7. Происхождение религии. Неистребимая хорошая идея
7. Происхождение религии. Неистребимая хорошая идея Бог умер …Ницше Ницше умер …Бог. — Граффити Когда в 1885 году философ Фридрих Ницше сделал свое знаменитое заявление о смерти Бога, он, разумеется, хотел сказать, что в реальности Бог никогда и не существовал. Подобно