Глава 7. Похвала биологии
Глава 7. Похвала биологии
Каждый из нас, к сожалению, хорошо знаком с неприятным явлением, которое все еще бытует кое-где, несмотря на строгие приказы министерств торговли, культуры и Госкомиздата СССР. Речь идет о так называемой «продаже с нагрузкой». Согласитесь, крайне неудобно и порой накладно приобретать вместе с дефицитной импортной кофточкой набор духов, вместе с книжкой новых стихов любимого поэта — ведомственный сборник «Вопросы изучения влагосодержания грунтов», а вместе с билетом на галерку Большого театра — билет в первый ряд… (пусть читатель сам заполнит оставленное осторожными авторами многоточие).
Это небольшое отклонение от темы имеет тем не менее прямое отношение к общему плану нашего сочинения. Ведь, казалось бы, наша книга получила логическое завершение. После того как жизненный цикл простейшего из живых существ принципиально описан в терминах физики и химии, авторы с полным правом могли бы счесть свою задачу выполненной. К чему же тогда эта последняя, «нагрузочная» глава?
Не претендуя на лестное сравнение предыдущих глав книги с импортным трикотажем, спешим, однако, заверить, что появление этой главы отнюдь не связано с желанием авторов во что бы то ни стало получить квартальную премию за перевыполнение плана по написанным страницам. Если бы дело обстояло подобным образом, не миновать бы читателю рассказа о принципах функционирования биологических мембран, о фотосинтезе, о молекулярном механизме зрения — да мало ли еще о чем! Даже о том, как, собственно, устроена живая клетка, авторы ухитрились умолчать. А все потому, что эти, несомненно, важные и интересные проблемы играют лишь второстепенную роль для доказательства тезиса «организм есть физико-химическая машина», который и был, собственно говоря, основой предыдущего изложения.
Но в том-то и беда, что этот тезис далеко не исчерпывает все принципиальные предпосылки, необходимые для понимания феномена жизни. Существует целая область явлений и понятий, относящихся к биологии как таковой, отличных от понятий физики и химии, и обойти их никак невозможно. Именно в этом причина возникновения последней — наконец-то чисто биологической! — главы нашей книги. Таким образом, хоть в последний момент, хоть в «нагрузку», но биология все же сможет занять подобающее ей первое место… среди наук о жизни.
Организм и машина
И все-таки, несмотря на безапелляционные утверждения авторов, что биология возьмет свое, призрак недоумения еще стоит, по-видимому, перед мысленным взором многих читателей. Как же так? Ведь, проследив шаг за шагом историю жизни поколения вирусов, каждый непредвзятый человек мог убедиться, что никаких специально «биологических» процессов она не содержит: ферментативные реакции, механизмы, обслуживающие цепочку ДНК — РНК — белок, наконец, самосборка вирусных частиц — все это вполне убедительно было разъяснено на «обычном» физико-химическом уровне. Более того, мы упорно подчеркивали роль белковых молекул во всех основных жизненных процессах. (А не авторы ли подшучивали в первых главах над таинственной «биологичностью» белков и громогласно заявляли, что ничего особенного в них нет: молекулы как молекулы?)
И еще один существенный аспект, на первый взгляд означающий новое противоречие: на страницах этой книги многократно назывались имена ученых, посвятивших свою деятельность выяснению тех или иных деталей устройства и функционирования биологических молекул — белков и нуклеиновых кислот. И всякий раз оказывалось, что еще одна молекулярная структура, химическая реакция или иной процесс, имеющий место в организме, ведут себя в полном соответствии с «предписаниями» физики и химии. Создается, по сути дела, впечатление, что вся история молекулярной биологии — это последовательное и неуклонное «вытравление» особого «биологического» начала из описания жизненных процессов, и, судя по рассказам авторов, «вытравление» вполне успешное.
Нет, по-видимому, организм все же можно определить как физико-химическую машину. А высказывания авторов в защиту биологии следует рассматривать попросту как тщетную попытку спасти честь мундира этой «науки». Тем более тщетную, что упомянутая выше деятельность молекулярных биологов приводит к законному вопросу: а существует ли вообще такая наука биология? Не сводится ли она к некоторым (причем частным) проблемам физики и химии?
Что и говорить, приведенная аргументация, «упраздняющая» биологию, выглядит солидно. Но все же обвинять авторов в том, что их сочинение послужило фундаментом для подобных утверждений, было бы рискованно: тезис «организм — машина» впервые был сформулирован известным французским мыслителем XVII века Р. Декартом. А сама идея уничтожения на этом основании биологии как науки получила впоследствии название редукционизма (от латинского reductio — отведение (назад); в данном контексте — сведение). Так что защитники антибиологических высказываний, приведенных выше, с полным правом могут гордо называть себя редукционистами.
(Надо сказать, что удачное, желательно латинское, название научного, литературного или политического направления значит очень многое. Вряд ли кто-нибудь без улыбки воспримет название «ничевоки» (одна из поэтических групп начала 20-х годов), а вот синоним этого слова — «нигилисты» (nihil по-латыни — ничто) произносится вполне уважительно.)
Пора, однако, противопоставить редукционизму, все-таки просочившемуся (вопреки желанию авторов) на страницу этой книги, аргументы в защиту биологии. Впрочем, аргументы — это слишком сильно сказано. Достаточно, пожалуй, напомнить одно-единственное, ускользавшее до сих пор от нас обстоятельство: всякий организм есть результат эволюционного развития и, будучи звеном эволюционного процесса, несет на себе его отпечаток.
Вот это-то «клеймо происхождения», которое лежит на организме (вплоть, как мы вскоре убедимся, до молекулярного уровня), принципиально невозможно объяснить в рамках физики и химии. Эти науки попросту не занимаются такими вопросами: физика может, скажем, с успехом объяснить, как работает двигатель внутреннего сгорания (или миоглобин — в данном примере это почти одно и то же), но абсолютно ничего не в состоянии сказать о том, как он возник. И если в случае двигателя внутреннего сгорания понимание его «родственных связей» с паровым котлом практически ничего не добавляет к нашему представлению о его работе, то аналогичный вопрос «Как функционируют живые организмы?» должен всегда сопровождаться другим: «Каким образом они создавались?» Ибо невозможно понять, почему организм (или даже отдельный его элемент — рука, плавник, чешуя, клетка, молекула гемоглобина) функционирует так, а не иначе, если не проследить, каким образом эволюционный процесс «отбирал» именно такое его устройство.
И в самом деле, задумываясь над всеми этими — будем откровенны — довольно хитроумными ДНК-РНК-белковыми механизмами, над «целесообразным» устройством молекул ферментов или взаимной «пригнанностью» молекулярных блоков в процессах самосборки, невольно задаешься мыслью о том, как это все возникло.
Ну хорошо, мы знаем, что вирус строится точно по образцу предыдущего, являющегося, в свою очередь, копией еще предыдущего, но ведь откуда-то должен был взяться первый?
Как говаривала госпожа Простакова из фонвизинского «Недоросля»: «Портной учился у другого, другой — у третьего, да первое-т-то портной у кого учился?»
Нет, нет, мы, конечно, далеки от того, чтобы подозревать у наших читателей полную неосведомленность в вопросах дарвинизма и теории эволюции. О том, что человек произошел от обезьяны, знают все, и все, несомненно, могли бы ответить госпоже Простаковой теми же словами, что и ее портной: «Да первое-т портной, может, шил хуже меня». Но уж коль скоро мы взялись описывать строение и функции организма на молекулярном уровне, совершенно необходимо придать конкретность также и механизмам процесса эволюции, и также на молекулярном уровне.
Охотники за гемоглобинами
Научно-исследовательские экспедиции в Африку в первой половине XIX века дали огромный географический, геологический и, разумеется, биологический материал: разнообразный и экзотический животный мир — львы, антилопы, леопарды, крокодилы — не только послужил предметом тщательного биологического исследования, но и вдохновил писателей-«приключенцев» на самые яркие и красочные эпизоды и без того захватывающих книг. Ж. Верн, Г. Хаггард, Л. Буссенар — эти мастера увлекательных описаний и сюжетных перипетий и необычной природы, окружающей их героев, несомненно, оказали сильнейшее воздействие на целые поколения молодых людей, так что «обращение» некоторых из этих юношей и девушек в биологию наверняка произошло не без влияния африканской экзотики.
В наши дни, увы, очарование африканской природы утратило черты загадочности и как бы поблекло: современные пресса и литература уделяют куда больше внимания символам, созданным руками человека, — Асуанской плотине или, скажем, медным рудникам Нигерии. И только, пожалуй, биологам, сохранившим в душе юношеский восторг читателей Л. Буссенара, и по сей день удается совершать в Африке весьма экзотические находки и открытия. Одна из таких находок как раз и имеет прямое отношение к теме нашего рассказа: речь идет о так называемой серповидноклеточной анемии — наследственном заболевании крови, довольно широко распространенном среди коренного населения Центральной Африки.
Происхождение этого названия следующее: эритроциты, красные кровяные тельца крови, у здоровых людей имеют форму двояковогнутой линзы. У лиц, страдающих серповидноклеточной анемией, такая форма эритроцитов сохраняется лишь при условии насыщения крови кислородом; при понижении его концентрации эритроциты начинают искривляться и под микроскопом действительно приобретают отдаленное сходство с серпом. В результате изменения формы эритроцитов значительно увеличивается вязкость крови и кровоток через мелкие вены замедляется (именно венозная кровь, как известно, обеднена кислородом). Это, в свою очередь, приводит к еще большему искривлению клеток, замедлению кровотока и в конечном счете может привести к закупорке сосудов.
Это необычное заболевание интересно для нас тем, что оно явилось объектом первого успешного исследования в области так называемой молекулярной патологии, поскольку природа его оказалась связанной со структурой и функцией уже хорошо знакомой нам молекулы гемоглобина. (Что лишний раз подтверждает глубокую правоту приведенного нами ранее высказывания одного из героев И. Ильфа и Е. Петрова о всемогуществе гемоглобина.)
Краткий «хроникерский» отчет о том, как была разгадана причина серповидноклеточной анемии, выглядит примерно так: сначала Л. Полинг (в который уже раз повторяется эта фамилия на страницах нашей книги!) совместно с американцем Г. Итано показали, что гемоглобин, присутствующий в эритроцитах больных серповидноклеточной анемией, отличается от гемоглобина здоровых людей, причем «серповидный» гемоглобин несет меньшее число функциональных групп, заряженных отрицательно.
Затем работами М. Перутца, фамилия которого тоже уже не раз нами упоминалась, было установлено, что в восстановленной, лишенной кислорода, форме «серповидный» гемоглобин намного хуже, чем нормальный, растворим в воде; выпадение внутри эритроцита кристалликов гемоглобина при понижении концентрации кислорода и является причиной деформации клеток.
Наконец, в конце 50-х годов американский биохимик В. Ингрэм смог найти различия в строении молекул нормального и аномального гемоглобинов. Оказалось, что в одном из типов полипептидных цепей, образующих молекулу гемоглобина (напомним, что молекула гемоглобина образована четырьмя полипептидными цепями двух различных типов), остаток глутаминовой кислоты, занимающий в нормальной цепи шестое положение, у аномального гемоглобина замещен остатком валина. Вот и все. Один-единственный остаток из полутора сотен!
(Не этот ли молекулярно-биологический факт предвидели народные поговорки насчет ложки дегтя в бочке меда и паршивой овцы, которая портит все стадо? Во всяком случае, будущим историкам молекулярной биологии не мешало бы иметь это обстоятельство в виду: всякая «приличная» наука просто обязана иметь солидные корни, по возможности уходящие в глубь веков.)
Каким же образом удается одному-единственному «пришельцу» так основательно испортить механизм функционирования гемоглобина? Все дело в том, что, как и предсказывали Л. Полинг и Г. Итано, в аномальном гемоглобине число отрицательно заряженных групп оказывается меньше: меньше на один карбоксил, принадлежащий этому самому остатку глутаминовой кислоты. Появление вместо сильно полярного остатка глутаминовой кислоты гидрофобного остатка валина, естественно, должно понизить растворимость белка в воде, что, как мы уже писали, и характерно для «серповидного» гемоглобина в восстановленном состоянии (без кислорода). Сохранение же растворимости в окисленном состоянии получило объяснение сравнительно недавно в работах того же М. Перутца и оказалось связанным с небольшими изменениями конформации молекулы гемоглобина при присоединении кислорода; остаток валина при этом как бы частично прячется внутрь глобулы.
Описав столь подробно результаты исследований природы серповидноклеточной анемии, мы хотели еще раз, как бы между делом, продемонстрировать возможности современной молекулярной биологии; главная цель этого повествования заключалась, однако, просто в утверждении единственного факта: встречаются наследственные аномалии, связанные с заменой одной-единственной аминокислоты в аминокислотной последовательности какого-либо белка.
Не следует, правда, думать, что экзотические белки из семейства глобинов «водятся» только в далекой Африке. Сразу же после начала описанных событий (1950 год) неутомимые молекулярные биологи приступили к планомерному «отлову» аномальных глобинов, и вскоре Г. Итано обнаружил еще один, в котором, как оказалось, все тот же шестой остаток глутаминовой кислоты был замещен остатком лизина. Общее же число аномальных глобинов, известных в настоящее время, составляет около двух сотен. Обозначаются они названиями мест, где были впервые обнаружены: Нв Париж, Нв Нью-Йорк, Нв Милуоки, Нв Ибадан, Нв Дофар, Нв Сидней или еще более загадочно: Нв Кушатта, Нв УбеII. При каждом таком названии указывается также и характер аминокислотного замещения: 12 аланин аспарагиновая кислота, 68 аспарагин аспарагиновая кислота и т. д.
Конечно, несмотря на чрезвычайно обширную географию, поиски аномальных глобинов лишены той буссенаровской или жюль-верновской романтики ночевок у костра под открытым небом, тревожных шорохов и криков в зловещих джунглях или смертельной опасности поединка отважного биолога с берберийским львом. И все же работу по изучению природы молекулярных патологий можно смело сравнить с теми, первыми экспедициями знаменитых Д. Ливингстона, Г. Стэнли. Н. Миклухо-Маклая, Н. Пржевальского: разница лишь в том, что интересы сегодняшних молекулярных биологов по большей части направлены не на окружающую организм среду, а, так сказать, «внутрь» организма. Именно туда, в глубь клетки, и пролегают маршруты их теперешних «экспедиций».
Проверьте свой гемоглобин
Приятно отметить, что авторы не уклоняются от своих обязанностей, а исправно подогревают воображение читателя картинами ночных джунглей и подвигами отчаянных сорвиголов, которые, презрев все опасности, добывают очередной сорт аномального глобина. Да и сама история расследования «дела» о серповидноклеточной анемии вполне способна, на наш взгляд, соперничать даже со знаменитой историей «пляшущих человечков», разгаданной Шерлоком Холмсом. Однако пора прислушаться и к той, наиболее ортодоксальной части читателей, которая с нетерпением ждет, когда же начнется обещанный разговор об эволюции на молекулярном уровне.
Такой разговор, по существу, уже давно идет: ведь все описанные ранее аномалии в строении белков являются наследственными, передающимися из поколения в поколение. Это означает, иными словами, что замена одного аминокислотного остатка другим обусловлена какими-то изменениями в основной генетической информации, то есть в последовательности оснований ДНК, точнее, в том ее участке, который кодирует последовательность соответствующей цепи гемоглобина.
При рассмотрении всех типов аминокислотных замен, обусловливающих появление аномальных глобинов, можно установить одну любопытную закономерность. Если сравнивать триплеты нуклеотидов, кодирующие пару аминокислотных остатков — подвергшегося замене и занявшего его место, — то окажется, что во всех без исключения случаях триплеты различаются одним-единственным нуклеотидом. Скажем, замене аланин ? аспарагиновая кислота соответствует переход ГЦУ ? ГАУ или ГЦЦ ? ГАЦ; замене глутаминовая кислота ? валин, вызывающей серповидноклеточную анемию — ГАА ? ГУА или ГАГ ? ГУГ и т. д.
Как мы знаем, точность воспроизведения, «переписывания» генетической информации весьма высока: за этим, в частности, и следят высокоспецифичные ферменты, обеспечивающие нужную для точного воспроизведения последовательность действий. И уж конечно, они справляются со своей задачей гораздо лучше, чем тот издательский коллектив, по вине которого, как уверяли И. Ильф и Е. Петров, после сорока корректур на титульном листе солидного издания появились слова «Британская энциклопудия». Ясно поэтому, что если ферменты и допускают «опечатку», то скорее всего именно такую — «однобуквенную».
Таким образом, происхождение аномальных глобинов может быть легко объяснено: они представляют собой следствие единичных ошибок репликации, ошибок изготовления комплементарных копий молекулы ДНК. Достаточно при репликации ошибочно включить в ДНК-овую последовательность «не то» основание — и это приведет в конечном счете к замене в аминокислотной последовательности какого-то из белков одного остатка другим.
Впрочем, правильнее было бы сказать «может привести». В очень многих случаях замена, например, последнего нуклеотида в триплете не приведет к каким-либо изменениям в кодируемом им остатке: например, такие остатки, как валин, аланин, пролин и т. п., кодируются, по существу, двумя первыми основаниями триплета, поскольку в третьей позиции может быть любое из четырех оснований.
Случайная замена в процессе репликации одного нуклеотида другим называется «точечной мутацией». Термин «мутация» был введен в генетику еще в конце прошлого века (русским ученым С. Коржинским и голландцем Г. Де Фризом) для обозначения скачкообразного изменения наследуемого признака. Очевидно, что элементарное, наименьшее изменение такого рода может быть достигнуто как раз за счет единственного изменения в нуклеотидной последовательности. В естественных условиях мутации, таким образом, являются, повторим еще раз, «опечатками» процесса репликации.

Возвращаясь к типографско-языковедческой аналогии, напомним темпераментную дискуссию о будущем правописании русского языка, которая происходила не так уж давно — где-то в начале 60-х годов: это та самая дискуссия, инициаторы которой предлагали писать «заец» и «мыш» в целях приближения правописания к произношению. Часть аргументов «преобразователей» нашла, если помните, довольно удачное, хоть и слегка вульгаризованное, отражение в поговорке, распространенной в те годы среди школьников: «Как ни пиши: „велосипед“ или „виласапет“, от этого он мотоциклом не станет». О забавном эпизоде из жизни языковедов мы вспомнили потому, что ситуация, создающаяся при переписывании генетических «текстов», принципиально иная: неправильно записанный нуклеотидный «виласапет» вполне способен в конечном счете породить белковый «мотоцикл»…
И в самом деле: какие же последствия может вызвать замена нуклеотида в цепи ДНК и, следовательно, одного аминокислотного остатка в белковой цепи другим? Как свидетельствует пример только что рассмотренного «серповидного» гемоглобина, это может, например, привести к изменению растворимости белка. Замена небольшого бокового радикала, находящегося внутри глобулы, более громоздким может вызвать разрыхление третичной структуры и снизить ее стабильность. В результате замены глицинового остатка каким-либо другим возможны ограничения конформационной подвижности полипептидной цепи и т. п. Вообще, чем более различаются по своим физико-химическим, а также «конформационным» свойствам «исходный» и «новый» остатки, тем больше это скажется на изменении строения и свойств молекулы белка.
Правда, как отметил известный советский биофизик М. Волькенштейн, структура генетического кода такова, что в результате замены одного нуклеотида в триплете в среднем наблюдается меньшее изменение физико-химических свойств остатка, чем это должно было бы иметь место при случайных заменах одного остатка другим.
Это означает следующее. Аминокислотные остатки различаются между собой по своим физико-химическим свойствам (и тем самым по своей роли в образовании и поддержании третичной структуры белковых молекул) в большей или меньшей степени. Мы уже говорили об остатках гидрофобных и гидрофильных; можно провести также разделение и по некоторым иным признакам. Например, аминокислоты лизин и аргинин содержат в своих боковых цепях щелочные группы, глутаминовая и аспарагиновая кислоты (естественно!) — кислые; фенилаланин, тирозин, триптофан, гистидин — обладатели ароматических боковых радикалов, и т. п. Так вот, оказывается, что триплеты, кодирующие близкие по свойствам аминокислоты, как правило, отличаются друг от друга лишь одним-единственным нуклеотидом; напротив, аминокислоты, физико-химические свойства которых резко различны, кодируются триплетами, различающимися двумя или даже тремя нуклеотидами. И если бы в результате точечных мутаций замены между любой парой аминокислотных остатков могли бы осуществляться с равной вероятностью, процент «брака», то есть доля организмов с «нежизнеспособными» белками определенного типа был бы гораздо выше, чем это имеет место на самом деле.
Иными словами, генетический код обладает известной «помехоустойчивостью», обеспечивающей как бы дополнительную защиту синтезируемой по инструкции ДНК белковой молекулы от случайных мутаций в этой самой ДНК.
Исследование мутантных гемоглобинов показало к тому же, что далеко не каждая аминокислотная замена из числа наблюдаемых сопровождается изменением физико-химических свойств белка, а тем более какими-либо функциональными расстройствами организма.
Точечные мутации, приводящие к очень сильным нарушениям свойств гемоглобина, не бывают обнаружены просто потому, что индивидуумы — носители таких мутаций нежизнеспособны. Если подобная мутация происходит, организм погибает на ранних стадиях развития плода.
С другой стороны, поскольку значительную часть мутантных гемоглобинов удалось обнаружить в результате биохимического исследования людей, страдающих заболеваниями крови, естественно, что именно мутации, обусловившие то или иное заболевание, представлены среди описанных аномальных гемоглобинов более часто сравнительно с их распространением. Ведь если мутация является нейтральной, то есть не вызывает никаких функциональных изменений, она чаще всего остается незамеченной. И ходят себе по белу свету тысячи, десятки тысяч (а может быть, и гораздо больше) людей, даже не подозревающих о том, что в ?-цепи их гемоглобина вместо положенного остатка валина в 98-м положении стоит бог знает что!
Так что если вы, уважаемый читатель, обладаете достаточно крепким здоровьем, чтобы регулярно подвергаться профилактическому медицинскому обследованию в районной поликлинике, проявите еще чуточку настойчивости и добейтесь, чтобы ваш гемоглобин был исследован с точки зрения правильного чередования его аминокислотных остатков.
Правда, пока такая процедура очень трудоемка и выполняется лишь в немногих лабораториях мира, но это вряд ли может служить препятствием для истинного энтузиаста профилактических обследований. Тем более что в результате такого обследования науке может стать известно существование еще одного мутантного гемоглобина — скажем, Нв Бобруйск.
Молекулярный дарвинизм?
«Нет худа без добра» — эта в высшей степени философская поговорка вполне могла бы послужить эпиграфом раздела, в котором (наконец-то!) будет приведен очерк основной идеи дарвинизма, изложенный «на молекулярном уровне». Как обычно, очерк этот будет крайне лаконичным и иллюстративным. И все же можно надеяться, что при всей упрощенности главные тезисы возникшего совсем недавно научного направления — так называемой молекулярной эволюционистики — будут в нем изложены.
Выяснение вопросов различия и сходства «добра» и «худа» будет проводиться, однако, вовсе не на уровне абстрактных и высоконаучных философских диспутов, а на вполне конкретных, а иногда даже и попросту примитивных молекулярно-биологических примерах. Тем не менее уже одно представление о «вредных» и «нейтральных» мутациях наводит на некоторые размышления.
Возьмем нейтральные мутации, в предположительном существовании которых мы (конечно, в шутку!) призывали читателей убедиться на примере их собственных гемоглобинов: известно, что они бывают иной раз распространены довольно широко и имеют возраст в несколько тысячелетий. Часто такая мутация передается из поколения в поколение у группы, занимающей определенный район обитания: так, у многих китайцев одна из цепей гемоглобина отличается от «нормальной» одним остатком. Этот признак настолько устойчив, что распространение той же мутации среди части американских индейцев считается еще одним убедительным доказательством их монголоидного происхождения. И, поскольку никаких частых случаев наследственных болезней крови ни среди китайцев, ни среди индейцев не отмечалось, мы вправе считать эту мутацию действительно «нейтральной».
Но вот задача похитрее: та же самая аминокислотная замена, которая вызывает серповидноклеточную анемию, будучи бесспорно вредной, влекущей за собой тяжелую болезнь и высокую смертность в детском и юношеском возрасте, тем не менее сообщает организму одно важное полезное качество. Именно эритроциты «серповидноклеточных» больных гораздо более, чем нормальные, устойчивы по отношению к малярийному плазмодию, а тем самым носители «серповидноклеточной» мутации оказываются невосприимчивыми к малярии. Так как же в конечном счете расценивать такую мутацию: как проявление «худа» или «добра»? И кто возьмет на себя смелость «выставить оценку» той или иной мутации, отнести ее к числу «положительных» или «отрицательных»?
В значительной мере этот вопрос является, конечно, риторическим, ибо ответ на него стал известен и получил свою окончательную форму уже в «Происхождении видов» — работе, которую без преувеличения можно назвать библией современной биологии. Естественный отбор, идущий под влиянием чрезвычайно сложной совокупности климатических, пищевых, экологических и многих, многих других условий жизни, — вот что определяет «полезность» или «вредность» изменений, происшедших в организме вследствие возникновения мутации. А главным мерилом «пригодности» организма в процессе эволюции являются с точки зрения естественного отбора шансы организма на выживание.
Следовательно, эволюционный процесс, по современным представлениям, идет следующим образом: среди случайным образом возникающих мутаций некоторая часть вызывает такие изменения строения и свойств соответствующих белков, которые на уровне целого организма находят выражение в виде каких-то функциональных изменений, понижающих (или повышающих) шансы индивидуума в борьбе за существование. Соответственно его потомство (если оно вообще появляется) оказывается сравнительно нежизнеспособным (или, наоборот, весьма жизнестойким). В конечном счете носители этой мутации оказываются либо обреченными на более или менее быстрое вымирание, либо, напротив, вследствие повышенной жизнестойкости, активно размножаются и завоевывают себе вполне подходящее «место под солнцем».
Как видите, никакого противоречия с «классическим» дарвинизмом эта «молекулярная» схема не содержит: напротив, представления молекулярной биологии во многом дополняют, придают конкретность понятию об элементарном «шаге» эволюционного процесса — точечной мутации. И по всей справедливости новая единица меры развития эволюционного процесса (в основу ее определения легло именно понятие точечной мутации) носит название «дарвин».
Здесь стоит, пожалуй, отметить, что в широких кругах людей, интересующихся наукой (но не занимающихся ею), почему-то распространено мнение, согласно которому всякая вновь возникшая область фундаментальной науки как бы «отрицает» сложившуюся до нее систему представлений. Каждый из нас, пожалуй, читал, например, что механика А. Эйнштейна «отрицает» механику И. Ньютона и Г. Галилея, а та, в свою очередь, «отрицала» положения, принятые во времена Аристотеля…
На самом деле это в корне неверная точка зрения: новая область исследований, как правило, дополняет, развивает, обобщает накопленные ранее наблюдения и выводы, но никак не «отрицает» их (достаточно вспомнить знаменитую фразу И. Ньютона: «Я видел так далеко потому, что стоял на плечах гигантов»). Вот и в нашем случае: система именно таких представлений об эволюционном процессе возникла задолго до появления самого термина «молекулярная биология».
Но, разумеется, выяснение деталей молекулярного механизма взаимосвязи событий: «точечная мутация ? аминокислотная замена ? изменение функциональных свойств белка» (как это было сделано на знакомом нам примере «серповидноклеточного» гемоглобина) — остается в полной мере прерогативой молекулярной биологии. И можно было бы в принципе сконструировать модель того, каким образом различаются «вредные» и «нейтральные» мутации на уровне белковой молекулы, допустим гемоглобина, благо примеры аномальных гемоглобинов нам уже известны.
Казалось бы, задача эта сравнительно проста: во всяком случае, повредить молекулу гемоглобина, «испортить ей жизнь» с помощью гипотетических аминокислотных замен чрезвычайно легко. Можно, скажем, включить в аминокислотную последовательность побольше остатков пролина. Это приведет к резкому изменению конформации белка, поскольку пролин, как известно, препятствует образованию регулярных участков структуры ?-спиралей, а в гемоглобине процент таких спиралей весьма высок. Или другой способ: заменить в последовательности остатки, непосредственно примыкающие к группе гема, которая отвечает за функциональную активность белка, на другие, совершенно иные по физико-химическим свойствам. Подойдут также замены типа «серповидноклеточной», существенно меняющие физико-химические свойства молекулы в целом. Ну а «нейтральные» замены можно проводить по обратному принципу: подбирать такие места в аминокислотной последовательности (и такие «заменяющие» остатки), чтобы изменения всех упомянутых выше характеристик молекулы были минимальными.
Привычное предупреждение авторов об абсолютной нереальности описанных выше издевательств — пусть даже гипотетических — над молекулой гемоглобина следует на сей раз еще более усилить: все эти манипуляции представляют собой чистейшей воды химеры, этакий плод распаленного воображения молекулярного биолога. И, что самое обидное, фантазии наши оказываются к тому же и бесполезными, ибо на вопрос, как именно повлияют на организм изменения молекулярных характеристик того или иного белка, мы, увы, не в состоянии ответить (во всяком случае, пока не в состоянии), а ведь отбор, напомним, проходит на уровне организмов…
Так что на самом деле классификация мутаций на «вредные», «нейтральные» и чрезвычайно редко встречающиеся «полезные» чудовищно условна. И не только из-за неоднозначности соответствия между изменением свойств белка и изменением свойств организма, что подтверждается примером «серповидноклеточного» гемоглобина, придающего эритроцитам антималярийные свойства. Основным препятствием, не позволяющим с уверенностью разделить мутации на «хорошие» и «плохие», является исключительная сложность процесса естественного отбора; иными словами, естественный отбор весьма трудно прогнозировать, и трудно сказать, какими окажутся шансы на выживание у организма, претерпевшего ту или иную мутацию, когда он предстанет «на суд» естественного отбора. Во всяком случае, носителям «серповидноклеточной» мутации, живущим, как упоминалось, в Центральной Африке, естественный отбор предоставляет на выбор анемию или малярию; и уж конечно, с точки зрения шансов на выживание сделать такой выбор нелегко.
Короче говоря, если даже молекулярные биологи проявят максимум энергии, умения и изобретательности и в конце концов до последней тонкости выяснят, как именно скажется данная мутация на уровне организма в целом, проблема приложения эволюционной теории к анализу путей происхождения какого-либо конкретного вида или группы видов останется, увы, решенной не до конца. Ведь для полного решения необходимо будет еще воссоздать весьма подробную картину факторов отбора, действующих на каждом этапе эволюции, а это, как ни жаль, практически невозможно.
Впрочем, нам пора остановиться: еще немного, и увлекшиеся авторы начнут красочно описывать «чужие», не молекулярно-биологические заботы. («Как будто им своих не хватает!» — принято, кажется, говорить в подобных ситуациях.) Нет уж, пускай «классические» эволюционисты сами рассказывают о проблемах и сложностях эволюции организмов, нас с вами интересует в первую очередь эволюция главных биологических молекул — белков.
Из мухи — слона
Нет, нет, завершающие слова предыдущего раздела насчет эволюции белков не являются ни обмолвкой авторов, ни оплошностью редактора: мы прекрасно понимаем, что эволюционировать в биологически точном значении этого слова, то есть подвергаться отбору, может лишь организм в целом, обладающий всеми атрибутами жизни. Белковые же молекулы, будучи сами по себе «неживыми», способны лишь изменять в результате мутаций свои аминокислотные последовательности. Именно в этом смысле и говорят об эволюции белков.
Но, с другой стороны, изменения в аминокислотной последовательности одного и того же белка в различных видах организмов дают прекрасную возможность подсчитать число элементарных шагов эволюции — точечных мутаций, разделяющих эти виды, и, оценив тем самым их сходство, сопоставить результат оценки с выводами «классической» эволюционной теории. Такое сопоставление и было проведено, как только удалось установить аминокислотные последовательности гемоглобинов, выделенных у различных животных.
(Не правда ли, обилие гемоглобинов в нашем сочинении начинает надоедать? Но что поделать — мы еще во второй главе предупреждали об уникальной роли гемоглобина в современной молекулярной биологии. Лет через двадцать, возможно, какой-нибудь другой белок — пепсин, карбоксипептидаза, парвальбумин — будет изучен лучше, но пока гемоглобин является бесспорным любимчиком биологов.)
Таким образом, подчеркнем еще раз, молекулярная теория эволюции ни в коей мере не попыталась вступить в конфликт с теорией эволюции «классической» или, упаси боже, подменить ее: она просто стала одним из разделов общего эволюционного учения.
В теории эволюции принято для большей наглядности производить описание происхождения и «родственных» связей некоторой группы видов с помощью построения так называемого филогенетического древа. Оценивая степень сходства между всеми парами подлежащих классификации видов, их располагают на «кроне» схематического древа, у «корня» которого находится их общий предок, а все ветки получены последовательным раздвоением. При этом наиболее разнящиеся пары видов окажутся на ветвях, расходящихся вблизи «корня», а виды, близкие друг другу, займут места на соседних ветвлениях кроны.
При сравнении аминокислотных последовательностей цепей гемоглобинов, выделенных из крови животных различных видов, выяснилось, что они тоже оказались «родственниками» и, что самое интересное, их филогенетическое древо, построенное на основании подсчета точечных мутаций, абсолютно ничем не отличается от такого же древа, построенного ранее на основании морфологических и анатомических данных.
Аналогичные построения были выполнены и по данным об аминокислотной последовательности других белков, причем диапазон сравниваемых видов был существенно расширен. Так, фермент-переносчик электрона цитохром С присутствует во всех животных и абсолютном большинстве растительных видов; при построении филогенетического древа на основании анализа аминокислотных последовательностей этого белка в рассмотрение были включены (помимо многих прочих), например, столь удаленные виды, как человек, цыпленок, моль, дрожжи. И в этом случае полученные филогенетические деревья не отличались от «классических», базирующихся на данных сравнительной морфологии и анатомии.
Итак, повторяем, молекулярная теория эволюции расширила круг представлений о механизмах эволюционного процесса, отнюдь не за счет опровержения классических результатов; наоборот, зачастую такие результаты получили более подробное истолкование. И, кроме того, стало очевидно, что происхождение, эволюция белков, несомненно, имеют прямое отношение к принципам организации белковых молекул; ведь аминокислотные последовательности глобинов, скажем комара и человека, различаются весьма существенно, а вот основные детали пространственной структуры остаются неизменными. На долгом пути эволюции белок, несмотря на аминокислотные замены, продолжает сохранять свой «смысл», выполнять свою основную функцию.
Процесс эволюции отдельного белка удивительно точно может быть проиллюстрирован с помощью одной старой головоломки. Называется эта головоломка «Из мухи — слона», а суть ее заключается в следующем. Заменив в слове «муха» одну из букв, можно получить какое-либо другое слово, имеющее смысл, например, «мука» или «мура». Полученное таким образом слово может быть опять преобразовано заменой одной буквы: например, «мука» — «рука», «мура» — «кура» и т. д. Задача заключается в том, чтобы с помощью таких вот последовательных переходов за счет замены одной буквы от одного осмысленного слова к другому в конце концов из «мухи» получить «слона»:
МУХА
МУКА
РУКА
…………
…………
СЛОН
Головоломка, надо признаться, довольно сложная, и авторам, например, так и не удалось ее решить; надеемся, однако, что изобретатель головоломки нас не разыгрывает и такое решение все же существует. Впрочем, нам важно вовсе не само ее решение, а удивительная аналогия процесса решения с эволюционным процессом на молекулярном уровне. В самом деле, некоторое «предковое слово» («муха») преобразуется путем последовательных замен одного из элементов каким-либо другим в новую последовательность, причем все промежуточные последовательности должны быть «осмысленными», то есть белок должен сохранять свои функционально важные свойства.
Головоломка эта была создана задолго до того, как стало что-либо известно о генетическом коде, первичных структурах, точечных мутациях и тому подобных вещах. Однако можно ли себе представить более удачную и общедоступную модель молекулярной эволюции — тем более что речь идет в ней о «взаимопревращении» живых существ: мухи и слона?
Авторы даже осмеливаются предложить основанную на этом же принципе игру для школьников младшего и среднего возраста под названием «Филогенетическое древо». В конце концов, нынешним первоклассникам, изучающим основы теории множеств, не повредят и основные понятия теории эволюции. Главное правило игры — «осмысленные» буквенные замены — остается неизменным, но вместо «цепочки» играющим предлагается построить «филогенетическое древо» какого-нибудь четырехбуквенного слова с единичными заменами типа «согласная — согласная» (правые ветви) или «гласная — гласная» (левые ветви). Каждое слово, как и положено в «настоящем» филогенетическом древе, должно, таким образом, «породить» два следующих «вида». Вот как, например, могло бы выглядеть начало «филогенетического древа» слова «кора»:
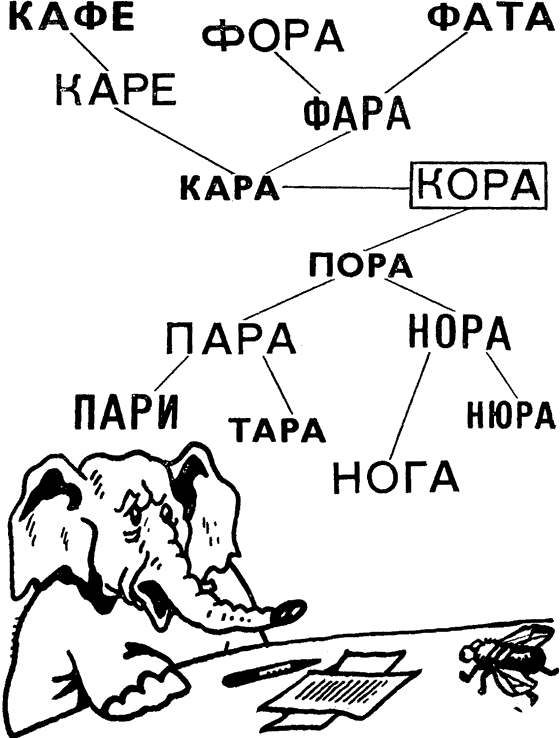
Выигрывает, естественно, тот, кому удастся получить более обильное «потомство», то есть избрать наиболее «беступиковый» путь «эволюционного» процесса. А это не так уж легко: во всяком случае, авторы не смогли избежать «тупика» с заменой гласной в слове «каре» и обошли такой же «тупик» в развитии слова «нора» с помощью полужульнического приема, включив в рассмотрение имена собственные. Так что, пожалуй, нашу игру можно смело рекомендовать также и старшим школьникам, студентам (в особенности студентам биологических специальностей) и даже научным работникам. Итак, как говорилось в песне, предваряющей ныне уже полузабытые телевизионные конкурсы КВН, «берите в руки карандаш» и… — становитесь «эволюционистами».
Нв Лепоре
После успешного сведения основных понятий о молекулярной теории эволюции к детским играм может сложиться впечатление, что ничего нового сравнительно с «обычной» эволюционной теорией она не внесла, тем более что мы постоянно подчеркивали: молекулярную теорию эволюции следует рассматривать как часть общего эволюционного учения. Однако дело обстоит вовсе не так: роль «молекулярной» части теории эволюции вовсе не сводится исключительно к объяснению и подтверждению результатов, полученных «классическими» способами. Новые методы открыли не только новые возможности наблюдения, они привели к открытию и некоторых принципиально новых явлений эволюционного процесса.
Давайте вернемся к рассмотрению молекулы все того же гемоглобина. Два типа полипептидных цепей, образующих эту молекулу, ?- и ?-цепи, несколько различаются по аминокислотной последовательности, но обнаруживают черты несомненного сходства. Это означает что они произошли от некоторого общего предка, и потом их эволюция продолжалась независимо в рамках эволюции одного и того же организма. По мере усиления степени «специализации» функции каждого типа цепей в составе молекулы гемоглобина различия в структуре усиливались.
Объяснение подобному явлению следует, по-видимому, искать в своеобразной «ошибке» процесса репликации, происшедшей в прошлом (и, судя по различию в аминокислотных последовательностях, в довольно отдаленном прошлом). Участок ДНК, несущий информацию об аминокислотной последовательности некоего предкового, «ископаемого» глобина, оказался в матричной копии сдублированным дважды, и каждая из двух последовательностей после этого формировалась в процессе дальнейшей эволюции отдельно.
Вообще говоря, последовательность этого типа дублировалась в геноме млекопитающих не один и даже не два раза, судя по наличию обладающих особыми функциями цепей гемоглобина — так называемых ?- и ?-цепей, а также уже упоминавшейся молекулы миоглобина (как мы помним, ее пространственная структура весьма сходна со структурой субъединиц, составляющих молекулу гемоглобина). Этот эффект, называемый дупликацией гена, был известен генетикам еще в «домолекулярную» эпоху, однако выяснение его роли в эволюционном процессе следует целиком «записать на счет» молекулярной биологии.
Описанный пример свидетельствует о том, что точечные мутации являются вовсе не единственным способом осуществления эволюционного процесса. Наоборот, помимо дупликации гена, эволюция может идти за счет многих других хитроумных, хотя и редких по сравнению с точечными мутациями, но крайне важных явлений.
Назовем прежде всего выпадения части последовательности генетического материала, так называемые делеции. Механизм их возникновения можно представить себе следующим образом: молекула ДНК, с которой в процессе репликации снимается комплементарная копия, изогнулась в какой-то части с образованием петли, скажем, так, как рисуют траекторию самолета на схемах, поясняющих, что такое «мертвая петля». В результате часть генетического «текста» оказывается пропущенной. При сравнении аминокислотных последовательностей белков, состоящих в сравнительно близком «родстве», такие выпавшие участки обнаруживаются очень легко.
Рассмотрим вкратце еще один эффект, влияющий на формирование аминокислотных последовательностей белков, — кроссинговер при аберрантной конъюгации. Использование здесь этих мудреных слов следует понимать всего лишь как авторскую шутку, желание немножко припугнуть читателя, до сих пор тщательно оберегаемого от всяких научных терминов. Мы обойдемся без объяснения точного смысла каждого из этих устрашающих понятий, а попросту рассмотрим пример названного эффекта — аномальный гемоглобин Лепоре.
В отличие от названий аномальных гемоглобинов, возникших в результате точечной мутации, название гемоглобина Лепоре не происходит от географической местности — это просто фамилия семьи, в которой он был впервые обнаружен.
Аномалия типа Лепоре отличается от только что рассмотренных. Состоит она в следующем: в нормальном организме среди прочих типов цепей гемоглобина встречаются уже упоминавшиеся выше ?- и ?-цепи. Они имеют одинаковую длину — 146 остатков и очень близки по аминокислотной последовательности; различия касаются лишь 10 положений. Так вот: у лиц с аномалией типа Лепоре есть только одна цепь такой длины. Ее структуру легко может себе представить всякий, кто хотя бы однажды видел кентавра или русалку: начальная часть этой молекулы имеет последовательность ?-цепи, конец — последовательность ?-цепи. Хорошо изучены два случая аномалий подобного типа: Нв Лепоре Вашингтон и Нв Лепоре Голландия. Различие между ними заключается в том, что у первого ?-последовательность сменяется ?-последовательностью на участке между 22-м и 55-м остатком, у второго — между 87-м и 116-м остатком. Столь приблизительное определение этой границы объясняется просто: на участках 23?54 и 86?115 аминокислотные последовательности обеих цепей совпадают.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Глава 1. О прогрессивном развитии в биологии
Глава 1. О прогрессивном развитии в биологии Мы, разумные существа, не должны забывать, что наша цивилизация — лишь одно из замечательных явлений природы, зависящих от постоянного притока концентрированной энергии солнечного излучения. Ю. Одум Вопрос о движущих силах
Глава 11. Что дает энергетический подход для теоретической биологии, или попытка ответить на вопросы «почему»?
Глава 11. Что дает энергетический подход для теоретической биологии, или попытка ответить на вопросы «почему»? Многие вещи нам не понятны не потому, что наши понятия слабы, но потому, что сии вещи не входят в круг наших понятий. Козьма
Глава 5. Похвала ферментам
Глава 5. Похвала ферментам Высокое и несколько уже позабытое в наш рациональный век искусство многозначительных умолчаний, таинственных намеков и прочего кокетства не должно, казалось бы, иметь никакого отношения к рабочему стилю литературного произведения,
Глава 3 Рождение современной биологии
Глава 3 Рождение современной биологии Новая анатомияЗнаменующим началом научной революции принято считать 1543 г. В этом году польский астроном Николай Коперник опубликовал книгу, где была изложена новая точка зрения на Солнечную систему, центром которой было Солнце,
Глава 13 Постсовременное состояние эволюционной биологии
Глава 13 Постсовременное состояние эволюционной биологии Пер. А. СамородоваВ предыдущих двенадцати главах мы рассмотрели многообразие аспектов эволюции жизни. Подобное рассмотрение, конечно, никоим образом не может быть всеобъемлющим, но это и не было моей целью. Так или
4.2. Основные понятия биологии развития
4.2. Основные понятия биологии развития В конце XX века зародилась новая междисциплинарная наука – биология развития, объединившая достижения эмбриологии, генетики, биохимии, цитологии и ставшая одним из ведущих направлений в познании «феномена жизни». Биологию развития
4.4. Теоретическое значение и проблемы биологии развития
4.4. Теоретическое значение и проблемы биологии развития Как уже отмечалось, проблема механизмов развития многоклеточного организма из оплодотворенной яйцеклетки является одной из ключевых проблем биологии. Биология развития в настоящее время находится на «переднем
5.6. Понятие прогресса в биологии
5.6. Понятие прогресса в биологии Согласно взглядам основоположника отечественной эволюционной морфологии А. Н. Северцева, наиболее общее направление эволюции – биологический прогресс, т. е. возрастание приспособленности потомков по сравнению с предками. Анализ
Глава 1. Нерешенные проблемы биологии
Глава 1. Нерешенные проблемы биологии 1.1. Предпосылки успеха Цель механистического подхода в биологическом исследовании особенно ясно была выражена более ста лет назад Томасом Хаксли в следующем определении:«Зоологическая физиология — это доктрина функций или
Заключение. Величайшая тайна биологии
Заключение. Величайшая тайна биологии Мой рассказ о происхождении секса у позвоночных подходит к концу, но исследования продолжаются. Всё новые экспедиции обследуют каждый уголок Гоугоу в поисках ископаемых свидетельств, в надежде однажды найти то, что либо подтвердит
Глава вторая ДНК Рационализация биологии
Глава вторая ДНК Рационализация биологии Почти все проявления жизни заложены на молекулярном уровне, и без понимания молекул мы можем иметь лишь весьма поверхностное понимание самой жизни. Френсис Крик Великая идея: наследственность закодирована в ДНККаждый из нас
1. Краткая история развития биологии
1. Краткая история развития биологии Вспомните!Какие достижения современной биологии вам известны?Каких учёных-биологов вы знаете?Современная биология уходит корнями в глубокую древность, мы находим её истоки в цивилизациях прошлых тысячелетий: в Древнем Египте,
Глава I. Основы мичуринской биологии Кандидат сельскохозяйственных наук Е. К. Меркурьева
Глава I. Основы мичуринской биологии Кандидат сельскохозяйственных наук Е. К. Меркурьева 1. Понятие о биологии Биология — это наука о законах развития живой природы. Она изучает жизнь как животных, так и растений. Основная задача биологии состоит в том, что она должна
1. Понятие о биологии
1. Понятие о биологии Биология — это наука о законах развития живой природы. Она изучает жизнь как животных, так и растений. Основная задача биологии состоит в том, что она должна вскрывать способы управления развитием живых организмов в интересах человека.Это означает,