Глава 5 Сетевая геномика мира прокариот: вертикальные и горизонтальные потоки генов, мобиломы и динамика пангеномов
Глава 5
Сетевая геномика мира прокариот: вертикальные и горизонтальные потоки генов, мобиломы и динамика пангеномов
Пер. В. Анисимова
Когда Дарвин писал об эволюции, он имел в виду животных и растения, по крайней мере он использовал эти сложные многоклеточные организмы во всех своих конкретных примерах. Одноклеточные формы жизни практически не упоминаются в «Происхождении видов…» или любой другой книге Дарвина. В любом случае, учитывая, что Дарвин серьезно обсуждал происхождение всех существующих ныне видов от одной или нескольких предковых форм (см. гл. 2 и 11), он должен был исходить из того, что эти предки были одноклеточными[47]. Эрнст Геккель, плодовитый немецкий последователь Дарвина, поместил протист (одноклеточных эукариотов, часто называемых этим термином даже сейчас) и дробянок (ныне известных как прокариоты — бактерии и археи) в основании своего монументального древа жизни, первого из подобных деревьев, которое было населено реальными жизненными формами. Естественно, животные доминировали на дереве Геккеля, в то время как протисты и дробянки располагались на неопределенных позициях поблизости от корня.
Вездесущесть и важность бактерий в биосфере постепенно становились очевидными параллельно с развитием эволюционной биологии, вначале благодаря полным драматизма исследованиям бактериальных патогенов, а позднее в результате достижений экологической микробиологии. Достаточно рано микробиологи показали, что бактерии в буквальном смысле являются основным действующим началом в биосфере. Подавляющее большинство живых клеток на нашей планете — это именно бактерии, они демонстрируют наибольшее биохимическое разнообразие среди всех организмов и являются главной геохимической силой. Однако, несмотря на биологическую важность и поразительное биохимическое и экологическое разнообразие микробов и огромный прогресс микробиологии в середине XX столетия (в качестве примеров можно упомянуть открытие антибиотиков и демонстрацию химической природы генетического материала бактерий), микробиология ничего не внесла в СТЭ и не была эволюционной дисциплиной на протяжении большей части этого столетия. Не то чтобы микробиологи совсем не думали об эволюции, но все их попытки расшифровать эволюционные взаимоотношения между бактериями, используя морфологию клеток, а также метаболические и фенотипические характеристики, и на основе этих признаков построить филогенетическую таксономию приводили к несовместимым и неприемлемым результатам. Весьма любопытно, что приблизительно в то время, когда происходила консолидация СТЭ, ведущие микробиологии того времени, включая Роджера Стейнира и Корнелиуса Ван Нейла, пришли к выводу, что, если какие-то эволюционные процессы и происходят в микромире, описать их и как-либо применить в сфере таксономии микробов и микробиологии вообще практически невозможно (Stanier and Van Niel, 1962; Van Niel, 1955).
Как отмечено в главе 3, все резко изменилось в 1977 году, когда Карл Вёзе с сотрудниками применил филогенетический анализ рРНК как основной метод изучения эволюции микробов и создания их таксономии (Woese, 1987). Возможности новой методологии были эффектно продемонстрированы открытием архей, по-видимому, первым крупным открытием в биологии, которое было сделано исключительно на основе анализа нуклеотидных последовательностей. За этим прорывом последовал период «бури и натиска» 1980-х и начала 1990-х годов, когда филогения рРНК была успешно применена для прояснения взаимоотношений среди многих групп прокариот. Среди молекулярных эволюционистов того времени превалировало мнение, что в принципе эти методы позволят точно реконструировать эволюцию микробов.
Однако дивный новый мир микробной эволюции оказался недолговечным — эволюционная геномика вновь запутала картину самым неожиданным образом. Первый полный бактериальный геном был секвенирован в 1995 году, а первый геном археи — в 1996-м[48]. Вскоре после этого прорыва установился экспоненциальный темп секвенирования геномов со временем удвоения около 20 месяцев для бактерий и около 34 месяцев для архей (см. рис. 3-1). Сравнительный анализ сотен секвенированных бактериальных геномов и десятков геномов архей привел к важнейшему выводу: микробы определенно эволюционируют, но их эволюция сильно отличается от той, что описана СТЭ (Doolittle, 1999b; Woese and Goldenfeld, 2009). Ключевым стало осознание того, что геномы прокариот ведут себя не так, как если бы они были стабильными, точно наследуемыми носителями генетической информации организма (вида). Геномы микробов оказались чрезвычайно динамичными, неоднородными образованиями, которые относительно стабильны лишь на коротких интервалах времени, имеют свою характерную скорость распада и существуют в динамическом равновесии между различными формами жизни, которые отличаются по принципам геномной организации. В «мире прокариот» эти взаимосвязанные и постоянно взаимодействующие формы жизни включают не только бактерии и археи, но также различные плазмиды, вирусы и другие мобильные элементы. В этой новой, динамической парадигме прокариотической эволюции традиционная концепция видов с четко определенным, стабильным геномом теряет существенную, если не большую часть своей применимости (Doolittle and Zhaxybayeva, 2009). Становится осмысленнее говорить о сериях «пангеномов» на всех уровнях, от пангенома, например, Escherichia coli или любого другого «вида» бактерий или архей, до пангенома всех прокариот (Lapierre and Gogarten, 2009; Mira et al., 2010).
В главе 3 мы уже обсуждали важные аспекты структуры генетической вселенной прокариот. Она рассматривалась в основном как сложный статичный объект, то есть в терминах распределения различных существенных переменных. В этой главе мы также рассматриваем распределения, но в основном пытаемся встать на динамическую точку зрения и исследовать мир прокариот в терминах потоков генов и взаимодействия между репликонами.
Размер и общая организация бактериальных и архейных геномов
Несмотря на огромные различия в образе жизни, а также метаболической и геномной организации, бактериальные и архейные геномы демонстрируют легко различимые общие архитектурные принципы (см. обзор в гл. 3). Секвенированные бактериальные и архейные геномы охватывают два порядка величины по размерам от около 144 Кб для внутриклеточного симбионта Hodgkinia cicadicola до примерно 13 Мб для обитающей в почве бактерии Sorangium cellulosum (Koonin and Wolf, 2008b). Примечательно, что бактерии демонстрируют бимодальное распределение размеров генома[49] с пиком в районе примерно 5 Мб и дополнительным плато в районе примерно 2 Мб (см. рис. 5-1). Хотя существует много геномов промежуточного размера, это распределение предполагает существование двух в достаточной степени разделенных классов бактерий с «малым» и «большим» геномами. К этим наблюдениям нужно относиться с известной осторожностью, так как они могут быть артефактом, обусловленным предпочтительным секвенированием небольших геномов (в первую очередь бактериальных патогенов), но с ростом числа секвенированных геномов такое объяснение становится все менее удовлетворительным.
Археи демонстрируют более узкое, но также сложное распределение размеров генома от примерно 0,5 Мб у паразита/симбионта Nanoarchaeum equitans до примерно 5,5 Мб у Methanosarcina barkeri, с острым пиком в районе 2 Мб, который практически точно соответствует расположению плато бактериальных геномов малого размера, вторым небольшим пиком около 3 Мб и тяжелым хвостом, соответствующим геномам большего размера (см. рис. 5-1). При этом смещения в базе данных опять могут быть существенными, так как в настоящее время геномов архей секвенировано примерно на порядок меньше, чем геномов бактерий, так что пока может быть еще просто недостаточно данных для выявления истинной формы распределения размеров геномов. Однако более вероятно, что археи действительно являются менее разнородной группой, как будет обсуждаться далее в данном разделе.
Все очень маленькие (менее 1 Мб) геномы бактерий и архей принадлежат бактериям-паразитам и внутриклеточным симбионтам эукариот и единственной известной архее-паразиту (или симбионту) Nanoarchaeum equitans, которая живет за счет другой археи, Ignicoccus hospitalis. Таким образом, кажется все более вероятным, что минимальный размер генома свободно живущего прокариота, по крайней мере автотрофа, который не зависит от других форм жизни для добывания пищи, немного превышает 1 Мб. Текущий рекорд редукции генома среди свободно живущих клеток, около 1,3 Мб, принадлежит фотосинтезирующей морской альфа-протеобактерии Pelagibacter ubique (SAR11), которая также является наиболее распространенной из известных клеточных форм жизни на Земле (Giovannoni et al., 2005). (Связь между размером популяции и размером генома потенциально важна, мы вернемся к этому вопросу в гл. 8.)
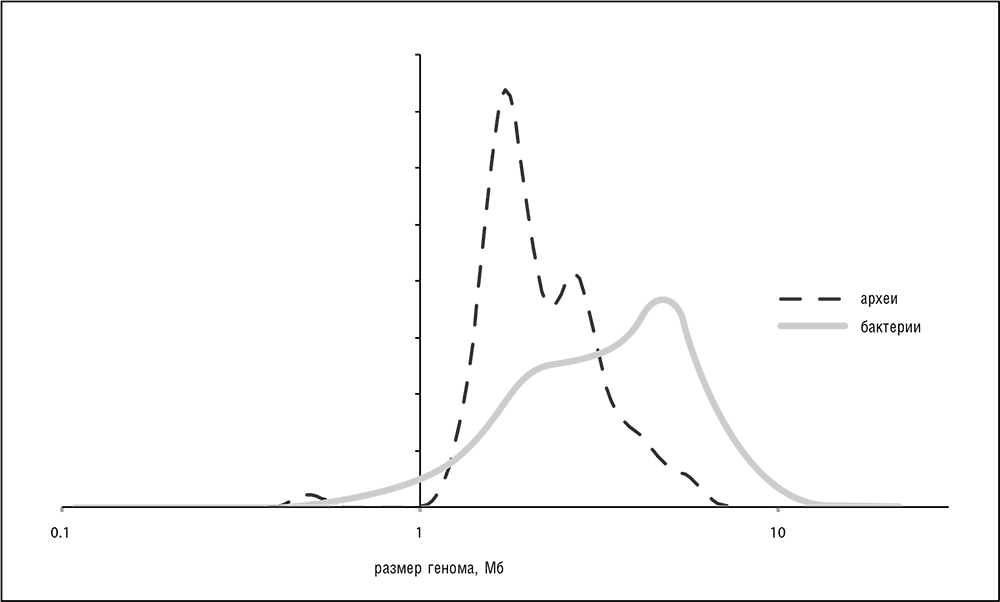
Рис. 5-1. Распределение размеров геномов среди бактерий и архей.
Как мы уже обсуждали в главе 3, бактериальные и архейные геномы характеризуются высокой плотностью белок-кодирующих генов, которые занимают большую часть ДНК. Бактериальные и архейные геномы демонстрируют одномодальное и довольно острое распределение плотности генов, большей частью 0,8–1,2 гена на Кб геномной ДНК (отсюда предельно простое эмпирическое правило: 1 ген на 1000 пар нуклеотидов). Архейное распределение по сравнению с бактериальным сдвинуто в сторону более высоких плотностей, таким образом, в среднем архейные геномы даже более компактны, чем бактериальные. Похоже, что как кодирующие, так и межгенные области у архей немного короче по сравнению с бактериями.
Таким образом, археи и бактерии весьма похожи в смысле характерных размеров и общей архитектуры геномов, но резко отличаются от эукариот, которые охватывают много больший интервал размеров генома, имеют белок-кодирующие гены, часто прерываемые интронами, и более длинные межгенные промежутки (см. гл. 8). Эти общие признаки бактерий и архей подтверждают концепцию «прокариотного принципа организации генома» (см. более подробно ниже).
Пространство-время прокариот и его эволюция
Фрактальное пространство-время генома, пангеномы и кластеризация прокариот
В главе 3 мы сосредоточились на трехкомпонентной структуре прокариотического геномного пространства, состоящего из ядра, оболочки и облака, и показали, что эта структура фрактальна. Одни и те же три компонента, а именно небольшое ядро, оболочка большего размера и огромное по сравнению с ними «облако», проявляются на любом уровне разбиения генного пространства, от мира прокариот в целом до совсем небольших групп бактерий (см. рис. 3-14). Непосредственным следствием этой фрактальности является важность «пангеномов» — всей общности генов, представляющих геномы, принадлежащие к кластеру архей или бактерий на данном уровне. Читатель может (и должен) немедленно спросить, что определяет кластеры и откуда берутся уровни. Пока предположим, что дерево рРНК Карла Вёзе (см. рис. 2-3) разумно описывает организацию пространства-времени мира прокариот и является по крайней мере одним из источников для кластеризации. В главе 6 мы обсудим применимость и смысл концепции древа жизни более глубоко и покажем, что дерево рРНК, хотя ни в коем случае и не является полным представлением истории эволюции прокариот, тем не менее вполне осмысленно.
Огромное множество архейных и бактериальных генов кодируют белки, которые не имеют никакого измеримого сходства с какими-либо другими доступными последовательностями белков. Эти гены часто обозначают как одинокие рамки считывания (ОРС)[50] (Daubin and Ochman, 2004). Обычно в архейных и бактериальных геномах ОРС составляют 10–15 процентов от всех предсказанных генов. Многие ОРС — очень короткие, и некоторые из них могут быть не реальными генами, а результатом ошибочного предсказания при анализе генома (Ochman, 2002). Кроме того, высказывается предположение, что большинство ОРС, являющихся полноценными генами, произошли от генов бактериофагов и, соответственно, характеризуются высокой горизонтальной мобильностью, хотя в некоторых случаях они могут быть задействованы для клеточных функций и, соответственно, фиксируются в бактериальных и архейных геномах. Последние оценки, следующие из метагеномных исследований бактериофагов, предполагают, что разнообразие фаговых последовательностей очень велико и остается по большей части неизученным (Edwards and Rohwer, 2005). Таким образом, кажется привлекательной идея, что бо?льшая часть бактериальных и архейных ОРС произошла из этого огромного резервуара генов. В трехкомпонентной структуре вселенной прокариотических генов, с которой мы теперь знакомы, ОРС естественным образом объединяются с «облаком» редких генов, которые количественно доминируют в генном пространстве, но не в индивидуальных геномах, как обсуждалось в главе 3.
Насколько велико все геномное пространство прокариот? Сколько генов в общей сложности оно содержит? Надежная экстраполяция расширения геномного пространства в результате продолжающегося секвенирования бактериальных и архейных геномов и достоверная оценка реального размера этого пространства трудноосуществимы. Однако с учетом большого разнообразия микробных виромов, которые являются основным резервуаром генов и их переносчиком (см. также гл. 10), наиболее вероятно, что число элементов прокариотического геномного пространства увеличится на порядки величины, в основном, если не исключительно, за счет расширения «облака» (Koonin and Wolf, 2008b; Lapierre and Gogarten, 2009).
Эволюционная динамика архитектуры генома прокариот: опероны, суперопероны и сети соседствующих генов
Как уже отмечалось в главе 3, практически сразу же, как только были опубликованы первые полные геномные последовательности, стало очевидным, что последовательность генов в бактериальных и архейных геномах относительно мало консервативна, она сохраняется существенно хуже, чем последовательность нуклеотидов в самих генах (см. рис. 3-6). Для того чтобы анализировать эволюцию последовательности генов, необходимо иметь надежный набор ортологичных генов в сравниваемых геномах (см. табл. 3-1). Как только такое множество ортологичных генов задано, становится достаточно просто оценить степень сохранения последовательности генов, например с помощью точечного графика (одно из самых ранних представлений степени сходства нуклеотидных и белковых последовательностей), в котором каждая точка представляет собой пару ортологов. Исследование этих графиков показывает быстрое расхождение порядка генов у прокариот таким образом, что даже между близкородственными организмами коллинеарность хромосом разрушена в нескольких точках (см. рис. 5-2а), a умеренно разошедшиеся организмы показывают лишь несколько протяженных коллинеарных районов (см. рис. 5-2б и 5-2в). Для любой пары более отдаленных друг от друга организмов график выглядит как карта звездного неба (см. рис. 5-2г). Разрушение синтении в процессе эволюции бактериальных и архейных геномов обычно явно бросается в глаза на графике, образуя картину в форме буквы X (см. рис. 5-2б и 5-2в). В свое время было сделано предположение, что такая картина возникает в результате симметричных хромосомных инверсий с центром в точке начала репликации (Eisen et al., 2000). Исходной причиной таких инверсий может быть высокая частота рекомбинаций в репликационных вилках, которые в кольцевых хромосомах бактерий и архей обычно располагаются с обеих сторон и на одинаковом расстоянии от точки начала репликации.

Рис. 5-2. Расхождение порядка следования генов между геномами бактерий: а — Borrelia afzelii PKo по сравнению с Borrelia burgdorferi B31; б — Shewanella oneidensis MR-1 по сравнению с Shewanella sp. ANA-3; в — Pseudomonas fluorescens PfO-1 по сравнению с Pseudomonas fluorescens Pf-5; г — Pseudomonas fluorescens Pf-5 по сравнению с Pseudomonas syringae pv. tomato str. DC3000. Каждая точка представляет пару ортологичных генов, идентифицированных с использованием метода наилучшего сходства при двунаправленном сравнении (см. табл. 3-1). Яркие точки показывают пары ортологичных генов, принадлежащих консервативным массивам генов; бледные точки показывают изолированные ортологи. DY — расстояние между сравниваемыми геномами в терминах порядка следования генов, как описано в Novichkov et al., 2009. DN — медианное расстояние между последовательностями несинонимических сайтов в белок-кодирующих генах.
Одной из наиболее ранних фундаментальных концепций бактериальной генетики является оперон, то есть группа совместно транскрибируемых и регулируемых генов (Jacob and Monod, 1961). Гипотеза оперона — выдающийся концептуальный прорыв Франсуа Жакоба и Жака Моно. Хотя за 50 лет, прошедших с момента ее первой публикации, было открыто огромное количество вариаций простой схемы регуляции лактозного оперона Lac репрессором, оперон выдержал проверку сравнительной геномикой как главный организационный принцип бактериальных и архейных геномов. В процессе эволюции опероны сохраняются гораздо лучше, чем протяженные синтении. Тем не менее сравнительный анализ порядка следования генов в бактериях и археях выявил небольшое количество оперонов, общих для широкого многообразия организмов. Как уже было отмечено ранее, высококонсервативные опероны, как правило, кодируют физически взаимодействующие белки, тенденция, легко объяснимая отбором, направленным против вредных эффектов дисбаланса между субъединицами сложных белковых комплексов. Наиболее эффектной иллюстрацией этой тенденции является рибосомный супероперон, включающий более 50 генов рибосомных белков, который встречается в различных комбинациях и локализациях во всех секвенированных архейных и бактериальных геномах. Анализ рибосомного супероперона и других частично сохраняющихся групп оперонов меньшего размера привел к идее сверхоперона (Lathe et al., 2000), или консервативного окружения гена (Rogozin et al., 2002), как некоего множества перекрывающихся, частично консервативных цепочек генов (известных или предсказанных оперонов; см. рис. 5-3). В дополнение к рибосомному супероперону, яркими примерами консервативного окружения являются предсказанная группа перекрывающихся оперонов, которая кодирует субъединицы экзосомного комплекса архей, и cas-гены, из которых состоит антивирусная система защиты (см. также гл. 9 и 10).
Большинство генов в каждом консервативном окружении кодируют белки, вовлеченные в один и тот же процесс или комплекс, но существуют и высококонсервативные участки, которые включают гены с функциями, как кажется, несвязанными. Яркий пример — частое присутствие гена енолазы в рибосомном окружении или генов субъединиц протеасомы в экзосомном окружении архей. Присутствие этих генов, на первый взгляд кажущихся неуместными в консервативном генном окружении, может объясняться скрытой функциональной связью, плейотропией (множественностью функций соответствующих белков), или «геномным автостопом», когда оперон объединяет гены функционально не связанные, но экспрессируемые в одинаковых условиях (Rogozin et al., 2002).
Концепция геномного окружения воплощает в себе парадигму эволюции генома прокариот, если не эволюции геномов вообще, так как она ярко демонстрирует баланс между частичным сохранением элементов ядра и огромной диверсификацией периферии (см. рис. 5-3а). Так же как для многих других объектов и их взаимоотношений в биологии, эти частично консервативные окружения могут быть естественным образом представлены в виде сети, в которой гены являются узлами, соседи соединены ребрами, а вес ребер пропорционален частоте встречаемости данной связи в геномах (см. рис. 5-3).
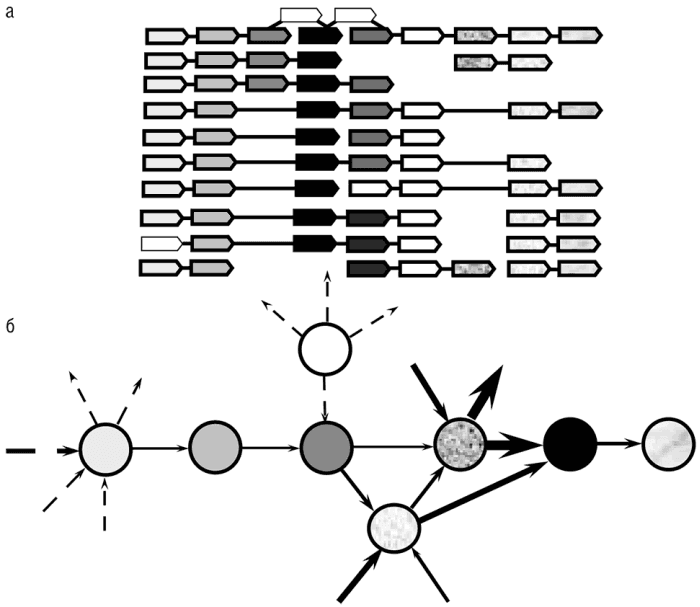
Рис. 5-3. Частично сохраняющееся окружение гена в геноме прокариот: а — перекрывающиеся, частично сохраняющиеся массивы генов. Гены показаны в форме стрелок с уникальной штриховкой или текстурой. Связывающие их жирные линии обозначают короткие межгенные промежутки, а тонкие линии показывают протяженные районы, разделяющие соответствующие гены. (Они содержат дополнительные гены и изображены без учета масштаба.) В случаях, в которых опероны не связаны, они могут располагаться в различных частях генома. На рисунке показаны реальные массивы генов, но названия конкретных геномов и генов не указаны, чтобы подчеркнуть общий характер геномной организации подобного типа. Данные по Rogozin et al., 2002; б — представление окружения гена в виде сети. Закрашенные окружности показывают гены, которые принадлежат к окружению, автоматически вычлененному с использованием алгоритма, описанного в Rogozin et al., 2002; показана только часть окружения. Незакрашенная окружность соответствует гену, который принадлежит окружению, но не был включен в него автоматической процедурой. Стрелки показывают связь между генами в оперонах (жирные стрелки соответствуют связям внутри окружения, а пунктирные стрелки — внешним связям). Толщина стрелок примерно пропорциональна числу геномов, в которых представлена данная пара генов.
Большинство оперонов находится не в сложном окружении, включающем разнообразные связи, а представляет собой простую последовательность от двух до четырех генов, порядок которых может различаться. Идентичные или похожие в смысле организации генов опероны часто обнаруживаются в сильно различающихся организмах и в различных функциональных системах. Примечательны в данном случае многочисленные опероны транспорта метаболитов, которые состоят из расположенных в одинаковом порядке генов, кодирующих трансмембранные пермеазы, АТФазы и периплазматические субъединицы так называемых ABC-транспортеров (три субъединицы обозначаются соответственно A, B и C). Присутствие таких общих оперонов в разнообразных бактериях и археях было интерпретировано в рамках гипотезы эгоистичного оперона (Lawrence, 1999), которая постулирует, что оперон так хорошо сохраняется не из-за функциональной важности совместной регуляции входящих в него генов, а из-за «эгоистичности» этой компактной генетической единицы, которая склонна к горизонтальному распространению среди прокариот (ниже в этой главе мы еще вернемся к данной концепции при обсуждении горизонтального переноса генов).
Систематическое сравнение расположения ортологичных генов в архейных и бактериальных геномах выявило относительно небольшую долю сохраняющихся (предсказанных) оперонов и гораздо большую распространенность уникальных директонов (последовательностей генов, считываемых в одинаковом направлении и разделенных короткими межгенными участками; Wolf et al., 2001). Как было показано, возможно несколько неожиданно, директоны довольно точно предсказывают опероны: большинство директонов в действительности, по-видимому, являются оперонами (Salgado et al., 2000). Таким образом, архейные и бактериальные геномы сформированы на оперонных принципах с небольшим числом высококонсервативных оперонов и намного более многочисленными редкими и уникальными оперонами. С учетом этого обстоятельства модель консервации оперонов, по крайней мере качественно, напоминает распределение кластеров ортологичных генов, с его трехкомпонентной структурой (см. выше): редкие гены и редкие опероны гораздо более многочисленны, чем повсеместно распространенные гены и опероны.
Степень «оперонизации» генома у бактерий и архей широко варьирует: некоторые геномы, например как у гипертермофильной бактерии Thermotoga maritima, почти полностью состоят из (предсказанных) оперонов, в то время как другие, как у большинства цианобактерий, по-видимому, содержат очень немного оперонов. Остается неясным, что определяет распространенность оперонов в организме, хотя высказывались предположения, что степень «оперонизации» зависит от баланса между интенсивностью рекомбинации и горизонтального потока генов, а также факторов отбора, препятствующих разрушению оперонов.
Регуляция экспрессии генов и передачи сигналов у бактерий и архей: от базовой схемы оперона к сверхоперонам, регулонам и сложным сетям
Бактерии и археи обладают сложной и элегантной системой регуляции экспрессии генов. Сравнительная геномика драматически изменила существующие взгляды на принципы организации, распределение в природе и эволюцию этих регуляторных механизмов. Концепция оперона Жакоба и Моно, представленная в предыдущем разделе как основной принцип локальной архитектуры бактериальных и архейных геномов, также является концепцией регуляции экспрессии генов и передачи сигналов у прокариот. В модели Жакоба—Моно регулятор (репрессор лактозы в их оригинальной работе) является сенсором внеклеточных и внутриклеточных сигналов (в данном случае концентрации лактозы), что влияет на структуру белка-регулятора и, опосредованно, на экспрессию оперона (в случае лактозного оперона репрессор, связывая лактозу, отсоединяется от регуляторной части оперона, делая тем самым возможной транскрипцию). В течение полувека, прошедших с момента фундаментального открытия Жакоба—Моно, было обнаружено множество вариаций этой темы, включая регуляторы, которые симметрично влияют на транскрипцию разных расположенных по соседству генов, и глобальные регуляторы, которые контролируют экспрессию многочисленных разрозненных генов и оперонов, в противоположность репрессору простого оперона в модели Жакоба—Моно. Наиболее заметными глобальными регуляторами являются белки — подавители катаболизма (CRP) и регулятор ответа на стресс (SOS) LexA. С учетом открытия этих и других глобальных регуляторов концепция оперона была усовершенствована понятием регулона — набора генов, экспрессия которых регулируется одним и тем же белком-регулятором. Сравнительный геномный анализ регулонов выявил их чрезвычайную эволюционную пластичность с существенными различиями между регулонами даже у близкородственных организмов (Lozada-Chavez et al., 2006). Глобальные регуляторы транскрипции, такие как LexA, широко распространены и высококонсервативны в различных бактериях, но состав генов в регулоне LexA является очень вариативным. Пластичность регулонов, наряду с изменчивостью архитектуры генома (см. выше), хорошо согласуется с идеей, что регуляция экспрессии генов и архитектура генома в эволюции архей и бактерий тесно взаимосвязаны. В резком контрасте с изменчивостью и пластичностью регулонов, регуляторы транскрипции у бактерий и архей демонстрируют примечательное единство архитектуры и структуры. Как правило, эти регуляторы содержат домен, связывающий небольшие молекулы-сенсоры и ДНК-связывающий домен. Подавляющее большинство ДНК-связывающих доменов являются вариациями одной и той же структурной темы, спираль — поворот — спираль. Более специфические, но тоже распространенные домены связывания с ДНК включают мотивы лента — спираль — спираль и цинковая лента (Aravind et al., 2005; Aravind and Koonin, 1999).
Более сложная схема передачи сигналов и регуляции экспрессии генов, которая процессирует сигналы, приходящие из окружающей среды, основана на так называемых двухкомпонентных системах (Casino et al., 2010). Двухкомпонентные системы состоят из мембранных гистидин-киназ и растворимых регуляторов ответа, между которыми сигнал передается путем переноса фосфата. Примечательно, что классические регуляторы транскрипции и гистидин-киназы содержат много общих сенсорных доменов. Это родство указывает на то, что регуляторы транскрипции (однокомпонентные системы) и двухкомпонентные системы образуют единую, интегрированную структуру передачи сигналов и регуляции экспрессии. Однокомпонентные системы, которые распространены практически повсеместно и, как правило, численно доминируют у бактерий и архей, предположительно являются наиболее древними устройствами передачи сигналов, в то время как двухкомпонентные системы, вероятно, являются произошедшей от них более сложной формой передачи сигнала, которая эволюционировала как механизм реагирования на стимулы, приходящие из окружающей среды (Ulrich et al., 2005).
Сравнительная геномика бактерий и архей внесла решающий вклад в открытие новых, до того неизвестных, но в действительности весьма распространенных систем передачи сигналов. В течение многих лет было известно, что широко распространенная форма глобальной регуляции у бактерий использует в качестве посредника цАМФ (циклический АМФ), при участии различных аденилатциклаз (яркий пример неортологичной замены генов), многочисленных белков, содержащих сенсоры цАМФ, такие как GAF-домен, a также белки катаболитной репрессии (CRP и FNR) и другие регуляторы транскрипции, которые тоже содержат цАМФ-связывающие домены. Сравнительный анализ выявил многочисленные неклассифицированные белки, содержащие гомологичные сенсорные домены, которые типичны для цАМФ-зависимых регуляторов и двухкомпонентных систем, объединенные с одним или двумя новыми доменами, GGDEF и EAL (обозначенными так по соответствующим мотивам консервативных последовательностей аминокислот). Геномный контекст этих доменов и наблюдение, что домен GGDEF является отдаленным гомологом одного из семейств аденилатциклаз, привели к гипотезе, что эти белки являются компонентами новой системы (или систем) передачи сигналов. Впоследствии эти предсказанные системы были открыты после того, как было показано, что домен GGDEF обладает активностью ди-ГМФ-циклазы, в то время как EAL является ди-ГМФ-фосфодиэстеразой. Зависимая от ц-ди-ГМФ передача сигнала, существование которой даже не предполагалось в догеномную эру, начинает рассматриваться как главная регуляторная система бактерий и архей (Seshasayee et al., 2010).
Другая интересная тема дискуссий — широкое представительство у прокариот различных модулей сложных систем передачи сигналов, которые, как считалось ранее, характерны только для эукариот. В частности, сравнительный геномный анализ убедительно показал, что белковые серин-треонин-киназы и соответствующие фосфатазы широко распространены и диверсифицированы среди архей и бактерий и являются важным компонентом многогранной системы передачи сигналов у прокариот. Анализ большего количества бактериальных геномов неожиданно выявил гомологи белков, которые, как считалось ранее, имеются только у эукариот, где они вовлечены в известные пути передачи сигналов, такие как программируемая клеточная смерть (ПКС), или апоптоз. Эти белки включают протеазы из суперсемейства каспаз, семейство апоптозных АТФаз и семейство ГТФаз NACHT; все они вовлечены в различные формы ПКС растений и животных (Koonin and Aravind, 2002; Leipe et al., 2004). Как правило, эти белки обладают сложной мультидоменной модульной архитектурой, для которой характерно соединение каталитических доменов с разнообразными доменами, обеспечивающими специфичность белок-белковых взаимодействий. Эти предполагаемые сигнальные молекулы наиболее распространены в бактериях со сложными фазами развития, таких как цианобактерии, актинобактерии и миксобактерии, а также присутствуют у метаносарцин, единственной известной группы архей с относительно большими геномами и сложной морфологией. Детальное исследование функций этих белков еще предстоит, но есть предварительные признаки того, что у некоторых бактерий они могут быть вовлечены в ПКС (Bidle and Falkowski, 2004). Эти наблюдения показывают, что по крайней мере для некоторых из сложных сигнальных систем эукариот существуют аналоги и вероятные эволюционные предшественники среди бактерий. Мы еще вернемся к этим связям, когда будем обсуждать в главе 7 происхождение эукариот.
Наряду с вышеупомянутой приблизительно квадратичной зависимостью от размера генома сравнительный геномный анализ выявил огромную вариацию в сложности систем передачи сигналов среди бактерий и архей. Эта изменчивость, по-видимому, отражает разнообразие стилей жизни среди соответствующих организмов. Вариации в доле генов, ответственных за передачу сигналов, были количественно отражены в «бактериальном IQ», показателе, который пропорционален квадратному корню от числа белков передачи сигналов (учитывая квадратичное масштабирование) и обратно пропорционален общему количеству генов (Galperin, 2005). IQ отражает способность бактерий и архей отвечать на различные стимулы, приходящие из внешней среды. Соответственно, внутриклеточные симбионты (паразиты) имеют наименьшие значения IQ. Он лишь ненамного выше у организмов с компактными геномами, живущих в стабильной внешней середе, таких как морские цианобактерии, и существенно больше у организмов, живущих в сложной и переменчивой среде, даже у тех, которые обладают сравнительно небольшими геномами.
Горизонтальный перенос генов — определяющий процесс в эволюции прокариот
Повсеместное распространение ГПГ в мире прокариот
Вездесущесть и огромную важность горизонтального переноса генов (ГПГ) в эволюции архей и бактерий можно рассматривать как самую большую новость, выявленную с помощью сравнительного геномного анализа прокариот. Никакое другое открытие не было причиной такого большого количества споров и (порою желчных) дебатов, в которых сталкивались прямо противоположные точки зрения на ГПГ, от утверждений о его повсеместном распространении и всеобъемлющей роли в эволюции бактерий и архей до отрицания любого значимого вклада ГПГ в эволюцию (Gogarten and Townsend, 2005; Kurland et al., 2003; O’Malley and Boucher, 2005). Существование ГПГ, переноса генов между неродственными организмами иным путем, нежели посредством вертикальной передачи реплицированной хромосомы в процессе деления клетки, было осознано задолго до того, как был секвенирован первый геном (Syvanen, 1994). Более того, стало понятно, что ГПГ может происходить исключительно быстро и эффективно — во всяком случае, под давлением отбора, как в случае распространения устойчивости к антибиотикам в популяции патогенных бактерий. Однако, до того как появилась возможность сравнения множества полных геномных последовательностей, ГПГ по молчаливому соглашению рассматривался как маргинальный феномен, возможно важный для таких специфических областей, как эволюция сопротивляемости инфекциям, но по большей части не принимавшийся во внимание при изучении эволюции организмов. Как читатель, вероятно, помнит, сама важность вопроса о роли ГПГ в эволюции была осознана в связи с другим революционным открытием: демонстрацией Вёзе и соавторами того, что филогенетический анализ рРНК прокариот реально возможен и может быть потенциально использован для описания эволюции бактерий и недавно открытых архей. Для большинства биологов трехдоменное эволюционное дерево рРНК, полученное Вёзе, стало синонимом гипотетического древа жизни (ДЖ), исходно постулированного Дарвином, a теперь реально полученного и готового для использования в качестве основы для картирования эволюционных событий всевозможного рода (Pace, 2006). Такова была парадигма, когда сравнительная геномика вызвала революцию, связанную с осознанием роли ГПГ.
Исторически и методологически проблема идентификации актов ГПГ и его влияния на эволюцию бактерий и архей резко различается для случаев (сравнительно) недавних и древних переносов, с одной стороны, и переносов между близкородственными и давно разошедшимися организмами, с другой стороны (Koonin et al., 2001a). Недавние случаи ГПГ, особенно между близкородственными организмами, широко распространены, бесспорны и легко обнаруживаются. Действительно, сравнение геномов бактериальных штаммов предоставляет отчетливые свидетельства большого количества актов ГПГ. Вероятно, наиболее характерным примером является открытие так называемых островов патогенности — генных кластеров, которые несут информацию, типичную для патогенов, подобную той, что содержится в генах, кодирующих различные токсины, компоненты секреторной системы третьего типа и другие подобные системы у бактерий-паразитов, а также похожие «симбиотические острова» у бактерий-симбионтов. Острова патогенности представляют собой протяженные районы генома размером до 100 Кб, которые обычно расположены недалеко от генов тРНК и содержат множество генетического материала профагов, откуда напрашивается предположение, что вставка этих островов в геном была осуществлена при посредничестве бактериофагов (Juhas et al., 2009). Ставший классическим сравнительный геномный анализ энтерогеморрагического штамма O157:H7 и лабораторного штамма K12 бактерии E. coli показал, что патогенный штамм содержит 1,387 дополнительного гена, распределенного между несколькими специфичными для штамма кластерами (островами патогенности), сильно различающимися по размерам. Таким образом, до 30 процентов генов у патогенных штаммов, по-видимому, были приобретены посредством недавнего ГПГ (Perna et al., 2001). Последующий детальный анализ индивидуальных линий O157:H7 показал, что процесс ГПГ непрерывно продолжается, внося свой вклад в различие степени вирулентности этих штаммов (Zhang et al., 2007). Воздействие недавнего ГПГ определенно не ограничивается патогенетическими эффектами. Большинство недавних (случившихся, по оценкам, в течение последних 100 миллионов лет) добавлений в метаболическую сеть E. coli явно были вызваны ГПГ, часто включающим опероны, кодирующие два и более фермента или белка-переносчика одного и того же метаболического пути. Вклад дупликации генов в метаболические инновации оказался в количественном плане существенно менее важным.
Многочисленные исследования выявили фундаментальный вклад ГПГ в эволюцию конкретных функциональных систем прокариот. Возможно, наиболее впечатляющие результаты были получены для кластера генов фотосинтеза цианобактерий и других фотосинтезирующих бактерий (Raymond et al., 2002). Филогенетический анализ уверенно показывает, что эти кластеры представляют собой сложную мозаику генов, собранных посредством множественных актов ГПГ. Попросту говоря, кислородный фотосинтез, который сформировал нынешнюю атмосферу Земли, вероятно, появился благодаря ГПГ (Mulkidjanian et al., 2006). К тому же большинство цианофагов несут один или более ген фотосинтеза, предположительно используя их для усиления фотосинтетической активности инфицированных клеток. Таким образом, бактериофаги фактически являются переносчиками генов фотосинтеза при ГПГ (Lindell et al., 2005).
Особенно важным представляется открытие агентов переноса генов (АПГ) в нескольких группах бактерий и архей. АПГ являются дефектными производными от хвостатых бактериофагов, которые упаковывают и переносят случайные фрагменты хромосомы (не являющиеся генами профагов, кодирующими капсид и аппарат упаковки) между прокариотами (Paul, 2008). В прямых экспериментах с сообществами морских микроорганизмов было показано, что АПГ переносят гены необычайно эффективно и малоизбирательно по отношению к реципиенту (McDaniel et al., 2010). Таким образом, как это ни поразительно, АПГ вполне правомочно можно рассматривать как специализированные средства перемещения генов путем ГПГ, которые, вероятно, вносят важный вклад в потоки генов в мире прокариот. Мы вернемся к роли вирусов и АПГ в ГПГ и эволюции геномов в целом в главе 10.
Кроме непосредственной экспериментальной проверки и сравнения геномов, недавний ГПГ определяется посредством анализа состава нуклеотидов, частот олигонуклеотидных последовательностей, частоты использования тех или иных кодонов и других «лингвистических» признаков нуклеотидных последовательностей, которые обнаруживают приобретение генов в горизонтальном направлении в виде композиционных аномалий данного генома. Однако перенесенные горизонтально последовательности относительно быстро изменяются, так как приобретенные гены «одомашниваются» в процессе эволюции, так что перенесенные гены в геноме-реципиенте скоро становятся «лингвистически» неразличимы (Ragan, 2001). Важно отметить, что молекулярные механизмы ГПГ между близкородственными организмами хорошо понятны (если не сказать полностью понятны) и включают конъюгацию, перенос бактериофагами (трансдукцию) и трансформацию (Bushman, 2001).
В отличие от четко установленных недавних случаев ГПГ, особенно между компактными группами родственных организмов, обобщение явления ГПГ на большие эволюционные расстояния, особенно в отдаленном прошлом, их механизмы и влияние на эволюцию архей и бактерий остаются предметом жарких споров (Gogarten and Townsend, 2005; Kurland et al., 2003)[51]. Сравнительная геномика предоставила достаточно свидетельств вероятного ГПГ, включая перенос между очень отдаленными организмами, в частности археями и бактериями. Первым явным свидетельством массивного ГПГ между археями и бактериями было обнаружение того, что гипертермофильные бактерии (конкретно Aquifex aeolicus и Thermotoga maritima) содержат намного больше гомологов белков, характерных для архей, чем мезофильные бактерии, а также белки, имеющие гомологи как среди архей, так и среди бактерий, но с аминокислотными последовательностями, существенно больше похожими на архейные гомологи, чем на бактериальные (см. рис. 5-4)[52]. Сравнение с мезофильными бактериями показало, что доля «архейных» белков у бактерий-гипертермофилов была намного больше (причем с высокой статистической значимостью), чем у мезофилов (Aravind et al., 1998; Nelson et al., 1999). Впоследствии было продемонстрировано, что мезофильные археи с относительно большим геномом, Methanosarcina и галобактерии, обладают намного большим количеством «бактериальных» генов, чем термофильные археи с небольшими геномами (см. рис. 5-4; Deppenmeier et al., 2002). Это обстоятельство позволяет грубо оценить долю генов, которые могли быть приобретены археями и бактериями в местах их совместного обитания за счет ГПГ между ними, по крайней мере в 20 процентов.
Несмотря на эти замечательные открытия, ГПГ между эволюционно далекими прокариотами остается предметом дебатов, и все имеющиеся к настоящему времени свидетельства часто (иногда жестко) критикуются (Kurland, 2005; Kurland et al., 2003). Таксономический анализ результатов сравнения последовательностей большого числа геномов дает серьезные аргументы в пользу предполагаемого ГПГ, особенно если учесть, что для прокариот с различными стилями жизни получаются сильно разнящиеся результаты (см. рис. 5-4). И все же эти свидетельства не «доказывают» ГПГ, и в свое время были предложены иные объяснения (не всегда правдоподобные), такие как конвергенция белковых последовательностей удаленных организмов, которые живут в похожих условиях среды обитания (например, гипертермофильные археи и бактерии). Так или иначе, в течение первой декады третьего тысячелетия многочисленные филогеномные исследования — анализ филогенетических деревьев для всех (или почти всех) генов прокариот, которые являются в достаточной степени консервативными и, таким образом, содержат достаточно филогенетической информации для надежных выводов, выявили обширный перенос генов между хорошо известными группами архей и бактерий, включающий даже перенос генов между царствами (Beiko and Hamilton, 2006; Puigbo et al., 2009; Sicheritz-Ponten and Andersson, 2001). Кроме того, эти исследования продемонстрировали существование «скоростных магистралей» (highways), предпочтительных путей для потока генов (Beiko et al., 2005). Широкие магистрали связывают, в частности, различные термофильные организмы (см. также гл. 6).
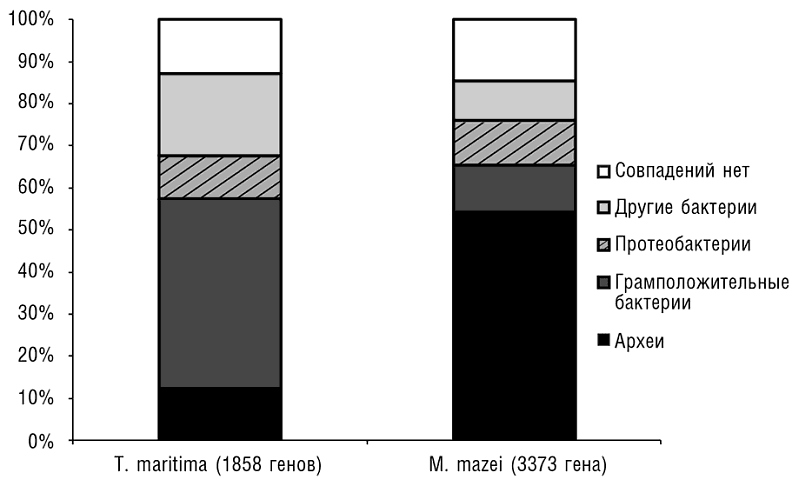
Рис 5-4. Анализ генов в геномах архей и бактерий на предмет таксономической близости наиболее близких гомологов. Показаны данные для гипертермофильной бактерии Thermotoga maritima и для мезофильной археи Methanosarcina mazei. Результаты были получены программой BLASTP путем поиска аминокислотных последовательностей всех белков в каждом геноме с использованием базы данных последовательностей белков NCBI (Altschul et al., 1997).
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава XIII Регуляция экспрессии генов
Глава XIII Регуляция экспрессии генов О проблеме регуляции экспрессии генов мы в этой книге говорим фактически во всех главах, рассматривая ее с разных сторон. Существует такое, может быть несколько одностороннее, определение развития: «Понять развитие — это значит
Глава 2. Потоки энергии и «самоорганизация» структур
Глава 2. Потоки энергии и «самоорганизация» структур Все обменивается на огонь и огонь на все, как на золото — товары, на товары — золото. Гераклит Несмотря на внешнее разнообразие, для большинство процессов переноса (тепла, вещества, электричества) имеются общие
Глава 3 Сравнительная геномика: эволюционирующие геномные ландшафты
Глава 3 Сравнительная геномика: эволюционирующие геномные ландшафты Пер. А. НеизвестногоВажность перехода к геномикеВ догеномную эру были установлены фундаментальные принципы молекулярной эволюции и было сделано немало конкретных наблюдений, имеющих большое значение
Глава 4 Геномика, системная биология и универсалии эволюции: эволюция генома как феномен статистической физики
Глава 4 Геномика, системная биология и универсалии эволюции: эволюция генома как феномен статистической физики Пер. К. МуратовойВ предыдущей главе была подчеркнута относительная стабильность отдельных генов, составляющая яркий контраст динамизму геномной эволюции.
7. СТРУКТУРА И ДИНАМИКА СУБЪЕКТИВНОГО МИРА ЧЕЛОВЕКА И ЖИВОТНЫХ
7. СТРУКТУРА И ДИНАМИКА СУБЪЕКТИВНОГО МИРА ЧЕЛОВЕКА И ЖИВОТНЫХ 7.1. Историческая детерминация уровневой организации систем Представления о закономерностях развития многими авторами разрабатываются в связи с идеями уровневой организации (см. в [Анохин, 1975, 1980; Роговин, 1977;
7.4. Динамика субъективного мира как смена состояний субъекта поведения
7.4. Динамика субъективного мира как смена состояний субъекта поведения С этих позиций динамика субъективного мира может быть охарактеризована как смена состояний субъекта поведения в ходе развёртывания поведенческого континуума (см. рис. 14.1). Упоминавшиеся ранее
3.1. Генетический материал вирусов и прокариот
3.1. Генетический материал вирусов и прокариот Генетический материал вирусов представлен одной молекулой нуклеиновой кислоты (либо ДНК, либо РНК), окруженной защитной белковой оболочкой – капсидом. Функционирование вирусов происходит по-разному, в зависимости от их
6.6. Регуляция экспрессии генов у прокариот
6.6. Регуляция экспрессии генов у прокариот В клетках прокариот процессы транскрипции и трансляции протекают почти одновременно, поэтому весьма сложно внести какие-либо изменения в структуру синтезированной РНК. Регуляция генной активности прокариот практически
Глава 5 ДИНАМИКА ПРОЦЕССОВ ВЫСШЕЙ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ
Глава 5 ДИНАМИКА ПРОЦЕССОВ ВЫСШЕЙ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ Вся сложная и разнообразная деятельность высших отделов нервной системы построена на работе двух основных нервных процессов — возбуждения и торможения. Протекая в подвижных пространственных и временных
Глава 10 Адаптации экспрессии генов в процессе развития
Глава 10 Адаптации экспрессии генов в процессе развития Жизнь -это сила, которая проделывает бесчисленное множество экспериментов, пытаясь организовать себя ... мамонт и человек, мышь и мегатерий, мухи и отцы церкви - все это результаты более или менее успешных попыток
5.3. Горизонтальные переносы и их роль в эволюционном процессе
5.3. Горизонтальные переносы и их роль в эволюционном процессе Приведенные выше палеонтологические данные свидетельствовали, что на Земле около 3.5 млрд лет тому назад уже существовали разнообразные микроорганизмы современного типа. Это означает, что бактерии и архе
3.3. Основные потоки
3.3. Основные потоки Прежде всего рассмотрим основные потоки, поступающие из желудочно-кишечного тракта во внутреннюю среду организма.3.3.1. Поток нутриентовОбязательное условие ассимиляции пищи — разборка ее сложных структур до простых соединений, которая происходит в
3.3. Основные потоки
3.3. Основные потоки Прежде всего рассмотрим основные потоки, поступающие из желудочно-кишечного тракта во внутреннюю среду организма.3.3.1. Поток нутриентовОбязательное условие ассимиляции пищи — разборка ее сложных структур до простых соединений, которая происходит в
Глава 6 Разведение генов
Глава 6 Разведение генов Древние греки уподобляли человеческую жизнь тонкой нити, которую прядут, отмеряют и перерезают три богини – Парки. Современные биологи ищут секреты человеческой судьбы в другой нити, вернее, в двух нитях – нитях молекулы ДНК, сплетенных
Глава 6. Разведение генов
Глава 6. Разведение генов …воспитывавшихся в разных приемных семьях. Bouchard et al., 1990.…чем у изучавшихся пар людей, выбранных случайным образом. Строго говоря, корректное сравнение следует проводить с двумя представителями различных пар однояйцевых близнецов, выросших