Нейрохимическая теория, или Как работают препараты для мозга
Мы с вами выяснили, что интерпретировать нервно-психические коды с позиций современной науки пока невозможно по целому ряду причин. Сейчас мы знаем, что есть цепочки из нервных клеток, по которым бегает нервный импульс. И бесконечное множество цепочек (объединяющихся в сети) обеспечивает самые разнообразные процессы обработки информации в мозге.
Строго говоря, как такового электрического импульса (да еще, как иногда это представляют в компьютерных моделях, со светящимися или искрящимися потоками световой энергии) в нервной системе нет. Вместо этого в результате выброса нейромедиатора происходит открытие ионных каналов (пор) для заряженных частиц. Эти поры находятся в мембране нервной клетки. Через них могут перемещаться ионы натрия, калия, хлора и так далее.
На самом деле правильнее говорить о потенциале действия, а не о нервном импульсе. Потенциал действия – это такая волна возбуждения, которая перемещается по мембране нервной клетки в виде кратковременного изменения мембранного потенциала на некотором участке.
Положительно заряженных ионов натрия (Na+) в 20–30 раз больше вокруг нейрона, чем внутри него. Из-за этого наружная поверхность мембраны нейрона заряжена положительно по отношению к внутренней поверхности этой же мембраны. Но когда медиатор связывается с рецепторами, происходит открытие натриевых каналов (пор). И положительно заряженные ионы натрия (Na+) поступают внутрь нейрона. Из-за этого мембрана нервной клетки приобретает условный отрицательный заряд (ведь положительно заряженные ионы Na+ уже утекли внутрь). Причем происходит эта смена заряда не сразу на всей мембране клетки, а на каком-то небольшом ее участке.
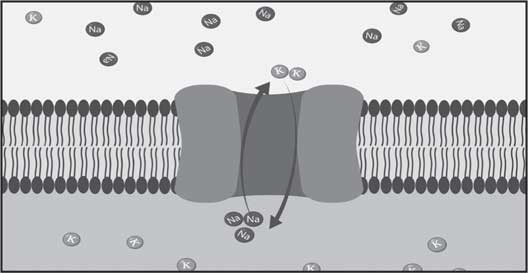
Рис. 28. Участок мембраны нейрона с ионными каналами (компьютерная модель)
И так постепенно, участок за участком, по мембране (в том числе и по длинному отростку) происходит смена заряда. Предыдущий кусочек мембраны как бы подначивает следующий участок менять заряд (как в цепной реакции). Таким образом, потенциал действия – это физиологическая основа нервного импульса.
Конечно, это очень упрощенная схема, потому что в процессе передачи импульса (возникновения потенциала действия) могут принимать участие и другие молекулярные системы.
Но в действительности, несмотря на понимание описанных выше биофизических и химических механизмов, у науки пока нет хорошо работающей модели мозга. Нужна такая модель, которая бы подробно отражала все аспекты его деятельности.
Фармакологи, медики и физиологи XX века активно искали вещества, с помощью которых можно было бы воздействовать на наше поведение. Наряду с открытием первых нейромедиаторов шел поиск препаратов, способных воздействовать на них. Так постепенно зарождалась нейрохимическая парадигма работы мозга.
Принцип воздействия нейромедиаторов на разные рецепторы
Как мы уже выяснили ранее, нейромедиаторы связываются со специфическими белковыми комплексами – рецепторами, после чего проводится нервный импульс. Причем узнавание происходит по принципу «ключ к замку», то есть лишь специфическая молекула конкретного нейромедиатора подходит определенному рецептору. Чтобы дальше понимать, как действуют нейромедиаторы, а также различные препараты, нужно всего лишь уяснить базовые принципы работы рецепторов на поверхности клеток мозга.
Существует два основных типа рецепторов. Первый тип имеет прямую связь с порами (ионными каналами) для заряженных частиц. Такой рецептор называется ионотропным. Как только медиатор связался с ним, пора открывается и частицы устремляются внутрь клетки (рис. 29).
Другой тип рецепторов называют метаботропным. Та-кие рецепторы не связаны напрямую с ионным каналом, но соединены с системой биологически активных молекул. Когда нейромедиатор связывается с таким рецептором, в клетке изменяется метаболизм.
Метаботропный рецептор, связавшись с нейромедиатором, посылает сигнал целой системе физиологически активных молекул внутри клетки. Например, это могут быть G-белки. А они уже проводят сигнал дальше, после чего происходит либо открытие, либо закрытие ионных каналов. Не нужно сейчас пытаться все это запомнить. Постарайтесь просто понять принцип действия: рецептор как бы активирует сигнальную систему, принимающую решение о том, что делать с порами (ионными каналами) клетки (рис. 30).
Обратите внимание, что обычно сигнальные системы состоят из множества молекул (они называются молекулами-посредниками). Возникает закономерный вопрос: а почему бы бабуле-природе не сделать все каналы ионотропными, чтобы не заморачиваться со всякими молекулами-посредниками?
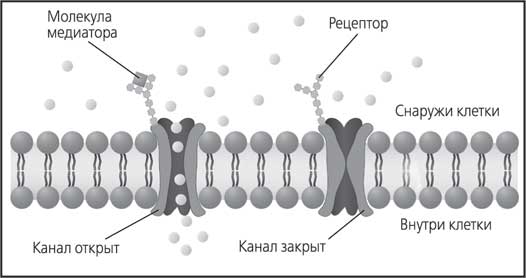
Рис. 29. Ионотропный рецептор
Предполагают, что дело тут в усилении сигнала. Одна молекула нейромедиатора, задействовав один рецептор, приводит к активации многих других молекул. Если рецепторов несколько, может быть открыто сразу множество каналов. Метаботропные рецепторы влияют на активность всей клетки, в то время как ионотропные – оказывают лишь локальное воздействие на небольшой по площади участок мембраны клетки вокруг самого рецептора. Более того, метаботропные рецепторы работают медленнее, но и эффект длится дольше.
Тормозные и возбуждающие нейромедиаторы
Стоит отметить, что физиологически нейромедиаторы бывают тормозными и возбуждающими. Из названий понятно, что одни активируют (запускают) работу систем мозга, другие, напротив, тормозят.
Если нейромедиатор связывается с рецептором и увеличивается поступление ионов Na+ и Ca2+ внутрь клетки, что приводит к возникновению потенциала действия и проведения нервного импульса, он называется возбуждающим.
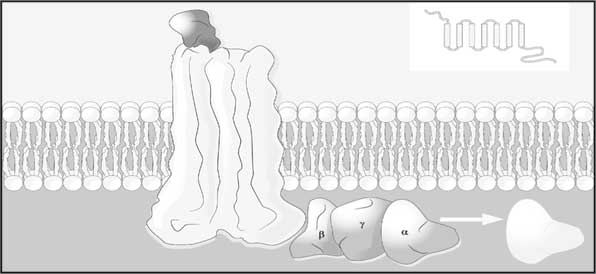
Рис. 30. Метаботропный рецептор. Изображена система молекул, которые активируются в ответ на присоединение нейромедиатора к рецептору
Если же при связывании нейромедиатора с рецептором наблюдается поступление ионов хлора (Cl-) внутрь клетки и выход ионов калия (К+) из нее, что приводит к снижению ее возбудимости, речь идет о тормозном процессе. По сути, механизм торможения или возбуждения сводится к связыванию нейромедиаторов с рецепторами и последующему открытию пор (ионных каналов) для тех или иных заряженных частиц. Как ни крути – далеко от нейромедиаторов уйти не получается.
Сами нейромедиаторы были открыты весьма любопытным образом.
В 20-е годы прошлого века биохимик Отто Леви проводил эксперименты, в ходе которых стимулировал блуждающий нерв лягушки. Это приводило к тому, что частота сокращений сердца животного замедлялась. Ученый собирал жидкость вокруг замедлившегося сердца лягушки и наносил на сердце другого животного. И оно тоже начинало замедляться! Это выглядело как настоящая фантастика.
Интересно, что параллельно с Леви это же вещество обнаружил американский физиолог Генри Дейл. Удивительным веществом оказался нейромедиатор ацетилхолин. Именно он выделяется в нервно-мышечном синапсе (контакте между нервным окончанием и мышцей).
За это открытие оба исследователя получили в 1936 году Нобелевскую премию. Так началась история нейрохимической теории мозга.
Именно в рамках этой концепции и было принято считать все нейроны, работающие с тем или иным нейромедиатором, отдельными системами. Ацетилхолиновая система достаточно обширно представлена в мозге. Иногда ее еще называют холинергической системой.
Ацетилхолин
На первом этаже (в стволе мозга) находятся нервные клетки, которые синтезируют ацетилхолин, а затем по отросткам отправляют его в структуры второго этажа (базальные ганглии). В этих структурах есть свои нейроны, выделяющие ацетилхолин. Их отростки густо расходятся по коре мозга, а также отправляются в гиппокамп (структуру, связанную с памятью).
Внутри ацетилхолиновой системы обнаружено два вида рецепторов: мускариновые и никотиновые. Мускариновые рецепторы являются метаботропными, а никотиновые – ионотропными. Сами рецепторы распределены в мозге неравномерно. Например, в среднем и продолговатом мозге представлены преимущественно мускариновые рецепторы, тогда как в гиппокампе и коре встречаются оба вида.
Обратите внимание, что никотиновые рецепто-ры являются ионотропными, а значит – быстрыми. Как вы можете догадаться, они реагируют на воздействие табака, содержащего никотин. Подробнее о том, как курение влияет на память и внимание, мы поговорим во второй части книги.
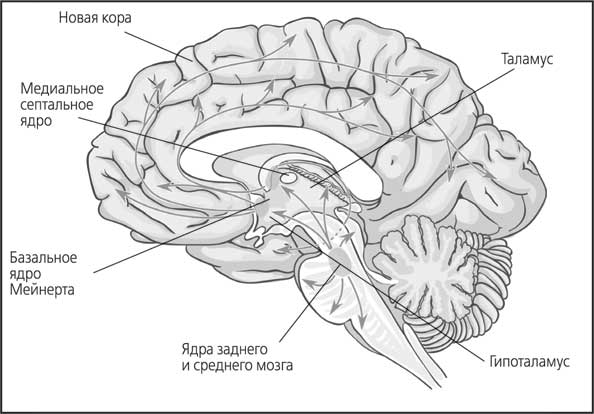
Рис. 31. Строение ацетилхолиновой (холинергической) системы
Работа ацетилхолиновой системы связана с таким явлением, как синаптическая пластичность. Это способность контактов (шипиков) изменять свою архитектуру во время обучения. Для запоминания новой информации необходимо создание синапсов или их перестройка.
Аксоны ацетилхолиновой системы способны помогать клеткам, использующим другие нейромедиаторы, проводить нервные импульсы. Так ацетилхолиновые нейроны открывают дополнительные ионные каналы на клетках гиппокампа, помогая последним передавать сигнал на следующий нейрон. Полагают, что это облегчает запоминание новой информации.
В исследованиях 2000-х годов было показано, что ацетилхолин играет важную роль в обеспечении процессов внимания. Причем особенно активно в работу включаются никотиновые рецепторы. Они быстрые, и за счет этого мы можем с большой скоростью переключать внимание с одного объекта на другой. Удалось доказать, что нарушение глубоких структур (первого этажа) ацетилхолиновой системы ухудшает работу некоторых отделов лобных долей, что ведет к снижению внимания.
Логично предположить, что раз ацетилхолиновая система обеспечивает внимание (пусть даже и частично), неплохо было бы ее простимулировать.
А теперь маленькое отступление. Мы с вами уже познакомились с принципами работы синапсов и поняли, что без молекул нейромедиатора никуда.
Почти все препараты, воздействующие на нервную систему, идут по одному из двух путей:
1. Напрямую воздействуют на рецептор и запускают процесс передачи импульса или же, напротив, блокируют сам рецептор, предотвращая передачу.
2. Увеличивают количество нейромедиатора в щели, чтобы он сам активировал рецепторы и запускал передачу импульса.
Вот и вся магия. В первом случае молекулы вещества (препарата или наркотика) имитируют нейромедиатор (потому что имеют химическую конфигурацию, похожую на него) и работают по принципу «ключ к замку».
Если надо заблокировать рецептор, молекула препарата обычно имеет в составе участок, способный связываться с ним. Так молекула садится на рецептор, не позволяя ему связываться с нейромедиатором. При этом передачи нервного импульса не происходит.
Во втором случае препараты воздействуют на системы клеток так, чтобы нейромедиатор накапливался в щели. К примеру, они могут подавлять действие фермента, разрушающего нейромедиатор. Либо блокируется захват нейромедиатора из щели. Такое втягивание молекул нейромедиатора (в пресинаптическую мембрану) называют обратным захватом. Бабуля-природа, вообще, экономичная старушка. Нет смысла многократно синтезировать молекулы, если можно обратно захватить те, что остались в щели.
То есть мы подавляем процесс обратного захвата, что позволяет нейромедиатору накапливаться в щели. В разных ситуациях могут быть свои особенности, но базовые принципы одни и те же.
В случае с ацетилхолиновыми препаратами применяются ингибиторы (подавители работы) ацетилхолинэстеразы – фермента, разрушающего нейромедиатор ацетилхолин прямо в синаптической щели. Как вы понимаете, это приводит к увеличению количества медиатора в щели и улучшению передачи сигнала между клетками.
К препаратам, воздействующим на ацетилхолинэстеразу, относят галантамин и ривастигмин. Есть данные, что эти препараты также способны уменьшить выраженность симптомов болезни Альцгеймера.
Важно понимать, что ацетилхолиновые рецепторы встречаются не только в мозге. Ацетилхолин – это ключевой нейромедиатор нервно-мышечной передачи. Именно с его помощью мышца получает сигнал о том, что надо бы поработать. Поэтому ацетилхолиновые рецепторы есть во всех мышечных органах (в том числе – в желудке и сердце). Ацетилхолин может оказывать серьезное влияние на сердечный ритм.
Поэтому воздействие препаратами на ацетилхолиновую систему должно проводиться крайне осторожно, под контролем специалистов.
Справедливости ради нужно заметить, что есть и пре-параты, блокирующие работу ацетилхолиновых рецепторов. Атропин связывается с рецепторами и делает их нечувствительными к ацетилхолину. Введение атропина приводит к увеличению частоты сердечных сокращений, расширению зрачков. То есть атропин выключает из работы ту часть нервной системы, которая работает на ацетилхолине. Например, в случае с сердцем блокируется тормозящее действие со стороны блуждающего нерва и поэтому сердечная мышца сокращается чаще.
Как мы видим, вполне себе механистично-физиологический эффект. Выключили тормоз – заработало быстрее.
В научной литературе вещества, оказывающие возбуждающее воздействие на мускариновые рецепторы, называют М-холиномиметиками, а препараты, подавляющие их работу, – М-холиноблокаторами.
Нет возможности в одной книге рассказать обо всех свойствах этих препаратов, поэтому предлагаю вам самостоятельно поискать информацию о них. Вы увидите, что они имеют широчайший спектр применения в самых разных областях медицины, начиная с подбора очков и заканчивая лечением насморка.
Дофамин
Очень часто в популярной литературе дофамин называют гормоном счастья. Но с точки зрения нейробиологии это не так. Исследователи до сих пор не обнаружили никаких гормонов счастья.
Мозг не был придуман для бесконечного счастья и ощущения удовлетворения. Напротив, природа постоянно преподносила нашим предкам «сюрпризы» в виде стихийных происшествий, опасных хищников, засух, безводья и так далее.
Как мы сумели понять, нейромедиаторы выполняют определенную физиологическую функцию. Так вот, главная функция нейронов, работающих на дофамине, заключается в создании определенного состояния, характеризующегося возбуждением, приливом энергии.
Когда нам сообщают, что в конце месяца мы получим дополнительную премию, внутри нас как раз и возникает это самое состояние психологического подъема. Наш мозг предвосхищает удовольствие. Вспомните, как крыса в эксперименте Олдса и Милнера жала на педаль. Она ожидала поощрения. Только мы, вместо нажатия на педаль, идем работать (также ожидая поощрения, но в виде премии). Правда, в отличие от крысы, мы способны держать в голове идею о том, что поощрение будет не скоро, а лишь в конце месяца.
Понять это мы способны благодаря хорошо развитому третьему этажу мозга с новой корой. Лимбическая система второго этажа (где синтезируется дофамин) играет роль такого эмоционального генератора внутреннего драйва, мотивации. У животных на этом все и заканчивается. Животные с плохо развитой корой мозга просто бросаются вперед при виде добычи (эту мотивацию им также создает дофамин) – мы же способны проанализировать целесообразность тех или иных действий.
Кора помогает нам остановиться и не натворить глупостей. Она помогает нам вытормозить излишние желания.
К примеру, человек, страдающий диабетом, видит большой вкусный торт. Дофаминовая система на втором этаже активируется, и у человека может возникнуть ощущение предвкушения удовольствия, которое он получит от тающего во рту крема. Но кора мозга знает, что такой сладкий десерт вреден для организма. Поэтому она блокирует подобное желание, подключая по нисходящим связям еще и амигдалу, которая заставит человека испытать страх за свою жизнь. Работу коры мозга мы рассмотрим чуть позже на других наглядных примерах.
Таким образом, можно сделать вывод, что дофамин нам нужен для создания некоторого эмоционального фона. Он как бы рисует в нашем мозге цель с «яблочком», в которое нужно непременно попасть. Вспомните состояние, когда вы были уверены в выигрыше вашего лотерейного билета, или считали, что точно победите в эстафете или совсем скоро отправитесь в оплачиваемый отпуск в теплые края. Вспомните эти ощущения.
Интересно, что, если в мозге вырисовывается путь удовлетворения потребности, мы испытываем ощущение некоторого удовольствия. Это и есть работа дофаминовой системы.
По сути, мозг стремится к некоторому состоянию комфорта, расслабленности. Мы как бы бежим от дискомфорта. Если испытываем голод, появляется мотивация встать с дивана и идти искать пищу в холодильнике, а если ее там нет, отправиться за ней в магазин или заказать на дом.
Вот почему важно ставить перед собой адекватные цели. Если вы не видите пути к их достижению, то и дофамин не вырабатывается. Конечно, человек может обманываться, полагая, что цель достигнуть проще, чем оно есть на самом деле. Такой человек витает в мире иллюзий, мечтаний. Да, какое-то время у него будет вырабатываться дофамин, но только до тех пор, пока он не столкнется с реальностью мира и не встретится с непреодолимым препятствием. Тут и наступит время расплаты за весь предыдущий дофамин. Таким образом, если не научиться выстраивать реалистичные цели и ожидания, каждый провал (и снижение дофамина) будет восприниматься мозгом как глубокий кризис. А этого допускать нельзя.
Самый простой способ избежать разочарований – тщательное планирование путей достижения ваших целей. Также полезно предварительно выслушать опытных людей. Быть может, вам и не понравятся их честные советы, но, по крайней мере, это позволит вам более реалистично смотреть в будущее и готовиться к тому, что путь будет чуть извилистее, чем вы изначально полагали.
Сейчас в дофаминовой системе обнаружено пять классов рецепторов: DRD1, DRD2, DRD3, DRD4, DRD5. DRD1 и DRD5 относят к рецепторам I типа, остальные – ко II типу.
Последствия воздействия на те или иные типы рецепторов различны. Группа Этана Бромберга-Мартина предположила, что связывание с рецепторами I типа приводит к активации клеток. Если же дофамин садится на рецепторы II типа, то наблюдается, напротив, снижение активности клеток.
Давайте рассмотрим, как работают рецепторы, на простом примере. Вам предлагают выполнить некоторую ра-боту за денежное вознаграждение. Перед получением денег и во время их получения за выполненную работу у вас происходит выброс дофамина в синаптические щели. В этот же момент в работу активно включаются клетки с рецепторами I типа. Постепенно выделение дофамина сдвигается по времени не к получению денежной компенсации, а к выполнению самой работы (потому что вы предвкушаете получение поощрения). Таким образом формируется мотивация к труду.
Если же после выполненной работы вам не выплачивают деньги, уровень дофамина снижается. Но все-таки часть клеток вырабатывает дофамин, который связывается уже с рецепторами II типа.
Итак, разные типы дофаминовой системы регулируют ценность выполняемого действия. Это во многом может предопределять наши предпочтения, желания, мотивации.
Но дофамин выполняет не только мотивирующую функцию. Он также участвует в регуляции двигательной активности. Давайте коротко рассмотрим организацию работы дофаминовой системы.
Три пути дофамина
Выделяют три основные дофаминовые подсистемы, называемые чаще путями. Первый такой путь – мезолимбический – начинается в области покрышки среднего мозга и заканчивается в области лимбической системы. Условно этот путь связан с нашими желаниями, эмоциональными сиюминутными «хотелками».
Второй путь – мезокортикальный – берет начало из все той же покрышки среднего мозга, но идет дальше, в кору. Здесь уже обрабатываются эмоциональные желания более сложного уровня, связанные с мотивацией, нередко устремленной в далекое будущее.
Оба этих пути работают, чтобы сформировать правильную эмоциональную реакцию на тот или иной стимул (событие), а также создать мотивацию двигаться вперед, что-то делать.
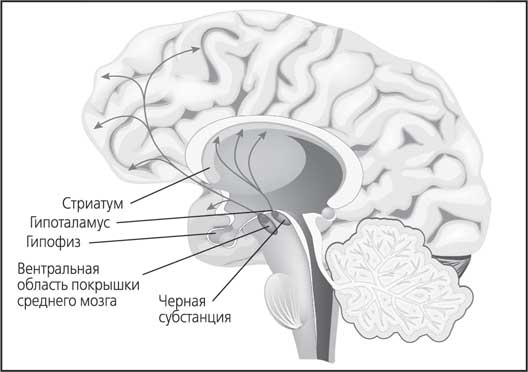
Рис. 32. Распределение различных путей дофамина в мозге
Наконец, третий путь – нигростриарный. Он достаточно короткий (рис. 32). Этот путь связывает черную субстанцию мозга с полосатым телом (стриатумом). Нигростриарный путь регулирует двигательную активность, влияя на тонус мышц.
Некоторые физиологи считают, что от того, насколько активно вырабатывается дофамин в нигростриарном пути, зависит подвижность человека. Выше я уже упоминал, что, если у человека клетки этого пути вырабатывают мало дофамина, он проявляет пассивные формы поведения.
Если же дофамина синтезируется много, у человека, напротив, наблюдается повышенная подвижность. Он получает наслаждение от движения. Все мы не раз встречали таких живчиков из разряда «физкульт-привет».
Несомненно, нельзя объяснять столь различные модели двигательного поведения лишь особенностью дофаминовой системы, поскольку есть множество других факторов. Но само по себе осознание, что наша двигательная активность зависит от уровня синтеза биохимических молекул, может заставить содрогнуться.
Только вдумайтесь, насколько сильно может быть предопределено некоторыми физиологическими факторами наше поведение.
Кстати, именно нейроны нигростриарного пути поражаются при болезни Паркинсона. У человека повышается тонус мышц и появляется характерное неконтролируемое дрожание рук.
Сегодня в арсенале врачей есть поистине волшебное вещество для лечения таких больных: леводопа – L-изомер диоксифенилаланина (L-допа). Только некоторая его часть проходит через гематоэнцефалический барьер. Но даже ее достаточно, чтобы значительно улучшить состояние многих больных. Конечно, у некоторых пациентов могут возникать побочные эффекты. Но если грамотно контролировать прием препарата, действительно наблюдаются изменения в лучшую сторону.
Есть и еще один путь дофамина – тубероинфундибулярный, который связывает дофаминовую систему с гипоталамусом. Для удобства запоминания я выделяю его в отдельную подсистему по причине того, что напрямую здесь дофамин не оказывает воздействия на поведение. Он делает это опосредованно, через гипоталамус. Поскольку гипоталамус – своеобразный химический компьютер мозга, у дофаминовой системы есть возможность влиять на работу некоторых гормонов.
Дофамин, шизофрения, антипсихотики
В настоящее время исследователи полагают, что такие симптомы шизофрении, как галлюцинации, мании преследования, бред, связаны с переизбытком дофамина в мезолимбическом пути. Другие симптомы шизофрении – утрата интереса к внешнему миру, уменьшение повседневной активности – ассоциируют с недостатком дофамина в мезокортикальном пути.
Мне бы не хотелось делать уклон в сторону медицинских аспектов. На эту тему есть масса как специальной, так и научно-популярной литературы. В этой книге и без того достаточно информации, которую нужно осознать и усвоить. Поэтому мы с вами будем касаться лишь базовых принципов работы тех или иных препаратов.
Сегодня для лечения шизофрении применяют антипсихотики, называемые также нейролептика-ми. Эти препараты блокируют дофаминовые рецепторы, не позволяя дофамину связываться с ними.
Антипсихотики бывают нескольких видов в зависимости от того, с какими рецепторами они связываются. Антипсихотики старого поколения (галоперидол, аминазин) связываются не только с дофаминовыми рецепторами, но и с серотониновыми. Они относительно эффективно убирают галлюцинации у больных шизофренией.
Антипсихотики нового поколения (рисперидон) воздействуют на мотивационную составляющую, увеличивая интерес к жизни у человека, страдающего шизофренией.
Как вы, наверное, догадались, антипсихотики способны воздействовать и на рецепторы нигростриарного пути, отвечающего за двигательную систему. Рецепторы дофаминовых нейронов блокируются, и они уже не выполняют свою функцию должным образом. В таком случае у пациентов могут наблюдаться скованность мышц, дрожание рук, то есть те же симптомы, что и при болезни Паркинсона. Итак, мы еще раз наглядно убеждаемся в верности предположения о том, что причина возникновения симптомов этой страшной болезни кроется именно в работе дофаминовой системы.
СДВГ и дофаминовая система
Дофамин так же, как и ацетилхолин, обеспечивает работу внимания – он связан с его переключаемостью. Помимо этого, дофамин позволяет человеку мотивировать себя долго концентрироваться на какой-то деятельности.
В ряде исследований авторы указывают, что нарушения в работе всех дофаминовых генов (DRD1 – DRD5) могут вызывать симптомы СДВГ (синдром дефицита внимания и гиперактивности). Это заболевание у детей и взрослых проявляется в неспособности долго удерживать концентрацию. Ребенок с СДВГ рассеян, может часто терять вещи, не способен долго поддерживать интерес к какой-то умственной деятельности. Такие дети часто выкрикивают с места, делают большое количество ошибок по невнимательности (хотя при этом зачастую обладают достаточно высоким уровнем интеллекта).
Сегодня ведутся дискуссии о том, можно ли считать СДВГ самостоятельным заболеванием. Некоторые ученые полагают, что симптомы СДВГ – это проявления разных нарушений систем, обеспечивающих познавательные функции в мозге. Другие исследователи думают, что синдром связан с засильем современных гаджетов. Возможно, злоупотребление компьютерами и смартфонами и может усугублять течение СДВГ, но я все же склоняюсь к тому, что СДВГ – самостоятельное заболевание.
На это же указывают, к примеру, данные о том, что нарушения в гене SNAP25, ответственном за работу дофаминовой системы, могут влиять на внимание и двигательную активность. То есть мы видим прямую связь между нарушением в генах, связанных с дофамином, и проявлением симптомов СДВГ.
В США и ряде других стран для коррекции симптомов СДВГ активно применяют препарат под названием «Риталин». Его действующее вещество – метилфенидат – блокирует обратный захват дофамина и норадреналина. Из-за этого активность работы определенных структур дофаминовой системы увеличивается. Как следствие, человек становится более собранным.
Но здесь важно понимать, что метилфенидат хоть и слабое, но все же наркотическое вещество, поэтому может вызывать привыкание.
Некоторые люди в США принимают «Риталин» пожизненно, и только так они ощущают себя относительно здоровыми. СДВГ действительно может катастрофически усложнять жизнь. Взрослым с СДВГ трудно выстраивать социальные взаимоотношения, строить карьеру и личную жизнь. К при-меру, они систематически опаздывают на работу, рассеянны, забывчивы.
Когда шесть лет назад я только начинал работать с детьми с СДВГ, мы с коллегами, безусловно, стремились, чтобы дети принимали как можно меньше лекарственных препаратов. Я всегда выступал за немедикаментозные методы терапии СДВГ. Хотя, конечно, есть и относительно безопасные лекарственные средства, применяемые для коррекции этого синдрома например ГАМК-препараты. Чуть ниже мы поймем, почему они не так опасны, как метилфенидат.
Для меня вопрос оправданности применения метилфенидата в коррекции СДВГ остается открытым. Мы должны крайне осторожно и взвешенно подходить к использованию-применению любого лекарственного средства, вызывающего привыкание.
Давайте коротко рассмотрим, как работают дофаминовые наркотики и почему они так коварны.
Наркотические препараты, влияющие на дофаминовую систему
Прежде чем говорить о препаратах и наркотических веществах, важно отметить, что сдвинуть хрупкий баланс в работе дофаминовой системы очень легко.
К примеру, какао воздействует на дофаминовую систему так, что у детей с СДВГ может увеличиваться подвижность, вследствие чего ухудшается усидчивость. Поэтому часто детям с СДВГ прописывают диету, исключающую шоколад и другие какаосодержащие продукты.
Особенное воздействие на дофаминовую систему оказывают психостимуляторы. Эти вещества активизируют психическую деятельность. Вообще, к наркотическим веществам можно так или иначе отнести практически все психостимуляторы (кофе, чай, табак, напитки, содержащие кофеин, и так далее).
Использование психостимуляторов поднимает ряд философских дискуссий на тему того, насколько честны достижения того или иного человека. К примеру, есть некий творческий человек, производящий какое-то количество продуктов интеллектуального труда в единицу времени. Этот человек не употребляет никакие психостимуляторы и честно работает собственным мозгом, долго и упорно. И есть другой человек, пусть даже просто постоянно пьющий кофе (и стимулирующий таким образом свой мозг), который производит в два раза больше. Насколько честны правила игры в таком случае? Можно ли говорить, что один из них более выдающийся?
Конечно, тема заслуживает отдельного разговора, но современная наука постепенно поднимает и такие неприятные вопросы. Возможно, в будущем на конкурсах работ художников, литераторов, режиссеров введут жесткие системы контроля за приемом психостимуляторов.
К более серьезным психостимуляторам относят, например, кокаин, метамфетамин, амфетамин.
Кокаин нарушает процесс обратного захвата дофамина и других нейромедиаторов. Из-за этого наблюдается их чрезмерное скопление в синаптической щели. Дофаминовая система посылает нервные импульсы, каждый раз высвобождая все больше нейромедиатора.
Если человек употребляет кокаин регулярно, постепенно количество дофамина в пресинаптической мембране уменьшается. Организм стремится компенсировать это и начинает наращивать число рецепторов на постсинаптической мембране.
Психическая зависимость от кокаина объясняется в основном неадекватной работой дофаминовой системы. Дофамина становится так мало, что приходится искать способы извне, чтобы хоть как-то почувствовать мотивацию и ощущение предстоящего удовольствия.
При регулярном употреблении кокаина (а психическая зависимость может возникнуть уже после первой дозы) со временем нарушается аппетит и нередко развивается анорексия. А затем, вместо повышенной мозговой активности, уже появляются провалы в памяти, рассеянность и другие неприятные когнитивные нарушения.
Последствия длительного приема кокаина плачевны: психозы, расстройства по типу шизофрении, нарушение репродуктивной функции, эпилепсия и так далее.
Другое наркотическое средство, метамфетамин, также оказывает психостимулирующий эффект за счет воздействия на дофаминовую систему. Метамфетамин очень хорошо проникает через ГЭБ, накапливается в мозге и действует очень длительно. У него сразу два механизма действия. Во-первых, он блокирует моноаминоксидазу – фермент, расщепляющий дофамин, серотонин и некоторые другие нейромедиаторы. Во-вторых, заставляет дофамин поступать в синаптическую щель в еще большем количестве.
Эти процессы вызывают эйфорию, усиливают стремление к творческой деятельности. Под влиянием наркотика художникам, писателям, поэтам в воображении могут являться самые необыкновенные образы.
Хотя в некоторых странах в небольших лечебных дозах метамфетамин иногда назначают в психотерапии, постоянный и бесконтрольный его прием вызывает сильную зависимость. В конечном итоге возникает так называемый абстинентный синдром, сопровождающийся нарушением сна, резкими перепадами настроения, а также появлением суицидальных мыслей. При длительном приеме может возникать расстройство личности, требующее психиатрической помощи.
К сожалению, в моем окружении есть немало очень талантливых творческих людей, которые употребляли различные наркотические вещества. Я не стесняюсь об этом писать. Я очень дорожу этими людьми, каждого из них люблю по-своему. Я потратил немало часов, рисуя им схемки работы синапсов, объясняя, как наркотические вещества самых разных классов убивают нейромедиаторные системы. Временами они злились на меня, сильно раздражались, даже срывались и кричали. Мягко, но настойчиво я вкладывал им в голову необходимые знания, объяснял, как пагубно наркотические вещества влияют на мозг.
Потом я предлагал им альтернативный поиск себя, призывал к честной состязательности в творческом мире. В общем, это было непросто, но достаточно плодотворно. Многие полностью отказались от употребления наркотических веществ, даже перестали пить и курить. Хотя бросить курить я от них не требовал. Это уже было настоящим подарком.
Я никому не рекомендую баловаться с наркотическими веществами. Да, сегодня в нескольких странах легализовано употребление ряда наркотиков. Но нет уверенности, что мы хорошо понимаем отдаленные последствия приема этих веществ. Как я уже сказал, в некоторых странах в психотерапевтических целях также разрешено применение наркотических препаратов, но, как правило, это происходит под строгим контролем специалиста.
Впереди вас ждет еще пара удивительных фактов о том, какие чудовищные вещи способны сотворить с мозгом наркотики. Но сначала несколько слов об антидепрессантах.
Дофаминовые антидепрессанты
К группе антидепрессантов можно отнести все вещества, способствующие либо накоплению нейромедиатора в синаптической щели, либо повышению чувствительности рецепторов и, как следствие, нормализации эмоционального фона человека.
Важно понимать, что клиническая депрессия – это медицинский диагноз. Она нередко требует медикаментозного лечения под контролем врача-психотерапевта.
Условно депрессии делятся на два вида. Первые вызваны сложными жизненными ситуациями, с которыми психика человека по каким-то причинам не смогла справиться самостоятельно. Депрессии этого типа обычно лечат серотониновыми антидепрессантами. Вторые – эндогенные, то есть вызванные внутренними факторами, например наследственностью. И хотя сейчас исследователи спорят о том, есть ли вообще эндогенные депрессии, мне, как человеку с нейробиологическим образованием это видится вполне возможным.
Я об этом пишу, поскольку нередко слышал от практикующих врачей-психотерапевтов, что при лечении некото-рых пациентов классические серотониновые антидепрессанты не работают, зато хорошо помогают дофаминовые. Вы можете догадаться, что к этой группе пациентов относятся те, у кого высока вероятность развития шизофрении. Как правило, таким тревожным пациентам назначают сразу несколько препаратов: какой-нибудь антипсихотик и дофаминовый антидепрессант, например «Велбутрин», который блокирует обратный захват дофамина.
Прием любых лекарственных препаратов, воздействующих на дофаминовую систему, должен производиться исключительно под контролем врача-психотерапевта.
Дофаминовый баланс
Резюмируя все вышеизложенное, мы с вами приходим к выводу, что вывести из строя дофаминовую систему может любое злоупотребление поощрением. Это любые зависимости и помешательства: лотереи, любовь к вкусной еде (особенно к сладкому) и так далее. Сюда же можно отнести просмотр видеороликов в интернете, непрестанный поиск нового развлекательного материала. Мы еще рассмотрим эту тему подробнее в третьей части.
Интересно, что просмотр материалов эротического содержания также вызывает некоторое подобие зависимости и приводит к сбою в работе дофаминовой системы. Некоторые специалисты полагают, что множество людей сознательно избегают реальных физических контактов, поскольку последние не дают таких же ощущений, как виртуальные.
Теоретически любая приятная мысль, на которой мы зацикливаемся, может подрывать работу дофаминовой системы.
Как мы с вами уже выяснили, наш мозг не задумывался природой для бесконечного удовольствия. Мозгу свойственно тревожиться, иногда быть в напряжении. Хотя постоянная тревога для него так же вредна, как и чрезмерная расслабленность.
Многие сейчас наверняка хотят услышать от меня практические рекомендации по поводу того, что делать с дофамином. Главное – не нужно насиловать свою дофаминовую систему, знать меру. К числу вещей, которых необходимо избегать, можно отнести и просмотр слишком большого количества развлекательного контента, и злоупотребление кофе и шоколадом.
На самом деле можно сделать кое-что конкретное для отслеживания своего дофамина. Когда вы изучаете (сканируете) пространство вокруг, всякий раз, обнаруживая нечто, что может удовлетворить вашу потребность, ваш мозг вырабатывает дофамин.
Постарайтесь понаблюдать за собой. Возьмите лист бумаги и разделите его линией пополам. Слева выписывайте то, что может помочь вам удовлетворить потребность, а справа – ваши ощущения. К примеру, с утра вы думали о том, что надо бы приготовить вкусный пирог вечером. Придя с работы, вы забыли об этом. И вот вы пришли на кухню, открыли холодильник и увидели, что кто-то из домочадцев купил целую миску вишен. Запишите это и ваше внутреннее ликование.
Еще можно отмечать успешно завершенные дела. А также записывайте ощущения, которые вы испытывали, когда совершали маленькие шажочки к своей цели (закрывали очередную задачу). Вообще, дофамин – удивительный нейромедиатор. Он обеспечивает нам интерес. Я помню, одна моя очень мудрая коллега сказала: «Я не болею, потому что мне интересно». И действительно, наблюдая за ней, я всегда удивлялся, почему она все время в строю, постоянно бодрая и живая. Ей просто интересно заниматься тем, что ей интересно (простите за тавтологию).
И напоследок: попробуйте «лишать» себя каких-то радостей хотя бы неделю-другую. Просто откажитесь от чего-то привычного. И вы поймете, как бывает вкусен мамин или бабушкин суп, каким приятным может быть газированный напиток, как чудесно полежать в горячей ванне, посмотреть очередной выпуск юмористического шоу и так далее.
Поскольку все-таки эта книга про мозг в целом, я вынужден свернуть разговор про дофамин. Хоть и могу говорить о нем еще очень долго, потому что это область моего научного интереса в прошлом. Но теперь пора рассказать еще об одном важном нейромедиаторе – серотонине.
Серотонин
В других главах я уже упоминал о функциях серотонина. Если в двух словах, он не делает нас радостными, но нормализует эмоциональный фон. Серотонин держит наш организм в тонусе.
Если с серотонином все в порядке, вы, скорее всего, не впадете в затяжную депрессию и у вас не будет долго длящегося ощущения апатии и безысходности. Серотонин как бы уберегает вас от таких состояний. Мне приходится акцентировать на этом внимание, поскольку так уж повелось, что и дофамину, и серотонину приписывают какие-то совершенно чудодейственные свойства – и радостными нас сделают, и счастье нам подарят.
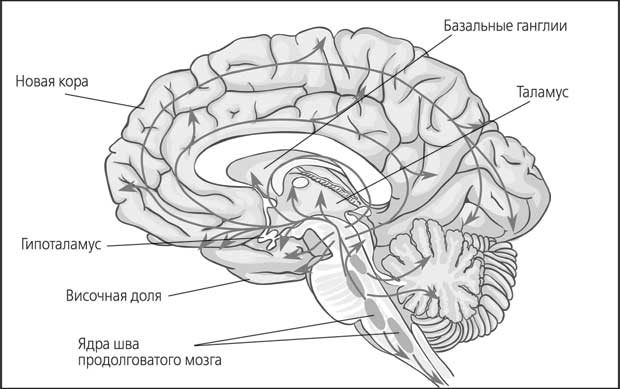
Рис. 33. Схема распределения путей серотониновой системы
Нет, ничего подобного на самом деле не происходит. Серотонин просто выполняет функцию регулирования степени нашей бодрости, помогая нам жить, бороться за свое место под солнцем.
Даже бегло окинув взглядом схему серотониновой системы, вы заметите, что пути этого нейромедиатора простираются по всему мозгу. И это неспроста. Серотонин регулирует великое множество самых разнообразных нейрофизиологических процессов: воздействует на гормональную регуляцию функций гипоталамуса, отвечает за порог болевой чувствительности, влияет на тонус сосудов, управляет эмоциональным фоном и так далее.
Обратите внимание, что серотонин может влиять на субъективное чувство боли. И действительно, при некоторых депрессиях возникают беспричинные боли в разных частях тела. Это связано с понижением уровня серотонина в синаптических щелях. Вообще, до сих пор центров болевой чувствительности в мозге так и не обнаружено. Боль – это реакция на некое неадекватное воздействие на наш организм. Причем речь идет как о физической боли, так и о душевно-психической. Например, сильное надавливание на кожу приводит к неприятным болезненным ощущениям. Чрезмерные психоэмоциональные нагрузки, апатия, чувство потери или безвыходности ситуации также могут приводить к болезненным ощущениям в теле. Предполагают, что баланс нейромедиаторов может создавать ощущение внутреннего безболезненного спокойствия.
Отсюда проистекает еще одна функция серотонина: он контролирует отрицательные эмоции, конкурируя с дофамином и норадреналином. Последние усиливают активность центра ожидания удовольствия. А серотонин подавляет центры отрицательных эмоций (задний гипоталамус, амигдалу).
Снижая градус отрицательных переживаний, серотонин контролирует настроение. Как я уже говорил, чрезмерная расслабленность или радость тоже вредны.
Очень важно понять эту принципиальную разницу. Серотонин не активирует специально центры удовольствия, а лишь тормозит центры негативных переживаний, не давая нам «скатываться» в депрессию.
Вот поэтому, когда его мало, появляются апатия и ощущение безнадежности. Некому нас вытащить из ямы депрессии и тревоги. А ведь это наши спутники еще со времен первобытных людей. Но современная нейрофармакология стоит на страже нашего настроения и разрабатывает вещества, способные поддерживать нормальный уровень серотонина в мозге.
Серотониновые антидепрессанты
В народе испокон веков людям с плохим настроением советовали прогуляться, порыбачить, принять спиртовую настойку из чего-нибудь. Сейчас советуют не только настойки, но и различные психостимуляторы. И эффект они действительно оказывают, но, к сожалению, от депрессии не избавляют.
До 1950-х годов депрессивные состояния лечили опиумными наркотиками и амфетамином. И выглядело это все ужасно, конечно.
Лишь в 1970-х годах стали формироваться представления о том, что депрессия может быть связана со снижением уровня серотонина и других нейромедиаторов (например, норадреналина).
К 1977 году синтезировали флуоксетин, который лишь спустя 14 лет поступил в продажу под названием «Прозак». Долгое время люди очень скептически относились к антидепрессантам. Никто не понимал, работают ли они вообще.
У антидепрессантов, в отличие от многих других препаратов, есть одна особенность: они начинают действовать далеко не сразу, а через недели, а порой и месяцы.
Мы с вами уже говорили об антипсихотиках (нейролептиках), которые используются при лечении шизофрении и психозов. В целом у человека с острым психозом за счет блокирования дофаминовой системы останавливается бурная психическая активность. Если дать антипсихотик здоровому человеку, его мозг просто опустеет: все внутри сделается тусклым, невыразительным, психические процессы затормозятся. В обоих случаях происходят схожие процессы подавления психической деятельности.
В случае же с антидепрессантами мы наблюдаем обратную картину. Антидепрессант никак не повлияет на эмоциональный фон человека, если тот здоров.
Селективные ингибиторы обратного захвата серотонина (СИОЗС) сейчас представляют собой золотой стандарт антидепрессантов. К препаратам этой группы относят «Прозак» (флуоксетин), «Золофт» (сертралин), «Ципрамил» (циталопрам) и другие.
После нескольких недель приема препаратов группы СИОЗС серотонин постепенно накапливается в синаптической щели. И через некоторое время у человека потихоньку выравнивается эмоциональный фон. Лучше всего прием подобных препаратов происходит на фоне когнитивно-поведенческой терапии. Вот почему желательно, чтобы врач-психотерапевт проводил с человеком еще и занятия, направленные на работу с мышлением.
Сегодня ведутся споры о том, как на самом деле работают антидепрессанты. В 2009 году вышла статья Катерины Хармер, где указывалось, что антидепрессанты запускают работу нейротрофинов (факторов роста), а те уже восстанавливают нормальную работу лимбической (эмоциональной) системы. Эта гипотеза объясняла, как психотерапевтическая беседа давала результаты на фоне приема препарата.
Но некоторые ученые подвергли критике эти выводы, ссылаясь на то, что наше мышление никак не может влиять на такие глубинные структуры мозга, как эмоциональная система.
Таким образом, механизм работы антидепрессантов пока остается не выясненным до конца.
Сейчас есть и другие классы антидепрессантов, помогающие выровнять эмоциональный фон. Они воздействуют на норадреналиновую систему. Подробнее о норадреналине мы поговорим во второй части.
Как вы уже могли догадаться, из-за того, что серотониновые рецепторы представлены в мозге очень широко, они становятся одной из главных мишеней наркотиков.
К числу самых известных веществ, воздействующих на серотониновую систему, относится, к примеру, ЛСД (диэтиламид лизергиновой кислоты). ЛСД, как и ряд других веществ, имитирует серотонин. Он сам напрямую связывается с различными серотониновыми рецепторами и вызывает смешение образов, галлюцинации, эйфорию, ощущение отрешенности от мира.
Хотя ведутся споры о том, вызывает ли ЛСД привыкание, пагубное влияние этого вещества на психику вполне доказано. Бесконтрольный прием ЛСД вызывает психозы, а в некоторых случаях развиваются суицидальные мысли (особенно под воздействием самого препарата).
Вполне вероятно, что со временем уровень синтеза серотонина снижается. Организму нет смысла его синтезировать, если извне поступает заменитель. А это уже может провоцировать затяжные депрессии.
Существует также ряд наркотических веществ, которые влияют сразу на несколько нейромедиаторных систем. К таким наркотикам относится, например, экстази (MDMA). Экстази воздействует на дофаминовую, серотониновую и норадреналиновую системы.
К сожалению, наркотики только на первый взгляд кажутся чем-то экзотическим – этаким уделом некой мифической маргинальной группы населения. На самом деле люди тысячелетиями употребляли такой доступный наркотик, как алкоголь. Его действие связано с работой тормозных синапсов, например ГАМК-ергических.
ГАМК (Гамма-аминомасляная кислота)
При выбросе ГАМК в синаптическую щель нервный импульс блокируется. Когда человек сильно взволнован, перевозбужден, система ГАМК-клеток тормозит его деятельность. В повседневной жизни это позволяет выдерживать некий баланс. Считается, что вещества, воздействующие на ГАМК-рецепторы, способны работать как успокоительные и средства от бессонницы.
Вообще, эти рецепторы очень сложные. Они связываются не только с молекулой ГАМК, но и с этиловым спиртом. В норме небольшое количество алкоголя синтезируется самим организмом. Вероятно, поэтому и рецепторы нам эволюционно достались.
Мы не замечаем действия небольшого количества собственного алкоголя. В больших дозах этиловый спирт связывается с ГАМК-нейронами, а те в свою очередь начинают тормозить все подряд.
Этим объясняется общий седативный эффект, расслабление скелетных мышц и прочие признаки опьянения. Очень сильно тормозится работа лобных долей (наши внутренние цензоры, отвечающие за нормы поведения в обществе). Поэтому тут и срабатывает уже упомянутая пословица «Что у трезвого на уме, то у пьяного на языке».
У человека в состоянии опьянения изменяется оценка поступающей информации. И он начинает слишком буквально понимать собеседника. Так могут возникать конфликты, драки, ссоры.
Считается, что ГАМК-нейроны включаются в работу при приеме доз в размере 60–80 граммов спиртового эквивалента. Условно, это стакан водки. Такая доза оказывает успокаивающее действие, антистрессорное. Поэтому люди, выпивающие регулярно, зачастую объясняют свою привычку тем, что алкоголь позволяет им снизить последствия стрессовых нагрузок.
Есть исследования, в которых доказано, что алкоголь может также воздействовать и на дофаминовую систему. У человека улучшается настроение, усиливается двигательная активность. Обычно это наблюдается при принятии небольших доз алкоголя.
При увеличении дозы может происходить выброс опиоидных пептидов (эндорфинов). Отсюда мы получаем состояние эйфории. Конечно, эффект не такой сильный, как при приеме кокаина например, но он все же присутствует.
И тут есть вот какая опасность. Раз задействуется дофаминовая система, связанная с мотивацией, у человека смещаются мотивационные потребности в целом. А в сочетании с подкреплением состояния эйфории, возникшего за счет опиоидных пептидов, все это приводит к самой настоящей зависимости. Вот почему с нейрофизиологической точки зрения алкоголь – это такой же наркотик как, например, опиаты (и другие виды наркотических веществ).
Существуют препараы бензодиазепинового ряда («Феназепам», «Диазепам»). Они применяются для лечения тревожных расстройств. Эффект этих лекарственных средств также основан на том, что они воздействуют на ГАМК-рецепторы. Вообще, ГАМК-рецепторы достаточно сложно устроены. У одного рецептора может быть несколько участков связывания с разными веществами. Барбитураты («Люминал») тоже воздействуют на определенные участки ГАМК-рецепторов. Этим объясняется снотворный эффект от приема «Корвалола», например, в состав которого входит фенобарбитал – один из барбитуратов.
Привиденные примеры хорошо иллюстрируют, как разные вещества запускают работу одной и той же системы. Несомненно, эффект, оказываемый ими, хоть несколько и различается, но во всех случаях наблюдается общая тенденция к торможению процессов психической деятельности.
Эндорфины
Эндорфины (эндогенные морфины) – группа химических (пептидных) соединений, которые могут уменьшать боль и влиять на наше настроение.
Вообще, если и говорить про какие-то «гормоны счастья», то, вероятно, эндорфины лучше всего подойдут под это определение (хотя с точки зрения нейробиологии это все равно не совсем так).
Сами по себе эндорфины нам необходимы для того, чтобы регулировать пороги болевой чувствительности. Если серотонин регулирует этот порог в целом, то эндорфины делают это более локально. Как я уже говорил, в мозге не обнаружено центров боли. Считается, что если оказывать сверхсильное воздействие на рецепторы разной чувствительности, то выделяются вещества, которые запускают неприятные ощущения. В третьей части мы еще вернемся к вопросу восприятия боли.
Если бы не было эндорфинов, даже слабое, неосторожное механическое воздействие на кожу вызывало бы сильнейшую боль. Но этого не происходит, потому что эндорфины как бы выравнивают ощущения, позволяя нам более адекватно взаимодействовать с окружающей средой.
Существует ряд веществ, имитирующих сами эндорфины. К ним относят опиумные наркотики, как естественные (морфий), так и полусинтетические (героин). Попадая в организм, они взаимодействуют напрямую с эндорфиновыми (опиатными) рецепторами.
Например, героин, в отличие от естественных эндорфинов, воздействует на все рецепторы без разбора. При этом в работу включаются и другие нейромедиаторные системы – дофаминовая, ГАМК, гистаминовая. У человека возникает сильнейший прилив эйфорического блаженства, снимаются все тревоги.
Вообще, последнее – это один из самых коварных эффектов приема именно опиумных наркотиков, таких как морфин и героин.
Для мозга крайне соблазнительно находиться в состоянии, когда его ничто не тревожит. Вообще ничто. Угнали машину – ничего страшного, куплю новую. Отключили свет – тоже хорошо, сэкономим на электроэнергии. Никаких тревожных мыслей ни о чем.
Даже после однократного приема человек начинает всеми силами стремиться к этому состоянию. Вот почему героин вызывает привыкание сразу после первой дозы.
При регулярном приеме героина количество опиоидных рецепторов снижается. Они просто выходят из строя. И дозу приходится увеличивать.
Прекращение приема наркотика вызывает состояние, называемое ломкой. Из-за того, что нарушена эндорфиновая система, у человека возникает неадекватное восприятие боли. Возникают судороги, сильные боли во всем теле, бессонница и так далее.
Как управлять эндорфинами
Несомненно, нам хочется как-то воздействовать на эндорфиновую систему без помощи опасных веществ. Один из эффективных способов получить дозу эндорфинов – это смех. Например, вы можете рассказывать какие-то безобидные смешные шутки в кругу близких людей.
Другой способ повысить количество выделяемых эндорфинов – продолжительные физические нагрузки, особенно если они завершаются упражнениями на растягивание мышц тела.
Попробуйте записать ваши ощущения после искреннего смеха в кругу близких друзей. Или после длительной физической нагрузки (бега на длительную дистанцию, часового занятия в спортзале и так далее).
На уровень нейромедиаторов в мозге можно воздействовать, корректируя диету: например, употреблять шоколад, бананы, сельдерей, творог, твердые сыры и другие продукты. Но диету лучше обсудить с врачом.
Помните, что прием антидепрессантов должен проходить только под контролем врача-психотерапевта.
Существуют и другие нейромедиаторы, например адреналин, глутамат, гистамин и так далее. Они тоже влияют на наше поведение.
Важно понимать, что все нейромедиаторы работают в тесном взаимодействии друг с другом. Иногда переизбыток или недостаток одного в той или иной степени компенсируется работой других. Природа так устроена, что она старается продумывать запасные пути или различные подстраховки.
Серьезные исследователи в области нейрохимии мозга никогда не позволяют себе объяснять поведение человека работой лишь одного какого-то нейромедиатора. К тому же надо понимать, что пока мы не знаем обо всех функциях тех или иных нейромедиаторов. Вполне вероятно, в ближайшие десятилетия будут открыты другие интересные свойства этих удивительных молекул.
Мы с вами рассмотрели несколько концепций – вариантов того, как можно изучать мозг. Мы познакомились с нейрофизиологической концепцией условных рефлексов и доминант, с концепцией клеточного строения мозга, взглянули на структурную концепцию уровней – этажей мозга, разобрали нейрохимическую концепцию работы молекул-медиаторов.
Я предлагаю вам, используя полученные знания, окунуться теперь в мир поведения человека и понять, как те или иные системы обеспечивают наши познавательные функции.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК