Глава 10. ЭЛЕКТРИЧЕСКИЙ ПУТЬ
Глава 10.
ЭЛЕКТРИЧЕСКИЙ ПУТЬ
При оценке действия изменений свободной энергии на химические системы ход химической реакции проще рассматривать по аналогии с движением в гравитационном поле. Это вполне разумное решение, поскольку на всем протяжении предыдущей главы мы доказывали, что химические реакции производятся под воздействием химического потенциала, так же как падающие тела движутся под воздействием гравитационного потенциала. А движение падающих тел нам настолько хорошо знакомо по бытовому опыту, что для нас вполне естественно визуализировать все по аналогии с ним.
Рассмотрим, к примеру, соединение водорода и кислорода, при котором формируется вода. Смесь водорода и кислорода содержит в себе определенное количество свободной энергии на моль смеси («молярная свободная энергия»), и вода тоже. Судя по тому факту, что водород с кислородом стремительно бросаются соединяться, стоит их лишь чуть-чуть подтолкнуть, — уровень свободной энергии смеси водорода и кислорода выше, чем образуемой при их соединении воды. Это можно представить в виде схемы (не претендуя при этом на использование каких-либо реальных цифр) — рис. 12. Точка А представляет собой уровень свободной энергии чистой смеси водорода и кислорода, а точка В (размещенная на оси ниже, чем точка А) представляет собой уровень свободной энергии чистой воды, образовавшейся при их соединении.
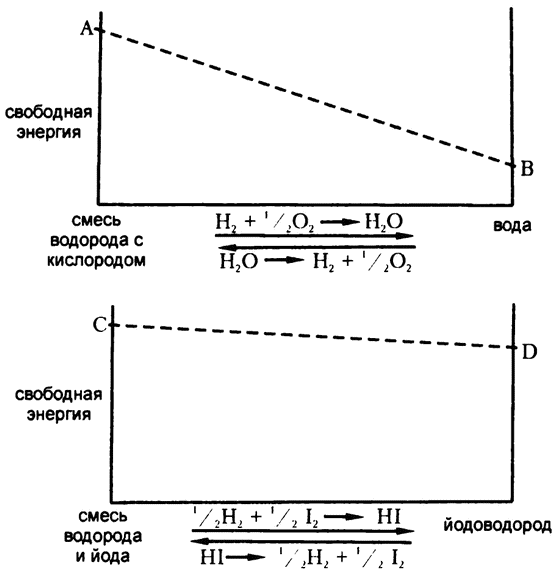
Рис. 12. Изменения свободной энергии при образовании воды (вверху) и йодоводорода (внизу)
По мере того как водород и кислород соединяются для образования воды, все большее количество молекул этих веществ в нашей воображаемой замкнутой системе уступает место молекулам воды. Постепенно смесь с высоким содержанием свободной энергии вытесняется веществом с более низким ее содержанием, так что общая свободная энергия системы постепенно снижается.
Самый простой способ продемонстрировать это — провести на диаграмме прямую линию от точки А до точки В. Таким образом мы получаем картинку наклонной плоскости, и общий жизненный опыт с легкостью подсказывает нам единственное направление, по которому будет осуществляться спонтанное движение по такой плоскости. Соединение водорода с кислородом для образования воды можно рассматривать как «скатывание вниз» по наклонной плоскости начиная с точки с высоким уровнем свободной энергии. Обратная же реакция — расщепление воды — отражает требующее усилий движение вверх по наклонной.
Точнее, нарисованный мной график в виде прямой линии был бы полностью справедливым только в том случае, если бы молярная свободная энергия водорода и кислорода не менялась вместе с концентрацией. Однако на самом деле уровень молярной свободной энергии по мере концентрации незначительно, но меняется, так что изображенная выше прямая линия в действительности не является совсем прямой. В данном конкретном примере отличие от прямой достаточно мало, чтобы им можно было пренебречь, но в тех случаях, где общая свободная энергия системы значительно меньше, чем у системы, состоящей из смеси водорода с кислородом, упомянутый параметр приобретает действительно важное значение.
Возьмем для примера реакцию соединения водорода и йода в йодоводород. В данном случае уровень свободной энергии, используемой в реакции, сравнительно невелик. Визуально это можно изобразить, как в нижней половине рис. 12, отметив значение уровня свободной энергии С смеси чистого водорода с чистым йодом лишь немного выше уровня свободной энергии D чистого йодоводорода, образуемого в ходе полного соединения водорода и йода.
Первое, что хочется сделать в подобной ситуации, — это снова провести прямую линию от одной точки до другой, так чтобы получилась еще одна наклонная плоскость, угол наклона которой был бы меньше, чем предыдущей, но в остальном аналогичная первой. Тогда реакция снова «катилась бы под уклон» — от смеси водорода и йода до йодоводорода, и образовавшийся в ее ходе йодоводород так и оставался бы неразлагаемым «у подножия», пока с помощью приложения некоторого усилия его не подняли бы «вверх». По такой логике смесь водорода и йода отличалась бы от смеси водорода и кислорода лишь скоростью и силой реакции, но не общим рисунком ее хода.
Но мы знаем, что на самом деле это не так. Водород и йод вступают в соединение не в полном объеме, а значит — не «скатываются вниз до конца». Более того, и чистый йодоводород до некоторого уровня будет сам по себе распадаться, что соответствовало бы по нашей схеме «движению вверх». Значит, график с прямой линией был бы неправильным.
Ответ кроется в том факте, что молярная свободная энергия снижается вместе с концентрацией вещества. Если концентрация смеси водорода и йода уменьшится на 10 процентов за счет образования йодоводорода, то уровень свободной энергии смеси снижается сильнее чем на 10 процентов. Это значит, что график изменения уровня свободной энергии, начинаясь от точки С, будет опускаться сильнее, чем прямая линия.
То же самое справедливо и в отношении йодоводорода. При разложении части его уровень свободной энергии оставшейся части окажется меньше, чем можно было бы ожидать. Поэтому от точки D график изменения уровня свободной энергии тоже будет опускаться вниз.
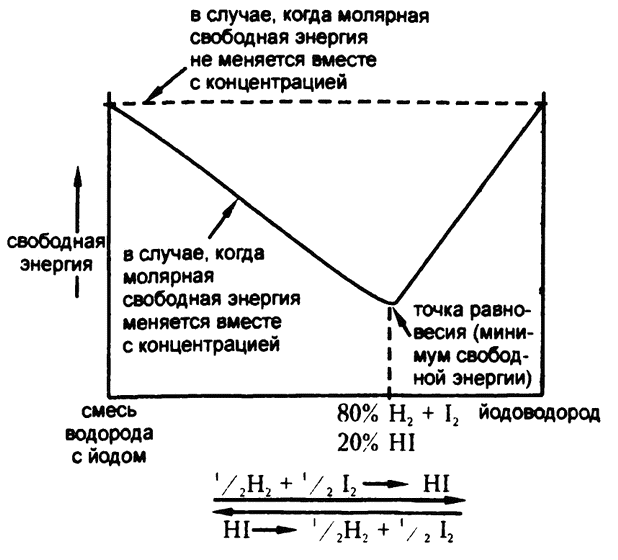
Рис. 13. Изменения уровня свободной энергии
Так что график будет напоминать не наклонную доску, а скорее подвесной гамак и на протяжении большей его части уровень свободной энергии будет меньше, чем на любой из крайних точек.
Этот факт надо подчеркнуть особо. Из-за зависимости молярной свободной энергии от концентрации свободная энергия заданной реакции не достигает минимума ни в одной из крайних точек, в которых реакция была бы завершена либо в одну, либо в другую сторону. Вместо этого минимум достигается в некоторой средней точке, в которой снижение концентрации всех составляющих приводит к максимальному снижению общей свободной энергии.
Следовательно, реакция, приведя к минимальному уровню свободной энергии, оказывается в положении равновесия. Более того, реакция останавливается в одной и той же точке с минимумом свободной энергии, независимо от того, с чего она начинается — со смеси йода с водородом или с чистого йодоводорода.
Поэтому для полноты аналогии с движением под влиянием силы тяжести надо представить себе не одну, а две наклонные плоскости, или, более образно — два горных склона, между которыми находится долина. Если шар отпустить с вершины С, он скатится в ту же самую нижнюю точку долины, что и в случае, если его отпустить с вершины D.
Чем меньше разность уровней свободной энергии между двумя крайними точками графика, тем ближе будет точка равновесия находиться к его середине. Чем выше разность уровней энергии между двумя крайними точками, тем ближе точка равновесия сдвигается в сторону той крайней точки, свободная энергия которой меньше.
В случае соединения водорода с кислородом точка равновесия сдвигается так далеко в сторону воды, что практически неотличима от точки, обозначающей чистую воду. В этой точке равновесия уровень свободной энергии будет, конечно, ниже, чем в точке чистой воды, но настолько неощутимо ниже, что эту разницу практически невозможно измерить (можно только высчитать из сведений о свободной энергии).
Это значит, что в замкнутой системе водород и кислород никогда не соединятся в воду полностью — всегда будет оставаться неизмеримо малое количество свободного водорода и кислорода, не вступивших в реакцию. Более того, если изначально мы имеем чистый водяной пар, то при тех же условиях (температуре и давлении) неизмеримо малое количество этой воды будет разлагаться на водород и кислород.
С точки зрения термодинамики получается, что все реакции обратимы. Однако с практической точки зрения можно продолжать расценивать в качестве необратимых те реакции, в которых точка равновесия неотличимо близка к одной из крайних точек.
Поскольку положение равновесия напрямую зависит от изменений уровня свободной энергии при переходе от одной стороны химического выражения к другой, то это изменение можно очень просто вычислить, исходя из постоянной равновесия. Проблема только в том, что саму постоянную равновесия определить бывает очень сложно, особенно в отношении реакций, которые принято считать необратимыми. Поэтому ученые долго искали другие способы подсчета изменений уровня свободной энергии — и находили. Один из таких способов заслуживает особого рассмотрения, поскольку это поможет осветить важные положения химии. В этом способе используется электричество.
Однако, перед тем как приступить непосредственно к описанию этой методики, нам надо чуть глубже взглянуть на атом. До сих пор, описывая кинетическую теорию газов, я рассматривал атомы как крошечные бильярдные шары. Однако на самом деле они представляют собой гораздо большее. Атомы сами по себе состоят из еще меньших частиц. Это открытие, совершенное в 1890-х годах, произвело поистине революцию в науке.
Эти элементарные частицы принадлежат к трем основным категориям: протоны, нейтроны и электроны. Протоны и нейтроны относительно массивны и плотно сгруппированы в единое тело (так называемое «ядро атома»), находящееся в самом центре атома. Они в обычных химических реакциях не участвуют.
Все остальное пространство атома, за исключением ядра, занимают электроны, представляющие собой очень легкие частицы. Количество электронов в каждом атоме равно количеству протонов в ядре этого атома, и число это свое у каждого химического элемента. Его так и называют — «атомное число». Самый простой атом — атом водорода — содержит всего один протон и один электрон, атомы остальных элементов содержат больше. У некоторых сложных атомов, искусственно создаваемых в последние годы в лабораториях ученых, атомное число превышает сотню. В таблице 2 приведены атомные числа некоторых наиболее распространенных элементов.
Каждый электрон имеет свой «электрический заряд»[4], так же как и каждый протон. У нейтронов электрического заряда нет, и поэтому хотя их значение и крайне велико, но нас в ходе дальнейшего рассмотрения они интересовать не будут. Величина заряда электрона и протона одна и та же, но природа этих зарядов различна. Один протон будет отталкивать другой протон и, наоборот, притягивать электрон. Точно так же и электрон будет отталкивать другой электрон и притягивать протон.
Совершенно произвольно было решено назвать электрический заряд электрона отрицательным, а протона — положительным. Поэтому заряд одного электрона обозначается как -1, а заряд одного протона — как +1. Кроме того, установлен закон, что одинаковые заряды отталкиваются, а противоположные — притягиваются.
В обычном атоме, как я уже сказал, количество протонов ядра (атомное число) в точности уравновешивается количеством удаленных от ядра электронов, так что атом в целом ведет себя как лишенный заряда, или «электрически нейтральный». Однако в отличие от протонов, хорошо укрытых в ядре от воздействия межатомных и межмолекулярных столкновений, легкие электроны, существующие на «внешних рубежах» атома, чувствуют эти события на себе в полной мере. И при химических реакциях неизбежно осуществляется некоторое перераспределение электронов между участвующими в реакции атомами. На самом деле именно наличие перераспределения электронов отличает химические реакции от изменений иного рода.
Таблица 2.
АТОМНЫЕ ЧИСЛА
Элемент — Атомное число
Водород (Н) — 1
Гелий (Не) — 2
Углерод (С) — 6
Азот (N) — 7
Кислород (О) — 8
Фтор (F) — 9
Натрий (Na) — 11
Магний (Mg) — 12
Алюминий (Al) — 13
Фосфор (Р) — 15
Сера (S) — 16
Хлор (Cl) — 17
Калий (К) — 19
Кальций (Са) — 20
Хром (Cr) — 24
Марганец (Mn) — 25
Железо (Fe) — 26
Кобальт (Со) — 27
Никель (Ni) — 28
Медь (Си) — 29
Цинк(Zn) — 30
Серебро (Ag) — 47
Олово(Sn) — 50
Йод (I) — 53
Вольфрам (W) — 74
Платина (Pt) — 78
Золото (Au) — 79
Ртуть (Hg) — 80
Свинец (Pb) — 82
Радий (Ra) — 88
Торий (Th) — 90
Уран (U) — 92
Плутоний (Pu) — 94
Лоуренсий (Lw) — 103
На электрическую нейтральность атома эти изменения могут влиять, а могут и не влиять. К примеру, два атома, столкнувшись, могут поделиться друг с другом электронами вполне стабильным образом (подробнее об этом чуть позже). Это «предоставление» электронов одним атомом другому сохраняется только до тех пор, пока атомы сохраняют контакт между собой. Для того чтобы разъединить атомы, необходимо теперь будет разорвать их стабильную связь, а на это потребуется значительное количество энергии. Без получения этой энергии атомы, имеющие общие электроны, будут неопределенно долго оставаться вместе, и именно это и есть основа тех химических связей, о которых я говорил в предыдущих главах. В молекулах водорода, кислорода, воды, углекислоты, йодоводорода и многих других соединений атомы удерживаются вместе с помощью «общих» электронов.
При подобного рода перераспределении электронов атомы продолжают оставаться электрически нейтральными.
Однако бывает и так, что определенные электроны в атомах некоторых элементов держатся крайне слабо. К примеру, в атоме натрия самый удаленный электрон не слишком-то прочно привязан к своему атому. Поэтому при соседстве с атомом хлора (который все собственные электроны удерживает очень крепко) самый удаленный атом натрия не то что становится «общим», а вообще переходит из атома натрия в атом хлора.
После такого перехода в атоме натрия остается всего 10 электронов, то есть на один электрон меньше, чем требуется, чтобы нейтрализовать положительный заряд 11 протонов ядра. Атом натрия теряет электрическую нейтральность. Теперь он несет общий заряд значением в +1, это заряд протона, потерявшего уравновешивающий его электрон. С другой стороны, у атома хлора теперь 18 электронов, то есть на один электрон больше, чем требуется для нейтрализации 17 протонов ядра. Поэтому его общий заряд теперь равняется заряду этого лишнего электрона, то есть составляет -1.
Такие атомы, несущие электрический заряд по причине избытка или нехватки электронов, называют «ионами». Естественно, ионы делят на положительные и отрицательные. Ионы обозначают приставляя к обычному символу элемента маленький плюс или минус, отражающий заряд иона. То есть ион натрия обозначается как N+, ион хлора — как Сl-.
Некоторые атомы могут терять в ходе химической реакции по два или даже три электрона, а могут и вести себя по-разному в разных условиях — при одной реакции терять два электрона, а при другой — три. Бывает даже так, что группа атомов, удерживаемая воедино с помощью обычных связей из «общих» электронов, теряет или приобретает электроны. Атомы остаются соединенными, но все вместе приобретают электрический заряд и становятся «сложными ионами». Мы не будем вдаваться в пущие подробности; однако на всякий случай приводим здесь список самых распространенных ионов (табл. 3).
Таблица 3.
ИОНЫ
Положительные
Название … Обозначение
Ион водорода … Н+
Ион натрия … Na+
Ион калия … К+
Ион магния … Mg2+
Ион кальция … Са2+
Ион цинка … Zn2+
Одновалентный ион меди … Cu+
Двухвалентный ион меди … Cu2+
Двухвалентный ион железа … Fe2+
Двухвалентный ион железа … Fe3+
Ион аммония … NH4+
Отрицательные
Ион фтора … F-
Ион хлора … Сl-
Ион йода … I-
Ион серы … S2-
Карбонат-ион … СО32-
Нитрат-ион … NO3-
Сульфат-ион … SO42-
Фосфат-ион … PO43-
Примечание. Когда атом или группа атомов теряют или приобретают более одного электрона, то этот факт отмечают приписывая перед плюсом или минусом соответствующий индекс.
Закон о том, что противоположно заряженные частицы притягивают друг друга, распространяется и на ионы. Поскольку ионы натрия и хлора формируются путем перехода электрона от атома натрия к атому хлора, то ионы остаются вместе, связанные силой притяжения между положительным и отрицательным зарядами двух ионов. В итоге получается соединение хлорид натрия — привычная нам поваренная соль.
Такие вещества, как хлорид натрия, удерживаемые воедино ионными связями, не состоят из молекул в том же понимании, что и углекислота или вода.
В кристалле поваренной соли любой отдельный ион натрия не является прочно соединенным с каким-то конкретным ионом хлора в единую двухатомную частицу. Нагляднее всего это видно на примере растворения поваренной соли. Ионы натрия и хлора свободно перемещаются в растворе. Точнее, существует всеобщее притяжение между положительными и отрицательными зарядами, но любой отдельный ион натрия может передвигаться, не таща за собой какой-то конкретный ион хлора. На самом деле под воздействием электрического тока оба набора ионов можно заставить двигаться в противоположных направлениях.
Некоторые химические реакции лучше всего рассматривать именно в свете такой вот ионной независимости; тогда проще всего описывать их, сосредоточившись на одном из ионов и упуская из виду второй.
К примеру, возьмем цинк (Zn) и медный купорос, молекула которого состоит из одного атома меди (Cu), одного атома серы (S) и четырех атомов кислорода и обозначается CuSO4. Если в раствор медного купороса добавить металлический цинк, то произойдет спонтанная реакция, в ходе которой цинк войдет в состав раствора, который станет теперь раствором сульфата цинка (ZnSO4), а медь выйдет из состава раствора и выпадет в осадок в виде знакомого нам красноватого металла.
Записанное обычным образом выражение для этой реакции будет выглядеть так:
Zn + CuSO4 ? ZnSO4 + Cu.
При этом создается впечатление, что сульфатная группа (SO4) отделяется от меди и прикрепляется к цинку. На самом же деле сульфатная группа ничего подобного не совершает. Изо всех компонентов системы она играет самую пассивную роль. Взглянем на происходящее, исходя из ионной картины.
Медный купорос удерживают воедино ионные связи (по крайней мере, частично), и в растворе он существует не в виде отдельных молекул, а в виде смеси ионов меди (Cu2+) и сульфат-ионов (SO2). В ходе реакции атом цинка (его можно записать как Zn0, чтобы лишний раз подчеркнуть его нейтральность в металлической форме) теряет два электрона и становится ионом цинка (Zn2+), и эти два электрона приобретает ион меди, становясь, таким образом, нейтральным атомом меди (Cu0) и оседая в этом виде.
Выражение можно записать так:
Zn0 + Cu2+ ? Zn2+ + Cu0.
Эта реакция подразумевает изменение в природе ионной связи. Изначально мы имеем ионную связь между ионом меди и сульфат-ионом, а в итоге — между ионом цинка и сульфат-ионом. Изменения ионных связей подразумевают и изменение уровня свободной энергии, как и любые другие изменения химических связей. В этом случае реакция проходит спонтанно в направлении, указанном в вышеприведенной формуле, так что мы можем быть уверены в том, что при переходе от металлического цинка и иона меди к иону цинка и металлической меди уровень свободной энергии снижается.
Теперь давайте предположим, что два реагента разделены. В одной камере находится полоска цинка, погруженная в раствор сульфата цинка, в другом — полоска меди, погруженная в раствор медного купороса. Между двумя камерами — пористая перегородка, сквозь которую ионы могут проникать в обе стороны, но, при обычных условиях, очень медленно. В такой системе сами по себе обсуждаемые реакции не будут проходить в каком бы то ни было значительном объеме.
А происходит в ней следующее: атомы цинка в полоске цинка начинают терять электроны и превращаться в ионы цинка. Ионов меди, которые могли бы перехватить эти электроны, поблизости нет, так что в растворе происходит накопление «свободных электронов». Этот процесс не заходит слишком далеко, поскольку срабатывает следующий механизм: все отрывающиеся электроны, обладая одинаковым зарядом, стараются оттолкнуться друг от друга как можно дальше, создавая, таким образом, в растворе нечто вроде «электронного давления». Любому электрону, который хочет в этих условиях оторваться от атома цинка, приходится теперь преодолевать это давление, которое с отрывом каждого нового свободного электрона становится все сильнее, и так продолжается, пока электроны не перестают отрываться вообще. На этом этапе количество накопившихся в растворе свободных электронов относительно мало. То же самое происходит и в «медной» камере, поскольку атом меди тоже имеет склонность терять электроны. И все же в «цинковой» камере электронное давление выше, поскольку склонность атома цинка к потере электронов сильнее, в ней накапливается больше свободных электронов.
Теперь предположим, что полоска цинка соединена с полоской меди металлической проволокой. Тогда мы станем наблюдателями нового для нас и крайне интересного процесса. Обычные атомы по проволоке перемещаться не могут — этому мешают атомы, уже находящиеся в ней. А вот электрон — гораздо меньше и легче, чем атом. Его масса в 1837 раз меньше массы самого легкого атома (имеется в виду конечно же водород). Поэтому электрон может скользить между атомами, из которых состоит металлическая проволока. Способность электрона проходить сквозь вещество зависит от электронного строения самих атомов этого вещества. Электронная структура многих веществ — серы, стекла, резины, например, — не позволяет электронам свободно проходить сквозь них.
Электронное давление в обеих камерах становится движущей силой, запускающей перемещение этих микрочастиц по проволоке. Поскольку в «цинковой» камере электронное давление выше, то электроны будут вылетать из «цинковой» камеры активнее, чем из «медной». Таким образом, общее движение электронов будет происходить в направлений из точки с большим электронным давлением в точку с меньшим электронным давлением, по тому же принципу, по которому камень катится вниз (из точки с высоким уровнем потенциальной энергии — в точку с более низким), а тепло переходит от горячих предметов к холодным (из области с высокой температурой — в область с низкой). Эта разность электронных давлений, служащая движущей силой электронного потока, называется «электрическим потенциалом», или «электродвижущей силой».
По мере того как электроны покидают «цинковую» камеру, электронное давление в ней понижается и находящиеся в ней атомы цинка начинают активнее избавляться от электронов. Эти освобождающиеся электроны тоже покидают камеру, и атомы цинка продолжают испускать электроны в прежнем темпе. Так продолжается неопределенно долго, и этот непрерывный поток электронов и есть знакомый нам электрический ток.
По мере того как электроны перетекают из «цинковой» камеры в «медную», их подхватывают ионы меди, окружающие медную полоску, превращаясь, таким образом, в нейтральные атомы меди. Дальше по мере притока электронов атомы цинка на одном конце проволоки превращаются в ионы и переходят из твердого состояния в раствор, а ионы меди на другом конце превращаются в атомы меди и выпадают из раствора в осадок. Общее количество положительных ионов в обеих камерах не изменяется, как и общий размер положительного заряда. Точнее, положительный заряд собирается в той части раствора, которая окружает цинк, и исчезает из той части, которая окружает медь; однако отрицательно заряженный сульфат-ион может перемещаться сквозь пористую перегородку из «медной» камеры в «цинковую» и поддерживает, таким образом, электрическое равновесие.
Поток электронов — это вид энергии, и его можно использовать для выполнения работы. Электрическая энергия возникает за счет снижения химической энергии, которое происходит в процессе превращения ионов меди и цинка в ионы цинка и медь.
Такое устройство, переводящее свободную энергию химической реакции в электрическую энергию, называют химической батареей, или электрической батареей, или электрохимической батареей, элементом питания или даже «гальваническим элементом», или «вольтовой цепью» (рис. 14), по имени Алессандро Вольта, итальянского ученого, который впервые изготовил химическую батарею в 1800 году. Описанная нами конкретная схема с использованием меди и цинка называется «элементом Даниеля» по имени разработавшего ее в 1836 году английского химика Джона Фредерика Даниеля.

Рис. 14. Поток электронов в гальваническом элементе
Обратите внимание — эти батареи уже изготавливали и использовали за столетие до того, как были открыты электроны! Однако именно с 1890-х годов отсчитывается невероятный рост применения потока электронов благодаря работе физиков, трудившихся в области электроники. Мораль тут такова: чтобы использовать некое явление — совершенно не обязательно его понимать, но если все же его удастся понять, то польза от него возрастет многократно!
Чем больше снижается уровень свободной энергии, задействованной в химической реакции, запускающей поток электронов, тем больше движущий электроны электрический потенциал. Электрический потенциал легко измерить; единицей измерения его служит «вольт», а прибор, которым его измеряют, называется «вольтметр» — опять же в честь Вольта. Математические выкладки Гиббса показали, что из этого потенциала можно высчитать уменьшение свободной энергии. Таким образом, Гиббс увязал с термодинамикой, которая изначально разрабатывалась в общем-то для тепловых машин, не только химическую, но и электрическую энергию.
Некоторые очень важные химические реакции остаются, таким образом, за пределами возможностей прямого изучения. Реакция соединения углерода и кислорода в углекислоту имеет точку равновесия настолько близкую уже к самой углекислоте, что снижение уровня свободной энергии, связанное с ней, подсчитать, исходя из точки равновесия, невозможно. Невозможно создать и химическую батарею на основе реакции соединения углерода и кислорода. Это была бы «топливная батарея», которая позволила бы производить дешевое электричество и представляла бы собой очень ценное и полезное устройство, если бы только ее возможно было создать.
К счастью, здесь можно воспользоваться эквивалентом закона Гесса. Как вы помните, закон Гесса позволяет обращаться с химическими выражениями так, как будто это выражения математические, и это распространяется на значения ?Н (см. главу 8). То же самое справедливо и для ?F. Манипулируя выражениями, для которых можно измерить изменения уровня свободной энергии напрямую, можно вывести из них и значения для тех реакций, для которых напрямую их измерить нельзя.
Таким образом, можно сказать с полной уверенностью, насколько в науке вообще можно что-то говорить с полной уверенностью, что
Н2 + 1/2О2 ? Н2О
?F = -54,6 ккал,
СН4 + 2O2 ? CO2 + 2H2O
?F = -195,6 ккал
и так далее для множества других реакций.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Электрический кабель цианобактерий
Электрический кабель цианобактерий Другая проблема, долго дожидавшаяся своего срока, — это передача энергии вдоль мембраны. С самого начала хемиосмотической эпопеи мне казалось очевидным, что разность электрических потенциалов весьма удобна для транспорта энергии в
ПУТЬ К СОЦИАЛЬНОСТИ
ПУТЬ К СОЦИАЛЬНОСТИ Итак, появление в эволюции бесполых особей — первоначальная причина превращения семьи в общество и причина существования обществ насекомых — было результатом недостаточного кормления личинок их родителями. Пара основателей у термитов,
ЖИЗНЕННЫЙ ПУТЬ
ЖИЗНЕННЫЙ ПУТЬ Итак, по-моему, не подлежит сомнению, что касты рабочих и солдат, точно так же как и самок и самцов, различны уже в самом яйце, что они родятся такими, а не образуются ввледствие различного рода питания и ухода в период раннего детства... Г. У. Бейтс.
Глава XII Итальянцы пролагают путь
Глава XII Итальянцы пролагают путь Идею о непрерывной циркуляции крови по организму XVI век практически не воспринял.Свыше четырех тысяч лет до этого легендарный китайский император Хуань-ди писал: «Поток крови течет непрерывно по кругу и никогда не останавливается…»
ГЛАВА 11 Электрический ток и магнитные поля
ГЛАВА 11 Электрический ток и магнитные поля О том, что некоторые рыбы могут генерировать электрический ток, было известно еще древним грекам, хотя они и не знали, что то шоковое оцепенение, которое вызывали у рыбаков электрические скаты, было связано с действием
ПУТЬ КЕНГУРЕНКА
ПУТЬ КЕНГУРЕНКА Крису и Джиму в память о пиявках, лирохвостах и велосипеде в дымоходе (не говоря уже о светлячках) ПРЕДВАРЕНИЕ Перед вами повесть о шестимесячном путешествии, во время которого мы побывали в Новой Зеландии, Австралии и Малайе. Путешествие это состоялось
Глава 14. От класпера к пенису: это был долгий путь, детка
Глава 14. От класпера к пенису: это был долгий путь, детка Если бы мне поручили выдать награду за лучшую идею всех времен, я бы вручил ее Дарвину, а не Ньютону, или Эйнштейну, или кому-либо еще. Идея эволюции путем естественного отбора одним махом объединяет все живое, его
Перспективный путь
Перспективный путь Во всех отложениях пермо-триасовой системы, всех материках, даже в Антарктиде, найдены тысяча окаменевших костей и полных скелетов особой группы рептилий — звероподобных ящеров (подкласс терапсида).Более сотни миллионов лет жили они на Земле.
В трудный путь
В трудный путь Взгляните на эту рыбу. Вам сразу станет понятно, почему ее назвали горбушей. Только не думайте, что она всегда бывает такой горбатой.Горбуши — стройные и красивые рыбы. Рыба — мать — серебристая, а у самца спина синяя с зеленым переливом. Такими плавают они в
Путь к морю
Путь к морю Не зная, что он уже подсчитан, «рваный плавничок» бойко плыл со своей стайкой по широкой реке. Рядом с ним был вертлявый сазанчик с царапиной на боку.Не успели они проплыть и нескольких шагов, как к ним метнулась какая?то тень, раскрылась зубастая пасть.«Рваный
2.1. Путь йоги
2.1. Путь йоги Философия йоги впервые стала известна западному миру, когда Свами Вивекананда выступил с речью в Религиозном парламенте в Чикаго 11 сентября 1893 года. Позже, в 1920 году, Парамаханса Йогананда обратился к Международному религиозному конгрессу в Бостоне. В том же
Путь вперед
Путь вперед Закончив первое фМРТ-исследование, я вернулся к своим энцефалограммам и интервью с новыми заключен ными. В свободное время я написал статьи о пяти ис следованиях для диссертации и подачи в рецензируемые журналы.Моя диссертация близилась к завершению,