Мутации, затрагивающие органогенез
Мутации, затрагивающие органогенез
Как мы убедились выше, события, происходящие на ранних стадиях развития, в значительной степени зависят от информации, поставляемой материнским организмом. Однако примерно ко времени гаструляции важную роль в дальнейшем развитии начинает играть генетическая информация самого зародыша, и организм приобретает возможность контролировать свою судьбу. Для морфогенетических событий, следующих за формированием бластодермы, необходим синтез РНК и ее трансляция в белок. О необходимости генетической информации зародыша можно также судить по большому числу мутаций, оказывающих влияние на события, происходящие после гаструляции, и указывающих, таким образом, на существование генов, регулирующих эти события. У этих мутаций не наблюдается наследования по материнскому типу.
В качестве примера можно воспользоваться локусом N (Notch) у Drosophila melanogaster. Notch-сцепленная с полом доминантная мутация, являющаяся одновременно рецессивной деталью. Гомозиготные самки (N/N) и гемизиготные самцы (N/Y) гибнут на стадии зародыша спустя примерно 6 ч после оплодотворения. Это время соответствует моменту, непосредственно следующему за гаструляцией, когда зародыш проделал примерно четвертую часть эмбриогенеза. Гистологические и морфологические исследования, проведенные Паулсоном (Paulson) на этих зародышах, показали, что вентральная и латеральная эктодерма, которая обычно дает начало эпидермису и нервным клеткам, образует только клетки, похожие на нейробласты, а эпидермиса не образует вовсе. Поэтому можно предполагать, что локус Notch необходим для дифференцировки из зародышевой эктодермы нервной ткани в противовес эпидермальной. Оказалось, однако, что это несколько упрощенное объяснение. Шелленберджер (Shellenbarger) и его сотрудники выделили из локуса Notch температурочувствительный аллель и охарактеризовали его. Мухи, содержащие этот аллель, при температуре 22°С развиваются нормально, тогда как при 29°С наблюдается описанная выше гибель зародышей. В экспериментах со сдвигами температур, подобных рассмотренным в начале этой главы для мутантов shibire, было установлено, что к дефекту локуса Notch и недостаточности продукта этого локуса зародыш чувствителен не только в этот ранний период эмбриогенеза. Результаты экспериментов с изменением температуры представлены на рис. 7-5. При помощи кратковременных повышений температуры были выявлены еще три периода, когда мутантному организму жизненно необходима нормальная активность локуса Notch. Воздействия непермиссивной температуры на личинок второго или третьего возраста или на куколок приводили к летальному исходу. Более того, кратковременные воздействия (pulses) в определенные периоды третьей личиночной стадии или на стадии куколки вызывали такие же рубцы на глазах и дефекты щетинок, как у мутантов shibire (рис. 7-5). Поэтому, подобно shibire, мутация Notch обладает гораздо более широким действием, чем можно было бы ожидать на основании ее главного фенотипического проявления. Все структуры, на которые она действует, эктодермального происхождения, и в своих дальнейших экспериментах с гинандроморфами Шелленберджеру удалось показать, что наблюдаемые морфологические дефекты автономны и присущи только эктодермальным клеткам. Таким образом, снова, как и в случае мутаций shibire, создается впечатление, что один и тот же продукт мутанта Notch необходим разным клеткам эктодермального происхождения в течение нескольких дискретных периодов на всем протяжении развития. Следует также отметить, что для завершения одного и того же набора онтогенетических событий необходимы два разных гена, Notch+ и shibire+ , и что отсутствие того или другого из них приводит к удивительно сходному комплексу нарушений.
У домовой мыши (Mus musculus) имеется один сложный ген, Т-локус, который во многом сходен с только что описанной системой Notch. Первый аллель этого локуса был описан как аутосомный доминантный аллель, названный Brachyury (Т). У мышей, гетерозиготных по этому гену, Т/+, хвосты короткие. В гомозиготном состоянии (Т/Т) этот ген летален и зародыши гибнут внутриутробно. Вскоре после обнаружения этой доминантной мутации было установлено, что потомки от скрещивания гетерозигот (Т/+) с мышами дикого типа часто вовсе лишены хвоста. Оказалось, что эти бесхвостые мыши - результат рецессивных аллелей Т-локуса, часто встречающихся в природных популяциях мышей. Следовательно, эти бесхвостые мыши имели генотип T/t. От скрещиваний между такими гетерозиготными мышами T/t были получены бесхвостые мыши, размножающиеся в чистоте. Позднее было показано, что это обусловлено «сбалансированной системой леталей». Как оказалось, среди потомков от скрещивания гетерозигот летальными были не только гомозиготы Т/Т, чего следовало ожидать, но и гомозиготы t/t. Таким образом, выживали только гетерозиготы T/t, которые и давали следующее поколение. Эта интригующая ситуация была изучена как генетически, так и эмбриологически в ряде изящных работ Денна (Dunn), его учеников Беннета (Bennett) и Глюксон-Вэлша (Gluechsohn-Waelsch).
В результате генетических исследований вновь полученных линий, сбалансированных по леталям, было установлено, что скрещивания между бесхвостыми мышами, получившими свой рецессивный аллель t от разных популяций, часто давали нормальных потомков. В частности, от скрещивания T/ta x T/tb были получены нормальные и бесхвостые потомки в соотношении 2:1. Можно показать, что потомки с нормальными хвостами имеют генотип ta/tb. Таким образом, этот генотип был не только нелетальным, но и нормальным морфологически. Еще одна особенность этого локуса была обнаружена при скрещиваниях между самими линиями, сбалансированными по летал ям. Обычно скрещивание гетерозиготы T/ta с такой же гетерозиготой дает только бесхвостых потомков. Однако изредка (1:500 - 1:1000) среди потомков встречаются мыши с нормальными хвостами. Эти нормальные мыши почти всегда получаются в результате редкой генетической рекомбинации в 17-й хромосоме, в участке, соответствующем локусу Т или примыкающем к нему. Можно показать, что наличие хвоста у этих реком-бинантных потомков обусловлено тем, что одновременно с рекомбинацией произошло превращение первоначального аллеля ta в новый аллель tx, который комплементарен аллелю ta таким же образом, как некоторые t-аллели, происходящие от мышей дикого типа, комплементарны друг друга. Различие, конечно, состоит в том, что tx в данном случае непосредственно связан с ta своим происхождением. Было показано, что такое превращение одного аллеля t в другие комплементарные типы происходит с большинством выделенных рецессивов. Некоторые возникающие при этом аллели, например tx, могут в свою очередь при помощи того же механизма превратиться в другой комплементарный аллель, например ty. Такое превращение одного рецессивного аллеля t в другой приводит к образованию ряда постепенно переходящих один в другой аллелей, а в конечном итоге к созданию так называемых t viable, или tv, аллелей. Все эти последние аллели нелетальны, и бесхвостый фенотип экспрессируется только в случае гетерозигот Т/tv; у особей tv/tvхвосты нормальные. Еще один класс рецессивных t-мутаций - это полулетали, жизнеспособность которых колеблется от 2 до 51% нормальной. Как и полностью летальные аллели, они путем постепенных превращений дают tv-типы. Комплементарные скрещивания (T/ta x T/tb) всех как природных, так и полученных экспериментально рецессивных аллелей показали, что 111 существующих мутаций распадаются на 8 отдельных групп, причем ни одна из них не комплементарна Т-аллелю. Число членов во всех группах различно - от одного в группе (tw73 до 66 в группе аллелей tv. Из пяти доминантных Т-мутаций одна была вызвана воздействием рентгеновских лучей, а все другие мутации, обнаруженные в этом локусе, по-видимому, возникли спонтанно.
Мы рассмотрели несколько особенностей этого сложного ряда генетических дефектов, связанных между собой либо тем, что они комплементарны и определяются соседними локусами, либо тем, что они происходят друг от друга. Перейдем теперь к эмбриологическим особенностям экспрессии сложного локуса.
Каждая из восьми комплементарных групп обусловливает разного рода дефекты, проявляющиеся в период от ранних до поздних стадий развития зародыша. Морфологические проявления этих дефектов представлены на рис. 7-10 и 7-11. Самые ранние дефекты обнаружены у зародышей, гомозиготных по аллелю t12. Оплодотворение и деления дробления зиготы приводят к образованию шаровидной массы клеток, называемой морулой. Первый признак клеточной дифференцировки у мышей наблюдается при переходе от этой морулы к следующей стадии - бластоцисте, состоящей из трофобласта (трофэктодермы) и внутренней клеточной массы. Гомозиготные t12-зародыши не достигают этой стадии и недифференцированные «морулы» гибнут, не имплантируясь в стенку матки, в отличие от нормальных зародышей, которые делают это примерно на 4-й день после оплодотворения. Кроме того, t12-клетки, по-видимому, автономны в своем летальном действии. Химеры, содержащие эмбриональные клетки t12 и нормальные эмбриональные клетки, летальны, и их развитие не заходит дальше той стадии, на которой гибнут зародыши t12. Поэтому мутация t12, по-видимому, затрагивает локус, необходимый для первого шага в дифференцировке мышиного зародыша - возникновения трофобласта, из которого в конечном итоге формируются хорион и другие характерные для всех плацентарных млекопитающих внезародышевые оболочки, образующиеся из зиготы.
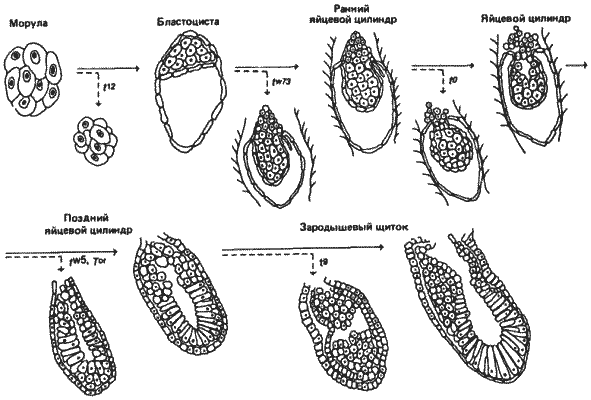
Рис. 7-10. Схематическое изображение событий, происходящих на ранних стадиях развития зародыша мыши. Сплошными стрелками показано течение нормального онтогенеза, а прерывистыми - момент отклонения от нормального развития зародышей, несущих различные t-аллели. Более подробные объяснения см. в тексте (Bennett, 1975; с изменениями).
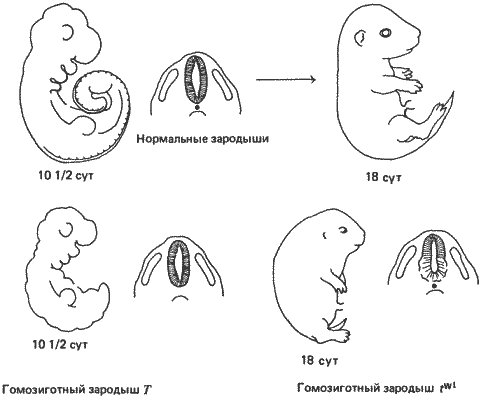
Рис. 7-11. Мышиные зародыши на поздних стадиях развития, иллюстрирующие эффекты двух t-аллелей, действующих на поздних стадиях. Подле каждого зародыша приведена схема поперечного сечения, на которой показаны нервная трубка (заштрихована), хорда (черная точка под нервной трубкой) и сомиты (продолговатые структуры по обе стороны нервной трубки). Полное описание мутантных фенотипов дано в тексте (Bennett, 1975).
Следующий из аллелей, вступающих в действие на очень ранних стадиях, - это аллель tw73. Зародыши, гомозиготные по этому аллелю, образуют бластоцисту. Однако трофобласт таких мутантных зародышей не вступает в надлежащую связь со стенкой матки, и недостаточно хорошо имплантировавшийся зародыш вскоре гибнет.
В норме после успешной имплантации зародыша в стенку матки внутренняя клеточная масса начинает расти и подвергается дальнейшей дифференцировке. Одно из происходящих при этом событий - формирование внезародышевой и зародышевой эктодермы. Из первой в конечном счете образуются плацента и части внезародышевых оболочек, а из второй - собственно зародыш. Мутанты t0 не образуют внезародышевую эктодерму и гибнут на стадии раннего яйцевого цилиндра.
Далее у нормальных зародышей продолжается рост внутренней клеточной массы и образуется продолговатое скопление эктодермальных клеток, покрытое энтодермой и называемое яйцевым цилиндром. Внезародышевые клетки также продолжают пролиферировать и дифференцироваться. Зародыши, гомозиготные по аллелю tw5, доходят до стадии, похожей на яйцевой цилиндр, после чего клетки зародышевой эктодермы подвергаются пикнозу и гибнут. Клетки внезародышевой эктодермы, по-видимому, остаются незатронутыми и на протяжении нескольких дней продолжают нормально развиваться, несмотря на находящийся внутри мертвый зародыш, но в конце концов также гибнут.
На этой стадии развития мышиного зародыша, достигаемой через 6,5-7 сут после оплодотворения, начинается дифференцировка собственно зародыша. Это проявляется в формировании на яйцевом цилиндре первичной полоски и образовании между уже имеющимися зародышевыми эктодермой и энтодермой слоя мезодермальных клеток. У зародышей, гомозиготных по аллелю t9, нормальная мезодерма не образуется и соответственно не образуется ни одно из ее производных. Поскольку мезодермальные клетки образуются из зародышевой эктодермы в области первичной полоски, можно предположить, что мутантные эктодермальные клетки неспособны к такому превращению. Мутантные t9-зародыши, пересаженные в брюшную полость нормальных взрослых особей, образуют злокачественные опухоли, целиком состоящие из эктодермальных тканей.
Первичная полоска - это место образования трех зародышевых листков и развития первичной оси зародыша.
По обе стороны первичной оси на большей части ее длины образуются сомиты, а медиально по отношению к парным сомитам - хордомезодерма. Последняя индуцирует лежащую над ней нейральную эктодерму к формированию нервной трубки - структуры, которая в конечном итоге становится спинным мозгом, а на переднем конце головным мозгом. Все эти события происходят и у зародышей tw1. Однако после образования нервных структур вентральная часть нервной трубки и головной мозг у них дегенерируют. Сохраняющиеся дорсальные клетки физически замещают мертвые вентральные клетки, но, по-видимому, не могут заменить их функционально, потому что у этих мутантных зародышей всегда наблюдаются разного рода дефекты и они гибнут до рождения.
Конечное летальное состояние, обусловленное локусом Т, можно видеть у особей, гомозиготных по доминантному аллелю Т. Летальная фаза у этих особей сходна с наблюдаемой у мутантов tw1, т. е. она наступает позднее, чем в случае большинства других рецессивных аллелей. У особей Т/Т первичная полоска не достигает заднего конца зародыша. Поэтому ни одна из структур, зависящих от формирования мезодермы, в этой области никогда не развивается. Кроме того, что более важно, аллантоисная ножка плаценты у них не образуется, т.е. зародыш лишается необходимых для его жизни нормальных связей с плацентой. Вдобавок не развивается ни одна из структур самого зародыша, находящихся позади почек передних конечностей. Наконец, несмотря на, казалось бы, нормальный передний конец первичной полоски и на образование сомитов и хорды, эти последние структуры не сохраняются, а исчезают. В результате строение переднего конца зародыша оказывается сильно нарушенным.
Создается впечатление, что, хотя дефекты, наблюдаемые у этой галереи уродцев, развивающихся под действием мутаций в сложном локусе Т, очень разнообразны, все они имеют одну общую особенность. Как отметил Беннетт (Bennett), все летальные Т-аллели вызывают дефекты эктодермы. Эти дефекты выражаются в нарушении способности эктодермы мутантов либо нормально дифференцироваться (t12 и t0), либо нормально функционировать (tw73 и tw1). Описанные выше дефекты схематически представлены на рис. 7-12. Как показано на схеме, можно представить себе, что различные мутации локуса Т должны делать ряд последовательных выборов из двух возможностей, определяющих дальнейшую судьбу эктодермы и всех ее производных. Первоначально морула состоит из недифференцированных клеток. Мутация t12 препятствует принятию первого решения - выбору между трофобластом и внутренней клеточной массой. Затем мутация tw73 нарушает надлежащее функционирование трофобласта. Мутация t0 препятствует образованию внезародышевой эктодермы; ее эффект, возможно, аналогичен эффекту мутации t12. На параллельном этапе мутация tw5 убивает эктодерму собственно зародыша. Наконец, мутации t9, tw1 и Т нарушают различным образом либо способность зародышевой эктодермы дифференцироваться в мезодерму, либо способность мезодермы, если она уже образовалась, индуцировать или поддерживать нервную ткань.
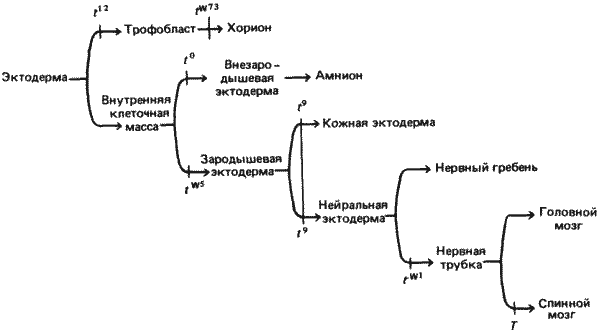
Рис. 7-12. Предполагаемая цепь последовательных решений, которые должны приниматься в процессе дифференцировки эктодермы и ее производных у мыши. Над стрелками указаны различные t-аллели, блокирующие соответствующие процессы.
Первичное нарушение, лежащее в основе всех этих далеко идущих эффектов всего лишь одного локуса, составляет в настоящее время предмет многочисленных споров и экспериментальных исследований. Однако, какова бы ни была непосредственная причина (или причины) этих дефектов, совершенно очевидно, что локус Т играет первостепенную роль в морфогенезе одного из трех зародышевых листков мышиного зародыша. Поэтому он, подобно локусу Notch у дрозофилы, принимает важное участие в развитии организма в целом.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Спонтанные мутации
Спонтанные мутации О внезапных изменениях наследственности знал еще Дарвин. Взгляните на рисунок, где изображены овцы. Слева овца нормальная, в центре и справа овца и баран с сильно укороченными ногами. Сперва появилось одно-единственное такое животное. Изменение
Глава 5 СОМАТИЧЕСКИЕ МУТАЦИИ
Глава 5 СОМАТИЧЕСКИЕ МУТАЦИИ В гл. 4 мы высказали предположение, что соматические мутации V-генов играли важную роль в эволюции иммунной системы позвоночных. Сформулируем теперь несколько вопросов и постараемся ответить на них. Вопрос первый: каким образом создается
Микробы и мутации
Микробы и мутации Рассказ о трансформации, трансдукции и конъюгации должен был убедить читателя, что микроорганизмы действительно могут изменять свою природу. Во всех рассмотренных случаях микробиологи использовали влияние генетического материала (ДНК) одних микробов
ВТМ помогает изучать мутации
ВТМ помогает изучать мутации Вирус табачной мозаики, который уже не раз помогал нам разгадать многие загадки жизни, предлагается и в качестве модели для изучения мутаций. ВТМ содержит рибонуклеиновую кислоту, которая, как мы увидим далее, выполняет ту самую генетическую
Мутации вирусов в лаборатории
Мутации вирусов в лаборатории Мы говорили о мутантах ВТМ, созданных природой. Сегодня нам известны уже и его лабораторные мутанты. Первые из них увидели свет в лаборатории Г. Шрамма.Шрамм в своих опытах исходил из возможности замены аминогруппы (—NH2) в молекуле цитозина
Хромосомные аномалии и мутации
Хромосомные аномалии и мутации Факты, которые мы приводили выше, известны ученым уже довольно давно. Сопоставлением и изучением этих фактов и занимается генетика — наука о явлениях наследственности и изменчивости. Основное положение менделевской генетики — учение о
Полезные мутации переключателей
Полезные мутации переключателей Устойчивость к ядам, вирусам, бактериям и прочим паразитам, защитная окраска, превращение опадающих семян в неопадающие — все это примеры простых адаптаций, для развития которых бывает достаточно одной-двух удачных мутаций, поддержанных
6.1. Органогенез и системогенез
6.1. Органогенез и системогенез В отличие от концепции органогенеза, постулирующей поэтапное развитие отдельных морфологических органов, которые выполняют соответствующие локальные «частные» функции, концепция системогенеза утверждает, что гетерохронии в закладках и
5.1. Мутации
5.1. Мутации Теория мутаций составляет одну из основ генетики. Ее основные положения были разработаны голландским ученым Г. де Фризом еще в начале XX в.Мутации – это наследственные изменения генетического материала. Они характеризуются как редкие, случайные,
Органогенез и гистогенез
Органогенез и гистогенез Органогенез – это процесс образования органов в результате прогрессирующей дифференцировки клеток. Процесс органогенеза всегда сопровождается параллельным процессом образования тканей – гистогенезом. Процессы формирования тканей и органов
Мутации
Мутации Мутация — внезапное изменение гена. Она проявляется в первом же поколении потомков, если мутантный ген будет доминантным. Но рецессивный ген — мутант может скрытно наследоваться в течение нескольких поколений до тех пор, пока в родительскую пару не подберутся
Мутации с материнским эффектом
Мутации с материнским эффектом У таких разных организмов, как морские ежи и лягушки, события, происходящие на ранних стадиях дробления, и, в сущности, большая часть, если не все развитие, предшествующее гаструляции, не зависят от генома зиготы. Информацию, необходимую для
Гомеозис и гомеозисные мутации
Гомеозис и гомеозисные мутации Действие генов теснейшим образом связано с онтогенезом, и эта их связь выявляется при возникновении мутаций, которые резко прерывают развитие организма. Существуют, однако, мутации другого класса, которые изменяют процесс онтогенеза, но
8.2. Мутации
8.2. Мутации Если бы организмы развивались поколение за поколением в одних и тех же окружающих условиях и передавали своему потомству все время одни и те же гены, сочетание эффектов генетической наследственности и морфического резонанса привело бы к бесконечному