12. Polycomb и Trithorax
К числу основных эффекторов, способных передавать сигналы к хроматиновой матрице и участвовать в поддержании клеточной идентичности (т. е. обеспечивать клеточную память), относятся члены групп генов PcG и trxG (Ringrose and Раго 2004). Эти гены были открыты у Drosophila благодаря их роли в регуляции кластера генов Нох в ходе развития и регуляции гомейотических генов. С тех пор было показано, что PcG и trxG являются ключевыми регуляторами пролиферации клеток и клеточной идентичности у многоклеточных эукариот. Кроме того, эти группы генов участвуют в нескольких сигнальных каскадах, которые реагируют на митогены и морфогены; регулируют идентичность и пролиферацию стволовых клеток, яровизацию у растений, гомеотические трансформации и трансдетерминацию, коммитирование линий в ходе дифференцировки В- и Т-клеток и многие другие аспекты развития Metazoa (главы 11 и 12). Теперь мы обратимся вкратце к тому, что известно о том, как семейства PcG и trxG превращают связанные с развитием сигналы в «эпигенетическую память» через посредство структуры хроматина.
Группы белков PcG и trxG функционируют по большей части антагонистически: семейство белков PcG устанавливает «молчащее» состояние хроматина, а семейство белков обычно способствует генной активности. Молекулярная идентификация гена Рс, о котором известно, что он стабилизирует паттерны репрессии генов на протяжении нескольких клеточных генераций, обеспечила первые данные о молекулярном механизме клеточной или эпигенетической памяти Равным образом РС явился примером белка, содержащего хромодомен с высокой степенью сходства с хромодоменом ассоциированного с гетерохроматином белка НР1 (Раго and Hogness, 1991). Как упоминалось выше, хорошо доказано, что хромодомены являются специфическими модулями, связывающимися с метиллизином гистона (изображено на рис. 3.10). У Drosophila идентифицированы 20 генов PcG и, по меньшей мере, 15 разных генов trxG. Функциональные анализы показали, что эти группы генов составляют спектр разных белков, но, тем не менее, они высококонсервативны у эукариот. Гены PcG кодируют продукты, в число которых входят белки, связывающиеся с ДНК (например, YY1), энзимы, модифицирующие гистоны (например. EZH2), и другие репрессивные ассоциированные с хроматином факторы, которые содержат хромодомен, обладающий сродством к H3K27me3 (например, РС). Гены группы trxG кодируют транскрипционные факторы (например, GAGA, или Zeste), энзимы АТФ-зависимого ремоделинга хроматина (например, Brahma) и HKMTs, такие как Ash 1 и Trx (или его гомологи у млекопитающих, MLL, Setl и семейство MLL). В большинстве случаев семейства белков PcG и trxG функционируют как компоненты разнообразных комплексов, устанавливая стабильные хроматиновые структуры, которые облегчают экспрессию или сайленсинг генов, регулируемых в развитии (главы 11 и 12).
Несмотря на успехи последнего времени механизм, посредством которого комплексы, содержащие PcG или trxG, «нацеливаются» на регулируемые в развитии районы хроматина, еще не вполне выяснен У Drosophila наследуемая репрессия гена требует рекрутирования белковых комплексов PcG к элементам ДНК, называемым «элементы ответа polycomb» (PREs, polycomb response elements). Эквивалентные последовательности у млекопитающих установить не удалось. Неясно, каким образом белковые комплексы PcG вызывают протяженный сайленсинг зависимым от PRE образом, потому что PREs обычно локализованы на расстоянии килобаз от сайта старта транскрипции генов-мишеней. Можно постулировать, что отталкивание или, наоборот, рекрутирование комплексов PcG могут дискриминироваться изменениями в транскрипционной активности или различиями в продуктивном versus непродуктивном процессинге иРНК (Pirrotta, 1998; Dellino et al., 2004; Schmitt et al., 2005). В современных моделях поддерживается представление о связывании PcG через взаимодействие с белками, связывающимися с ДНК, и сродство хромодомена в белке PcG к модифицированным гистонам (H3K27me3) (Cao et al., 2002). Однако комплексы PcG могут также ассоциироваться in vitro с нуклеосомами, лишенными гистоновых хвостов (Francis et al., 2004) и, более того, элементы PRE имеют сниженную плотность нуклеосом (Schwartz et al., 2005). Наиболее логичное объяснение некоторых из этих не согласующихся друг с другом наблюдений заключается в том, что обычно связывание PcG in vivo первоначально нуждается во взаимодействии с факторами, связанными с ДНК, которое затем стабилизируется ассоциацией — с нуклеосомами и модифицированными H3K27me3 в прилегающем участке хроматина. Очевидно, необходимы дальнейшие исследования для того, чтобы связать существующие данные о том, как комплексы PcG «нацеливаются» на участки хроматина, и о том, каким образом они опосредуют репрессию. Вполне вероятно, что Это зависит от организма, поскольку имеет место большая гетерогенность комплексов PcG (глава 11).
Белки группы Trithorax поддерживают обычно активное состояние генной экспрессии в генах-мишенях и преодолевают сайленсинг, опосредованный PcG (или предотвращают его). Этот переход еще менее понятен, но последние данные позволяют предполагать, что некий, базирующийся на РНК, механизм мог бы служить триггером для рекрутирования Ashl к промоторам-мишеням (Sanchez-Eisner et al., 2006). Полагают, что в результате может происходить ряд временных и стабильных изменений в структуре хроматина, которые могут облегчаться межгенной транскрипцией, способной устанавливать открытый хроматиновый домен и опосредовать активное замещение гистонов В число документированных изменений хроматина входят вставка «активных» метальных меток по лизинам гистонов с помощью таких trxG HKMTs, как Trx и Ashl, и считывание этих меток (например, распознавание H3К4те с помощью WDR5; Wysocka et al., 2005). Требуется также действие зависимых от АТФ факторов ремоделинга хроматина, таких как Brahma, хотя еще предстоит определить, каким именно образом взаимосвязаны эти механизмы (детали см. в главе 12).
Многие белки PcG и trxG действуют кооперативно, поддерживая в нормальной клетке жестко контролируемый уровень репрессированного гетерохроматина по отношению к активному эухроматину. У млекопитающих в соматических интерфазных ядрах морфология ядер показывает, что конститутивные домены околоцентромерного гетерохроматина сгруппированы в 15–20 фокусов (рис 3.16). Дерегуляция клеточной судьбы и контроля пролиферации, приводящая к аномалиям развития и раку, нередко проявляется в аномальной морфологии ядер. Например, ядерная организация в клетках больных PML-лейкемией (родственной смешанной лимфоцитарной лейкемии [MLL]) демонстрирует отсутствие перицентромерных фокусов (Di Сгосе, 2005). В противоположность этому стареющие (непролиферирующие) клетки обнаруживают ядерную морфологию с крупными эктопическими кластерами гетерохроматина (Narita et al., 2003; Scaffidi et al., 2005). Таким образом, морфология ядер оказывается хорошим маркером, позволяющим различать нормальные и аберрантные клеточные состояния; это показывает, что архитектура ядра может, помимо всего прочего, играть регуляторную роль в поддержании специализированных доменов хроматина.
Изучение уровней модификации гистонов является еще одним индикатором нормальности или ненормальности клеток. Многие из этих изменений приписываются дерегуляции HKMTs группы PcG (например, Ezh2) или trxG (например, MLL), что вносит вклад в прогрессию и даже метастатический потенциал опухолей (см. раздел 15). Действительно, увеличение общих уровней содержания любого из вышеупомянутых белков связано с повышенным риском возникновения рака простаты, рака груди, множественной миеломы или лейкемии (Lund and van Lohuizen, 2004; Valk-Lingbeek et al., 2004). В других случаях неопластической трансформации имеют место явное снижение уровня репрессивных гистоновых меток и увеличение общего ацетилирования (Seligson et al., 2005), вызывающие повышение уровня транскрипции генов и нестабильности генома. Очевидно, что изменения в глобальном контроле хроматина, может быть через нарушение работы энзимов, модифицирующих гистоны, влияют на функциональность генома и нарушают специфический профиль экспрессии генов в нормальной клетке.
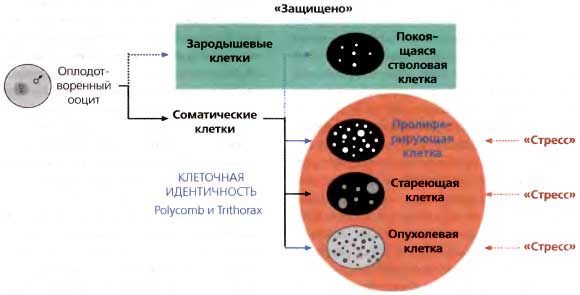
Рис. 3.16. Клеточная идентичность, определяемая белками PcG u trxG
В ходе эмбриогенеза устанавливаются два клеточных компартмента, различающихся по своему дифференцировочному потенциалу: это зародышевые клетки (тотипотентные) и соматические клетки (включая стволовые клетки) с ограниченными дифференцировочными потенциями. Пластичность потенциала экспрессии генома зародышевых или стволовых клеток отражается в сниженных уровнях репрессивных гистоновых меток, которые больше не видны в околоцентромерных фокусах. Нормальные пролиферирующие клетки обычно обладают ядерной морфологией с 15–20 гетерохроматиновыми фокусами. Комплексы, содержащие Polycomb и Trithorax, действуют, определяя эпигенетическую и, отсюда, клеточную идентичность разных линий. Они функционируют также в ответ на внешние «стрессорные» воздействия, стимулируя клеточную пролиферацию и соответствующую экспрессию генов. В стареющих клетках происходит утрата пластичности генома и пролиферационного потенциала, что находит свое отражение в аномально крупных гетерохроматиновых фокусах и в общем повышенном уровне репрессивных гистоновых меток. Однако интенсивно пролиферирующие опухолевые клетки обнаруживают изменения в балансе репрессивных и активирующих гистоновых меток через дерегуляцию модифицирующих гистоны энзимов PcG и trxG. Это сопровождается нарушениями ядерной морфологии
В случае клеточного старения увеличение уровня реперессивных меток гистонов также является индикатором клеточной дисфункции. Такое увеличение, сопровождаемое сниженным выявлением ацетилирования гистонов, может укрепить и даже повысить уровни «молчащего» хроматина, блокируя клеточную пластичность и направляя клетки в антипролиферативное состояние (Scaffidi et al., 2005). Это в значительной мере связанный с возрастом эффект, хотя особое болезненное состояние, прогерия, может преждевременно ускорять старение. Напротив, когда у мутантов, не имеющих трансдуцирующего энзима (Suv39h), снижается уровень репрессивных перицентромерных метальных меток, клетки обнаруживают повышенные скорости иммортализации, отсутствие старения и повышенную нестабильность генома (Braig et al., 2005). Эти примеры являются иллюстрацией того, что дерегуляция хроматина, которая проявляется в уровнях характерных гистоновых меток, часто трансдуцируемых энзимами PcG и trxG, и ядерная морфология оказываются важным индикатором прогрессии болезни.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК